
胰腺癌新药研发屡次失败,即使是制药巨头诺华也难迎曙光。
2023年8月25日,XOMA Corporation公司的SEC文件显示诺华制药Novartis致函XOMA 表示计划停止与TGF β单克隆抗体NIS793相关的研发活动。Novartis将停止其余正在进行的TGFβ临床研究中的患者招募工作,并将在这些研究结束后收集所有数据。Xoma在向SEC 提交的文件中写道:“有效性和安全性尚未确定,目前还不能保证NIS793能够投入商业使用。”

NIS793是一种完全人源且可能是同类首创(first-in-class)单克隆抗体,该药物通过阻断TGFβ细胞因子发挥作用,TGFβ细胞因子是一种参与许多癌症途径(包括转移、血管重塑和免疫逃避)的蛋白质。该候选药物此前曾于2021年7月获得FDA治疗胰腺癌的孤儿药称号。

诺华于2015年10月首次获得NIS793的使用权,当时诺华以3700万美元的预付款从Xoma购买了该资产,根据XOMA和Novartis之间的协议,NIS793里程碑的大约30%将作为XOMA对Novartis部分债务付款,剩余部分将以现金支付给XOMA。此外,XOMA有可能获得高达4.45亿美元的额外里程碑付款。若NIS793获得商业化监管批准,XOMA将获得一定百分比的销售分成。
早在2023年7月18日,Novartis在二季报中就宣布,根据获益-风险评估,其TGF-β抑制剂NIS793用于治疗转移性胰腺导管腺癌的Ⅲ期研究将停止,仅保留正在进行的针对结直肠癌的II期研究。

在结束其开发之前,诺华正在进行NIS793针对转移性胰腺导管腺癌(mPDAC)一线治疗的大规模临床III期试验(CTR20220174),在一线环境中测试该候选药物与吉西他滨和白蛋白结合型紫杉醇的组合,该药物曾有望成为较具潜力的mPDAC治疗策略。
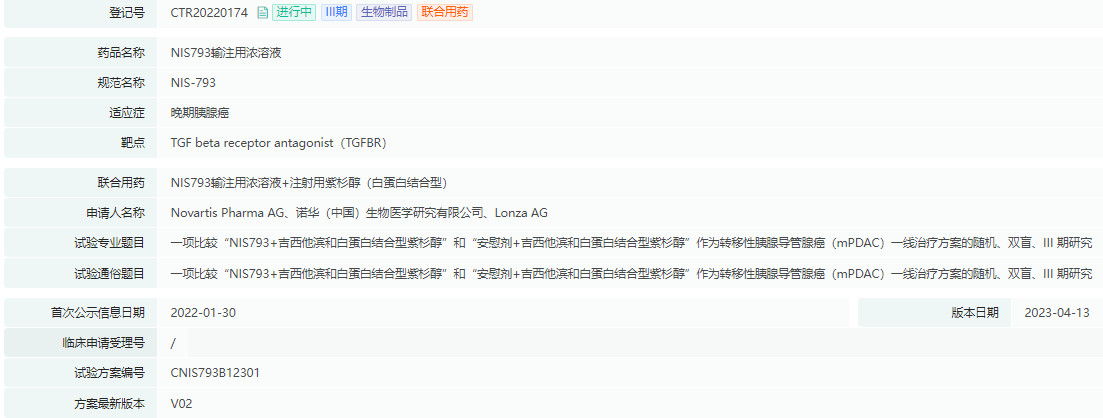
数据来源:药融云中国临床实验数据库
晚期新药冲刺
胰腺癌领域最近取得了重大进展。
2023年6月,Ipsen宣布FDA已接受其补充新药申请,寻求将Onivyde(伊立替康脂质体注射液)扩大到转移性胰腺导管腺癌的一线治疗。III期NAPOLI 试验的数据显示Onivyde 与白蛋白结合型紫杉醇和吉西他滨相比,总体生存率和无进展生存率显著提高。
2023年8月25日,Exelixis停止并提前揭盲了其针对晚期胰腺和胰外神经内分泌肿瘤(NET)的 III期CABINET试验。CABINET正在经治晚期胰腺和胰腺外NET患者中评估卡博替尼(cabozantinib)与安慰剂相比的疗效和安全性。在两个试验队列中,卡博替尼显著延长了患者的无进展生存期(PFS)。详细研究结果将在即将召开的医学会议上公布,并递交FDA进行讨论。
参考资料:
1.公司官网
2.药融云数据库
<END>
要解锁更多企业药品研发信息吗?查询药融云数据库(vip.pharnexcloud.com/?zmt-mhwz)掌握药品各国上市情况、药品批文信息、销售情况与各维度分析、市场竞争格局、一致性评价情况、集采中标情况、药企申报审批信息、最新动态与前景等,以及帮助企业抉择可否投入时提供数据参考!注册立享15天免费试用!

















































 浙公网安备33011002015279
浙公网安备33011002015279 本网站未发布麻醉药品、精神药品、医疗用毒性药品、放射性药品、戒毒药品和医疗机构制剂的产品信息
本网站未发布麻醉药品、精神药品、医疗用毒性药品、放射性药品、戒毒药品和医疗机构制剂的产品信息
收藏
登录后参与评论
暂无评论