近日,国家药监局官网显示,恒瑞医药自主研发的1类新药抗PD-L1单抗——阿得贝利单抗注射液(SHR-1316)获批上市(受理号:CXSS2200006)。根据恒瑞医药早先新闻稿,该药本次获批的适应症为:联合化疗一线治疗广泛期小细胞肺癌(ES-SCLC)。据悉,这是国内获批上市的第5款PD-L1单抗,也是国产的第3款PD-L1单抗。

来源:NMPA官网
一、国产首个小细胞肺癌PD-L1单抗,恒瑞医药为患者带来新选择
肺癌是我国目前发病率和死亡率均排名第一的恶性肿瘤。小细胞肺癌(SCLC)约占肺癌总体发病率的15%左右,是一种侵袭性强、高级别肺神经内分泌肿瘤,其分化程度低,恶性程度高,生长迅速,侵袭力强,容易耐药,且较早发生转移,预后较差。小细胞肺癌分为局限期和广泛期,约70%的患者初诊时已经为广泛期。广泛期小细胞肺癌(ES-SCLC)作为高侵袭性恶性肿瘤,治疗选择有限,为患者带来沉重的疾病负担。ES-SCLC存在巨大的未被满足的医疗需求。
阿得贝利单抗是恒瑞医药自主研发的人源化抗PD-L1单克隆抗体,能通过特异性结合PD-L1分子从而阻断导致肿瘤免疫耐受的PD-1/PD-L1通路,重新激活免疫系统的抗肿瘤活性,从而达到治疗肿瘤的目的。历经艰辛探索和潜心钻研,阿得贝利单抗正式获批上市,验证了在我国小细胞肺癌患者中的价值,交出一份治疗ES-SCLC的“中国方案”。作为中国首个自主研发的获批小细胞肺癌适应症的PD-L1单抗,阿得贝利单抗将为患者带来全新治疗选择。

截图来源:药融云全球药物研发数据库
此次阿得贝利单抗获批上市是基于吉林省肿瘤医院程颖教授和中国医学科学院肿瘤医院王洁教授共同牵头开展的一项多中心、随机、安慰剂对照的III期研究——CAPSTONE-1的成功。该试验由全国49家中心共同参与,入组462例受试者,按照1:1随机入组,分别接受阿得贝利单抗或安慰剂联合依托泊苷和卡铂,每3周给药1次,完成4-6个周期联合治疗后,进入阿得贝利单抗或安慰剂维持治疗,直至疾病进展、毒性不可耐受或其他需要终止治疗的情况。
该研究显示,相较于安慰剂联合化疗组,阿得贝利单抗联合化疗可显著改善患者的总生存期(OS)达15.3个月,降低死亡风险达28%,2年生存率达31.3%,且具有可控的安全性。研究结果表明:阿得贝利单抗联合化疗显著延长患者的中位OS(15.3个月vs. 12.8个月),降低28%的疾病进展死亡风险,2年OS率达31.3%(对照组17.2%)。这一突破性成果也于2022年5月在线发表于国际权威学术期刊《柳叶刀·肿瘤学》杂志,获得国内外学界的广泛认可。
据药融云数据库,除此次获批的小细胞肺癌适应症外,阿得贝利单抗仍在继续深入探索其他适应症。在肺癌领域中,同样由程颖教授牵头的阿得贝利单抗用于局限期小细胞肺癌的Ⅲ期临床研究正在开展,另一项由吴一龙教授牵头的针对可切除的II-III期非小细胞肺癌围手术期治疗的III期临床研究也正在进行中。此外还有多项临床研究正在推进,以评估阿得贝利单抗在各类实体肿瘤的抗肿瘤作用。
阿得贝利单抗中国临床试验情况

截图来源:药融云中国临床试验数据库
二、PD-L1成热门靶点TOP1,国内共上市5款PD-L1单抗
据药融云《中国I类新药靶点白皮书》统计,2022年,我国1类新药合计受理1239个,其中化学药757个、生物药482个,涉及靶点总计311个(数据截至2022年11月30日,不含中药和原料药数据)。热门靶点的竞争愈发激烈,相信随着资源投入的增多,热门靶点的开发程度将飞速提高。肿瘤领域仍是新药研发最热门的疾病领域,涉及的靶点和药品数量仍高居榜首。肿瘤相关靶点排名靠前的有PD-1/L1、CTLA4和PI3Kδ(《2022年PD-L1新药受理数量增至76个!超越EGFR成为热门靶点TOP1!》)。
其中,后来居上的PD-1/L1,是最近几年最热门的靶点之一,上市品种均为新药,多家知名药企纷纷入局厮杀。2022年的热门靶点TOP6分别是:PD-L1、HER2、PD-1、EGFR、CD3、TIGIT ,PD-L1超越EGFR成为热门靶点TOP1。由此可见,PD-L1受众多药企追捧,研发赛道异常火热,且不乏还有药企持续入局,内卷严重,国内市场已经趋近饱和。
I类新药热门靶点变迁(按药品名称计数,2017-2022)

截图来源:药融云《中国I类新药靶点白皮书》
至此,国内共获批上市了5款PD-L1单抗,分别是阿斯利康的度伐利尤单抗、罗氏的阿替利珠单抗、康宁杰瑞生物的恩沃利单抗、基石药业的舒格利单抗、以及此次恒瑞医药的阿得贝利单抗,其中后3款为国产PD-L1单抗,累计批准的适应症达10个。据药融云统计,2021年院内PD-L1单抗的销售额为3.09亿元,市场由阿斯利康(60.52%)与罗氏(39.48)平分秋色。随着国内越来越多的PD-L1单抗陆续获批,市场规模将会持续扩大,份额也将会被更多药企瓜分。
PD-L1单抗院内销售情况
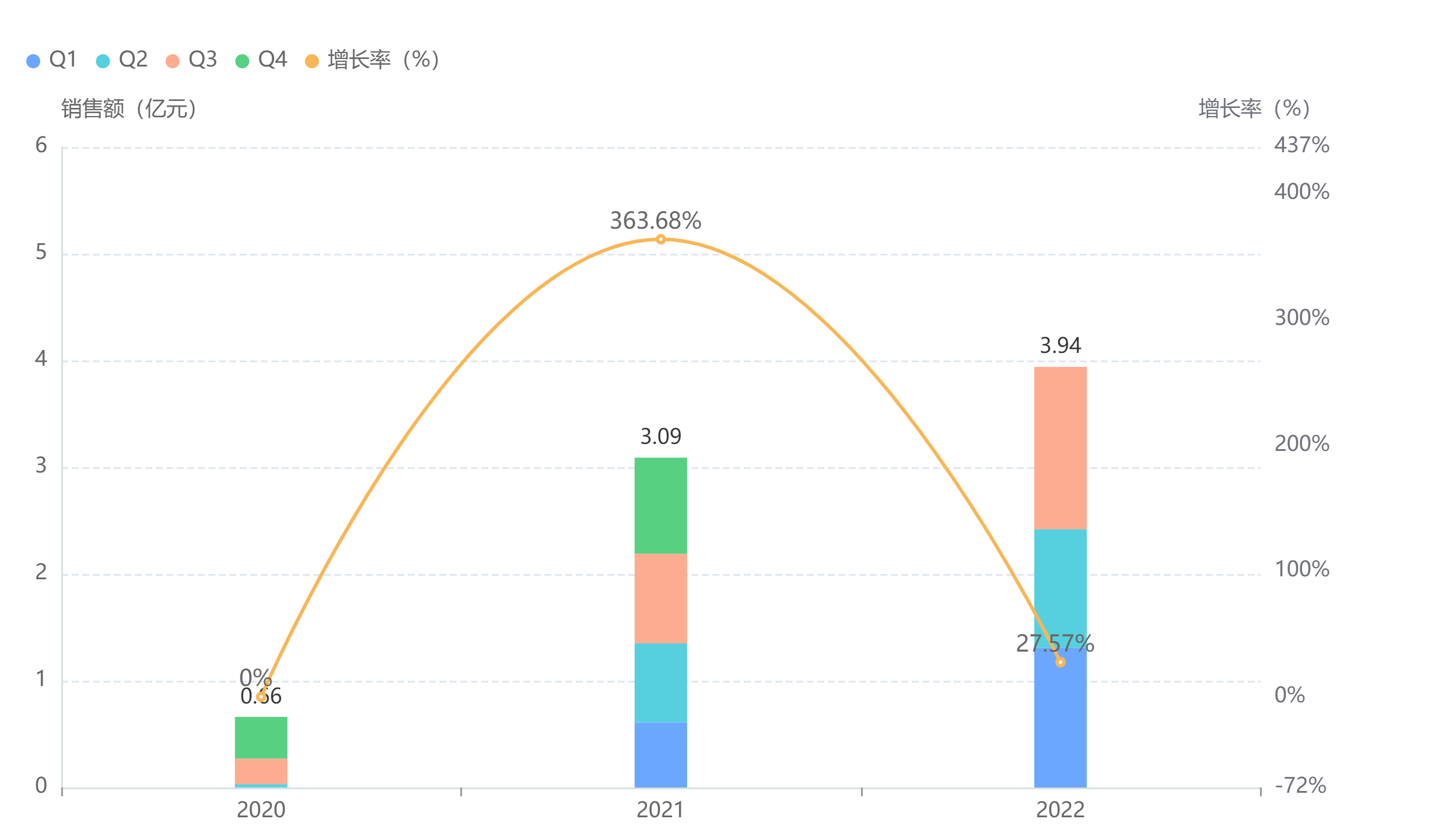
截图来源:药融云全国医院销售数据库
另外,正大天晴的TQB-2450、李氏大药厂的首克注利单抗(socazolimab)、和铂医药/四川科伦药业的泰特利单抗(tagitanlimab)也已递交了上市申请,现均在审评审批中,谁能成为国产第4家获批上市的PD-L1单抗呢,让我们拭目以待。
国产PD-L1单抗申请新药上市审评情况(红框内为在审评审批中)
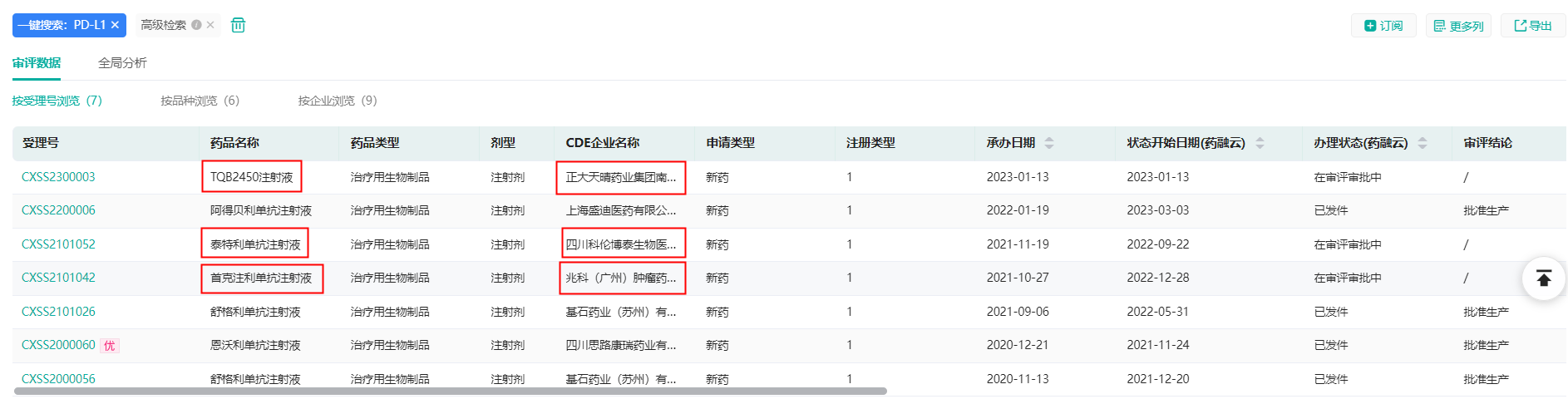
截图来源:药融云中国药品审评数据库
三、总结
随着阿得贝利单抗的上市,“创新药一哥”恒瑞医药在中国获批上市的创新药已达到12个,此前上市的11个创新药已全部纳入国家医保目录;公司引进的创新药林普利塞也已获批上市;此外还有60多个创新药正在临床开发,260多项临床试验在国内外开展。同时,恒瑞医药近年来大力推进科技创新和国际化战略,在全球多个国家和地区设立研发中心,积极拓展海外市场,目前已有多个国际多中心临床项目迎来重要节点。恒瑞医药在国内外布局的新药研发管线,未来将会陆续开花结果。
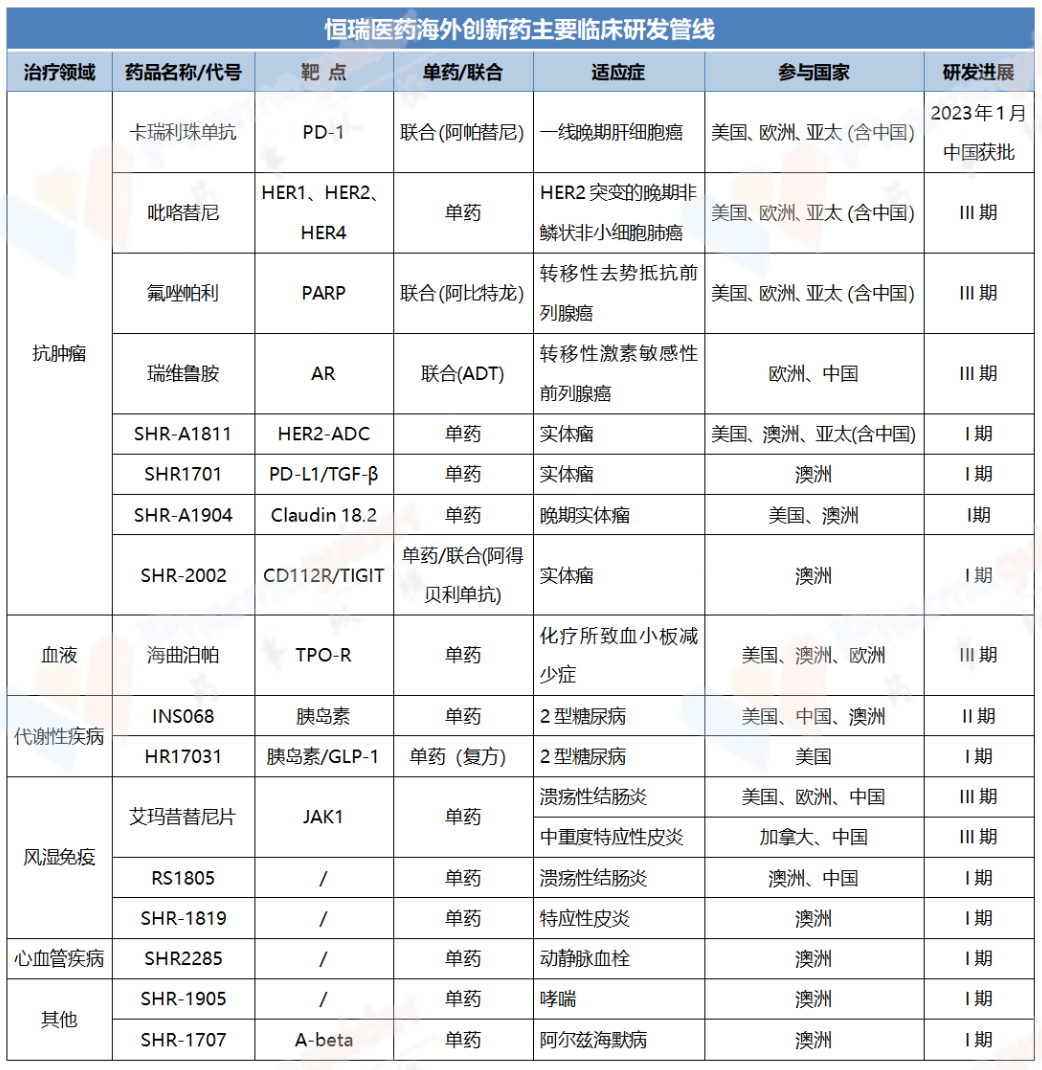
参考资料:
[1] NMPA官网
[2] 药融云数据库
[3] 恒瑞医药官方发布
想要解锁更多药物研发信息吗?查询药融云数据库(vip.pharnexcloud.com/?zmt-mhwz)掌握药物基本信息、市场竞争格局、销售情况与各维度分析、药企研发进展、申报审批情况、最新市场动态、市场规模与前景等,以及帮助企业抉择可否投入时提供数据参考!注册立享15天免费试用!

<END>























































 川公网安备51019002008863号
川公网安备51019002008863号 本网站未发布麻醉药品、精神药品、医疗用毒性药品、放射性药品、戒毒药品和医疗机构制剂的产品信息
本网站未发布麻醉药品、精神药品、医疗用毒性药品、放射性药品、戒毒药品和医疗机构制剂的产品信息
收藏
登录后参与评论
暂无评论