本以为1+1>2,却没想到1+1<1。这句话用在罗氏的Tecentriq(atezolizumab)和Exelixis的Cabometyx(cabozantinib)的抗癌组合进行的III期试验结果再合适不过。
近日,罗氏和Exelixis合作的第二个III期试验CONTACT-03显示:Tecentriq/Cabometyx组合未能达到肾细胞癌(RCC)无进展生存期的主要终点,宣告III期试验再次失败。与单独使用Cabometyx相比,Tecentriq/Cabometyx组合未能显著改善局部晚期或转移性透明细胞rcc或非透明细胞rcc患者的无进展生存期。此次试验共招募了522名患者。
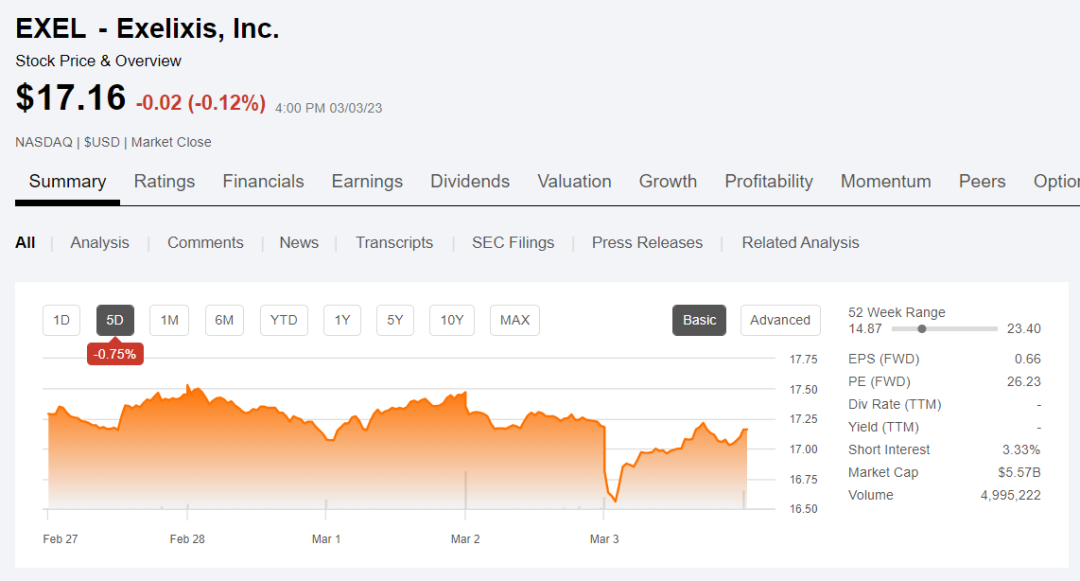
受此次III期试验再次失败的影响,Exelixis周四股价一度下跌近9%,周五上午价格下跌约4%。
01.Tecentriq
作为罗氏旗下的PD-L1产品,Tecentriq2022年销售额达到37亿瑞士法郎,同比增长14%。
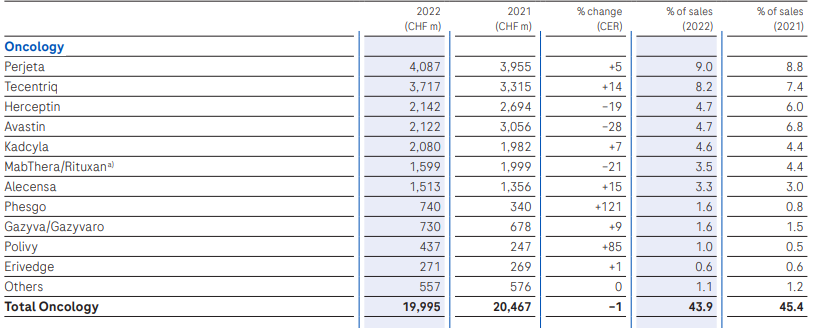
截图来源:罗氏2022财报
据药融云数据库显示,Tecentriq最早于2016年5月获FDA批准,现已有13个适应症上市。2020年2月,罗氏在中国递交的Tecentriq新药上市申请获批进口,首次进入国内市场,中文名阿替利珠单抗,后又陆续增加新的适应症获批,截止目前共有5个适应症上市。
Tecentriq适应症研发现状(部分)
截图来源:药融云全球药物研发数据库
02.Cabometyx
Cabometyx是一种酪氨酸激酶抑制剂(TKI),通过靶向抑制MET、VEGFR2 及RET信号通路而发挥抗肿瘤作用,能够杀死肿瘤细胞,减少转移并抑制血管生成。
Cabometyx在肾癌治疗中已经很成熟,它与Opdivo作为一线治疗用于晚期肾癌患者。它还作为肝癌和甲状腺癌的二线治疗药物上市销售。在商业销售和与Ipsen合作的收入上, 2022年Cabometyx为Exelixis带来了14亿美元的收入。
据药融云数据库显示,Cabometyx首次上市是在2013年1月24日,美国FDA批准其用于治疗甲状腺髓样癌。截止目前,已在60个国家陆续获得批准,但还尚未进入国内。然而,Cabometyx可能在未来几年面临仿制药竞争,因为其主要“物质组成”专利将于2026年到期,但其知识产权可能会将独占期延长至2033年。
Cabometyx各国上市时间轴(部分)
截图来源:药融云全球药物研发数据库
总结
其实,早在2017年,罗氏和Exelixis便开始临床试验合作。此次试验是Exelixis一直在进行的三项联合研究之一,其中两项试验均以失败告终。除了此次III期试验失败,还有去年12月,Cabometyx/Tecentriq方案在接受免疫疗法和化疗后进展的非小细胞肺癌患者的试验中也失败了。另外一项针对前列腺癌的3期试验预计今年晚些时候公布结果。
此次试验的失败,导致Cabometyx在关键专利到期前进一步扩大适应症的机会落空。而Tecentriq/Cabometyx抗癌组合III期试验再次失败,可能会支持Cabometyx成为肾癌最合适的酪氨酸激酶抑制剂。
参考资料:
[1]Exelixis官网
[2] 药融云数据库
[3]https://www.fiercepharma.com/pharma/roche-exelixis-tecentriq-cabometyx-pair-fails-again-time-kidney-cancer
[4]https://www.biopharmadive.com/news/Exelixis-cabometyx-tecentriq-kidney-cancer/644104/
想要解锁更多药物研发信息吗?查询药融云数据库(vip.pharnexcloud.com/?zmt-mhwz)掌握药物基本信息、市场竞争格局、销售情况与各维度分析、药企研发进展、申报审批情况、最新市场动态、市场规模与前景等,以及帮助企业抉择可否投入时提供数据参考!注册立享15天免费试用!

<END>






















































 川公网安备51019002008863号
川公网安备51019002008863号 本网站未发布麻醉药品、精神药品、医疗用毒性药品、放射性药品、戒毒药品和医疗机构制剂的产品信息
本网站未发布麻醉药品、精神药品、医疗用毒性药品、放射性药品、戒毒药品和医疗机构制剂的产品信息
收藏
登录后参与评论
暂无评论