
近日,经国家药监局审查,批准佰奥达生物科技(武汉)股份有限公司、基蛋生物科技股份有限公司和泰普生物科学(中国)有限公司3个企业的3个新冠病毒抗原检测试剂产品。截至目前,NMPA已批准39个新冠病毒抗原检测试剂产品。
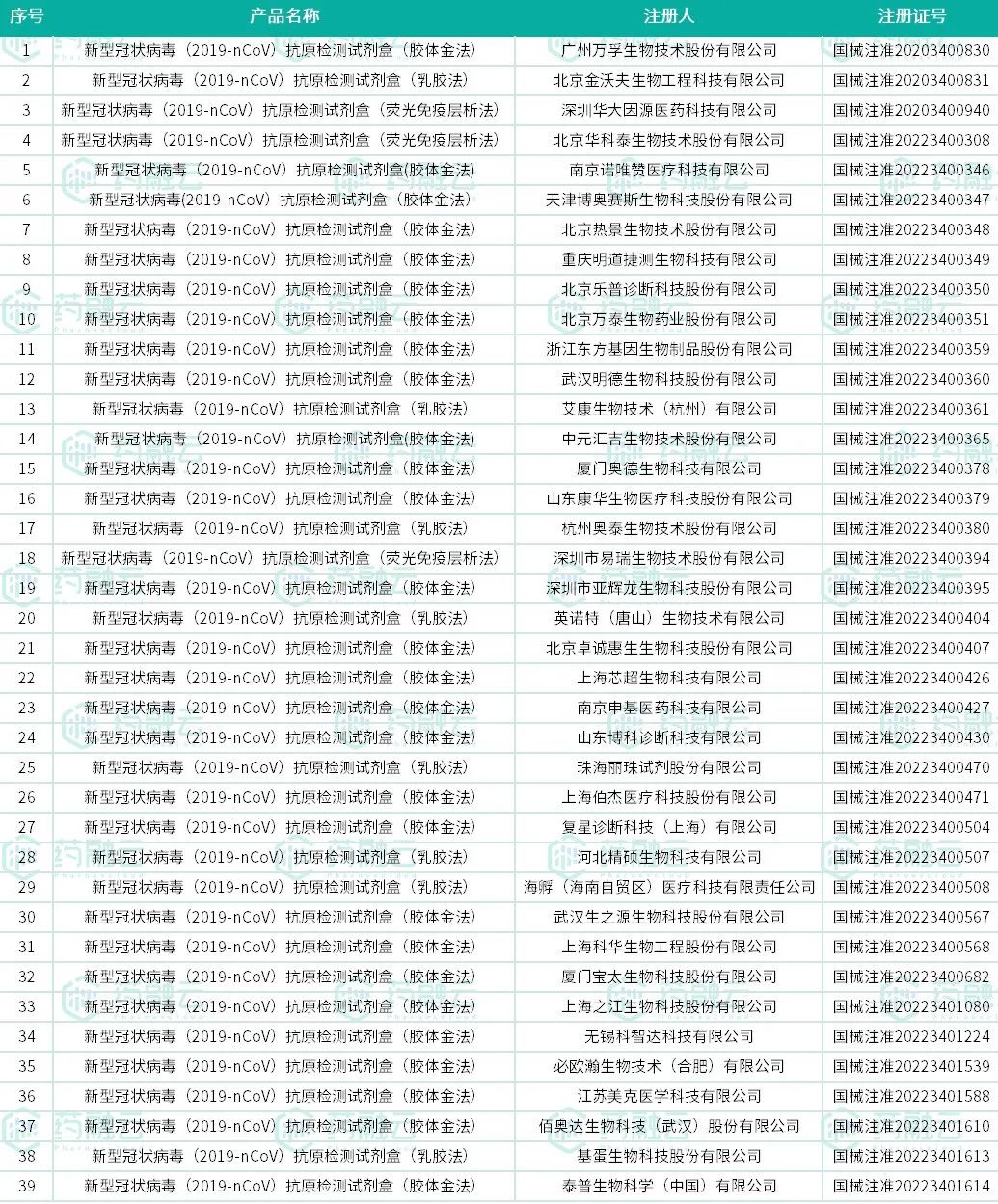
药融云公众号(yrydata)后台回复关键词“抗原”,可下载此表格文件
获批的39个新冠病毒抗原检测试剂,涉及多家上市公司或者其相关子公司,如万孚生物(300482)、「华大基因」的子公司深圳华大因源医药科技有限公司、万泰生物(603392)、亚辉龙(688575)、「丽珠医药集团」的子公司珠海丽珠试剂股份有限公司、「复星医药」的子公司复星诊断科技(上海)有限公司等。药品监督管理部门将加强相关产品上市后监管,保护患者用械安全。
12款新冠疫苗陆续获批上市!mRNA新冠疫苗还在路上
在2022年12月4日15时至5日16时,25小时内,四款新冠疫苗宣布获批紧急使用。其中三款重组蛋白类疫苗,分别由神州细胞、三叶草生物、威斯克生物研发;另有一款鼻喷流感病毒载体新冠疫苗,由万泰生物研发。
加上本月新获批的四款,国内现共有12款新冠疫苗可供选择,包括5款灭活疫苗、4款重组蛋白疫苗、1款腺病毒针剂、1款吸入用重组新型冠状病毒疫苗和1款鼻喷流感病毒载体疫苗。在疫情政策发生重大变化的情况下,进一步通过异源加强针疫苗的注射加强人群保护,对保护人民生命健康安全具有重要意义。
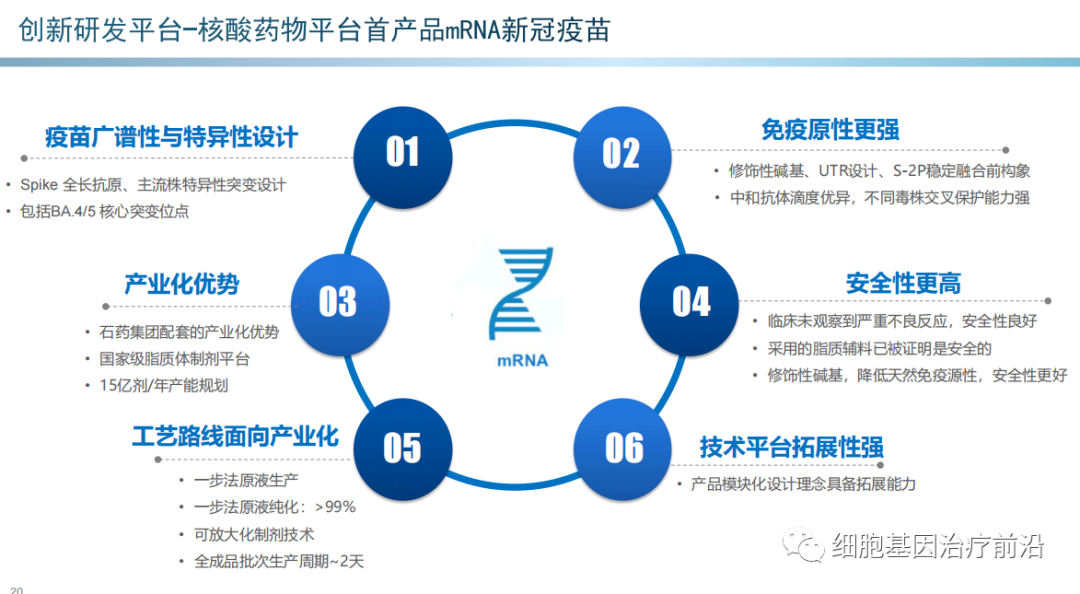
至于大家都非常关心mRNA新冠疫苗,近期也迎来了许多进展,国内首个mRNA新冠疫苗或将迎来上市,且很有可能花落石药集团(01093.HK)。据石药集团发布的三季报显示,其mRNA新冠疫苗SYS6006的1、2期临床试验及序贯加强免疫的临床研究报告均已上交CDE,且公司近期应疫苗专班要求提交了紧急使用报告。目前公司跟监管部门沟通顺利,在CDE有阶段性评审结果之后将以论文或会议形式陆续发布临床数据。
此外,复星医药/BioNTech的mRNA新冠疫苗目前在国内正处审批阶段。公司三季报显示,2022年,复必泰(mRNA新冠疫苗)持续推进在港澳台地区的接种及新剂型注册,针对奥密克戎BA.4/BA.5的二价疫苗也于2022年10月获批中国台湾地区紧急使用、还已在港澳地区分别递交了紧急使用/特別进口申请。
沃森生物:mRNA新冠疫苗目前国内处于III期。2022年9月30日公司新型冠状病毒mRNA疫苗获得印度尼西亚紧急使用授权(“EUA”),系我国自主研发的首个获批海外上市的新冠mRNA疫苗,用于18岁及以上人群基础免疫或加强免疫。公司还在积极布局mRNA技术平台:和蓝鹊生物合作的新冠变异株mRNA疫苗正在滚动提交临床申请资料;和艾博生物合作的带状疱疹mRNA疫苗、和蓝鹊生物合作的RSV mRNA疫苗和流感mRNA疫苗、和圣诺合作的通用流感siRNA药物处于临床前研究。
艾博生物:2020年1月mRNA新冠疫苗项目ARCoV立项,当年6月获得国内首个IND批文,2021年9月启动国际多中心III期临床,目前正在等待揭盲,有望于2022年底申报上市。
斯微生物:mRNA新冠疫苗2021年1月获批 IND,目前处于II期临床。2017年7月,公司获得康奈尔大学休斯顿卫理公会医院沈海法教授发明的mRNA递送技术——脂质多聚物纳米载体技术平台(LPP/mRNA)相关专利的全球独家授权。LPP递送载体可规避LNP的专利纠纷风险,有望带来差异化疗效。
......
根据药融云数据(vip.pharnexcloud.com/?zmt-mhwz)显示,目前国内mRNA新冠疫苗研发企业还有沃森生物、斯微生物、康希诺、艾博生物、艾美疫苗、石药斯微生物、瑞科生物、海昶生物、天境生物、嘉晨西海、美诺恒康、丽凡达生物、星亢原、蓝鹊生物、深圳瑞吉生物、云顶新耀、厚存纳米、深信生物、传信生物等。现在以及未来还将会有越来越多的药企加入,为防疫保驾护航。
想要解锁更多药物研发信息吗?查询药融云数据库(vip.pharnexcloud.com/?zmt-mhwz)掌握药物基本信息、市场竞争格局、销售情况与各维度分析、药企研发进展、申报审批情况、最新市场动态、市场规模与前景等,以及帮助企业抉择可否投入时提供数据参考!注册立享15天免费试用!

—END—






















































 川公网安备51019002008863号
川公网安备51019002008863号 本网站未发布麻醉药品、精神药品、医疗用毒性药品、放射性药品、戒毒药品和医疗机构制剂的产品信息
本网站未发布麻醉药品、精神药品、医疗用毒性药品、放射性药品、戒毒药品和医疗机构制剂的产品信息
收藏
登录后参与评论
暂无评论