
近日,Oyster Point Pharma (纳斯达克代码:OYST)宣布与晖致公司(Viatris Inc.,纳斯达克代码:VTRS)达成协议,根据该协议,晖致将收购Oyster Point Pharma。该交易表明了晖致打算专注并大力投资眼科疾病的战略计划,本次收购将为晖致提供具有强大竞争力的眼科治疗产品。
根据协议条款,晖致公司将以每股11.00美元的现金在收盘时收购Oyster Point Pharma所有已发行的股票,加上一项或有价值权利(CVR),即在Oyster Point Pharma实现指定的2022年全年绩效目标(Oyster Point Pharma的净产品收入为2400万美元或以上,Tyrvaya的处方总计为146469份)后,可能获得最高每股2美元的现金付款。
晖致公司的首席执行官Michael Goettler表示:“Oyster Point Pharma为晖致带来了伐尼克兰溶液(Tyrvaya)鼻腔喷雾剂的优势,这是第一种也是唯一一种治疗干眼症症状的鼻腔喷雾剂。Oyster Point Pharma还给我们带来了专注于眼部护理的产品管线,以及一支在临床,医学,监管和商业等角度对眼科领域拥有丰富经验的团队。我们相信,我们正在为下一任全球眼科领导者奠定基础,加速解决眼科疾病患者的需求,并为晖致的前进发展做好准备。”
关于Oyster Point Pharma
Oyster Point Pharma是一家商业化阶段的生物制药公司,专注于发现,开发和商业化治疗眼科疾病的首创药物(first-in-class)疗法。据药融云数据库显示,2021年10月,FDA批准了该公司的用于治疗干眼症体征和症状的伐尼克兰溶液(Tyrvaya)鼻腔喷雾剂,该药目前在中国正在开展临床3期试验。Oyster Point Pharma也一直在对角膜炎的适应症进展开发,现进展到临床2期。
varenicline tartrate研发现状
截图来源:药融云全球药物研发数据库
Oyster Point Pharma拥有不断增长的临床和临床前项目,并通过内部创新和外部合作继续扩大其研发渠道。
Oyster Point Pharma研发管线
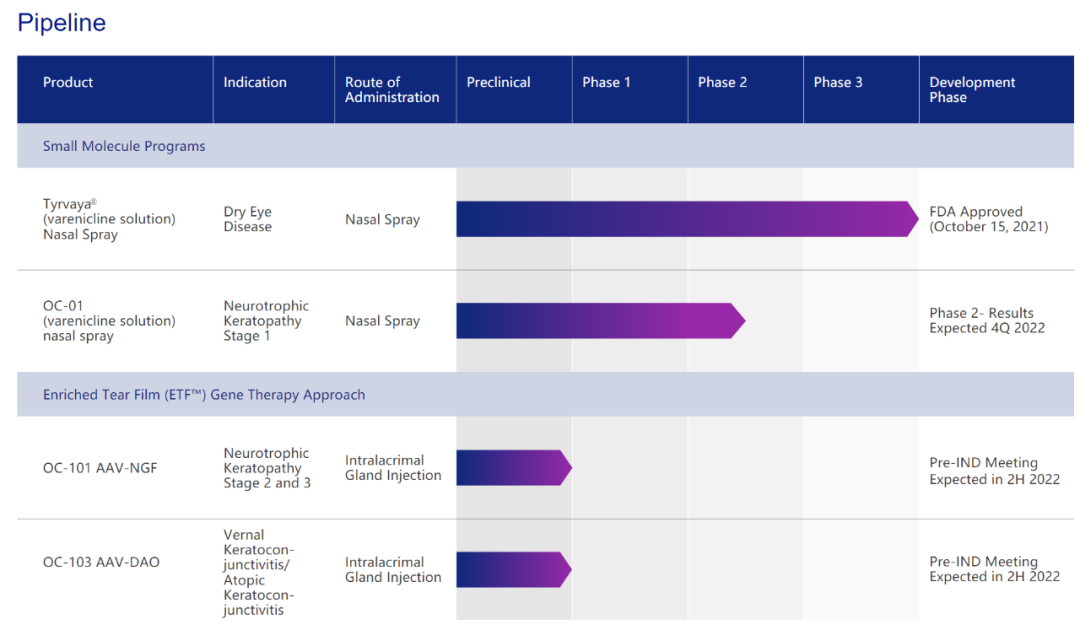
截图来源:Oyster Point Pharma官网
关于晖致(Viatris)
2020年11月16日,随着迈蓝(Mylan N.V.)和辉瑞旗下的业务部门辉瑞普强(Pfizer Upjohn)的成功合并,晖致公司正式成立。由这两家优势互补的公司合并成的晖致具备科学、生产和分销专业知识,以及成熟的注册、医疗和全球商业能力,为超过165 个国家和地区的患者提供优质药物。
晖致作为一家全新的全球医疗健康公司,其使命是帮助世界各地的人们在生命的每个阶段生活得更加健康,并通过三大途径践行使命:为世界各地患者提供值得信赖的优质药物;促进可持续性的运营及创新解决方案,改善患者健康;利用多方面的专业能力将人们与产品和服务相连接。
信息参考:
[1] Oyster Point Pharma官网
[2] 药融云数据库
想要解锁更多药企信息吗?查询药融云数据库(vip.pharnexcloud.com/?zmt-mhwz)掌握药企公司基本信息、投融资情况、产品管线分布、药物销售情况与各维度分析、药物研发信息、仿制药布局情况、最新进展动态、临床试验信息、市场规模与前景等,以及帮助企业抉择可否投入时提供数据参考!注册立享15天免费试用!

<END>






















































 川公网安备51019002008863号
川公网安备51019002008863号 本网站未发布麻醉药品、精神药品、医疗用毒性药品、放射性药品、戒毒药品和医疗机构制剂的产品信息
本网站未发布麻醉药品、精神药品、医疗用毒性药品、放射性药品、戒毒药品和医疗机构制剂的产品信息
收藏
登录后参与评论
暂无评论