
2019年2月,强生(JNJ)旗下杨森制药与临床阶段基因治疗公司MeiraGTx Holdings达成了全球合作和许可协议,开发、制造和商业化其临床阶段遗传性视网膜疾病资产(包括先导疗法),用于治疗由CNGB3或CNGA3基因突变导致的全色盲和X-连锁视网膜色素变性( XLRP )。

6月28日,强生公司和英国生物技术公司 MeiraGTx 表示,正在开发的一种用于遗传性眼病的实验性基因疗法安全的且耐受性良好,并且在早期临床试验中显示出改善视觉功能的初步迹象。令人鼓舞的是,在治疗后六个月,与对照组相比,接受 botaretigene sparoparvovec 治疗的患者的视网膜、视觉功能和功能性视力都有显着改善。
botaretigene sparoparvovec药物信息
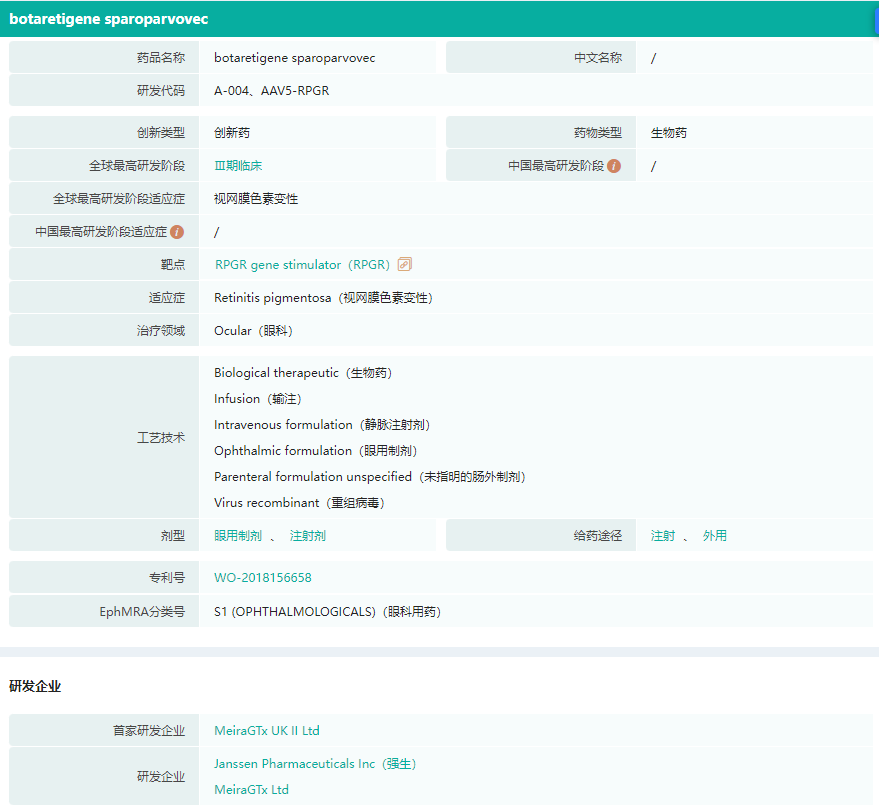
截图来源:药融云全球药物研发数据库(新版)
该治疗旨在纠正一种严重的眼部疾病视网膜色素变性,在 1/2 期研究中,共对45 名参与botaretigene sparoparvovec多个剂量的测试,在 MGT009 研究的剂量递增和扩展阶段,与 6 个月时的同期对照组相比,接受低剂量和中剂量 botaretigene sparoparvovec 治疗的患者的视力有所改善。
同时, MeiraGTx 和强生公司用于 XLRP 的 botaretigene sparoparvovec 的 3 期研究正在积极地进行患者给药。3期研究主要测试患者的功能性视力和视网膜敏感度的变化,详细的试验数据将在未来的医学会议上报告。
MeiraGTx 说,试验研究人员报告的大多数副作用与手术分娩过程有关,而添加预防性类固醇方案可减少炎症反应。
另外,据药融云数据库查询,botaretigene sparoparvovec在此前已先后陆续获得多项特殊审批,包括先进的药物治疗方法 、FDA快速通道、孤儿药、EMA优先药物等。
botaretigene sparoparvovec获得的特殊审批
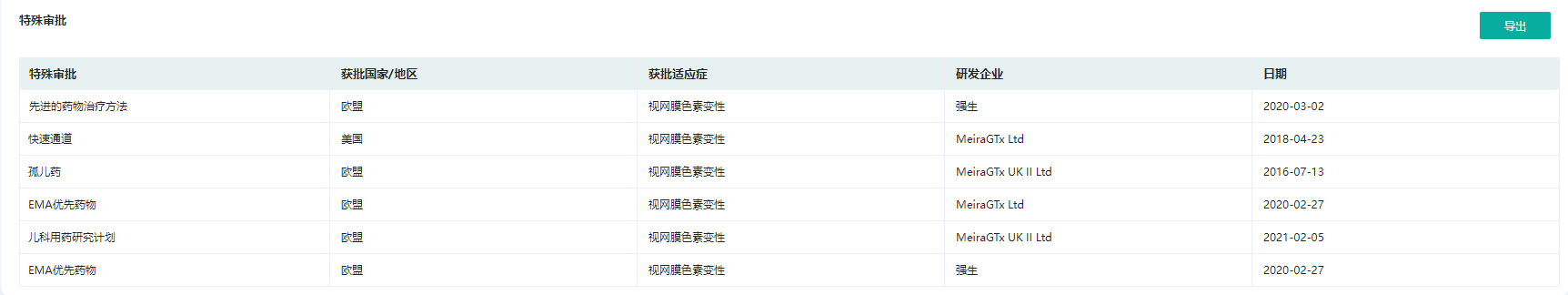
截图来源:药融云全球药物研发数据库(新版)
除了强生的眼部基因疗法取得积极进展外,Applied Genetic Technologies Corporation 也在开发一种用于 XLRP 的基因疗法,并在 5 月报告了一项小型研究的积极中期结果。
要知道,Spark的基因疗法Luxturna是全球首款治疗眼科疾病的基因疗法,于2017年底获得FDA批准上市,用于治疗 REP65 基因突变引起的遗传进行性视网膜疾病。当时对遗传疾病的基因治疗领域产生深远而积极的影响,为数百万患有遗传性疾病但目前治疗方案有限的患者带来曙光。
而此次强生与MeiraGTx开发的眼部基因疗法取得的积极的研究结果也将对遗传性眼病的治疗带来新的希望。
虽然眼部基因疗法取得了重要进展,但是也有挫折。2021年,Biogen 开发的两款眼部基因疗法BIIB111、BIIB112试验失败。而BIIB111和BIIB112两种基因疗法是渤健在2019年3月通过8.77亿美元收购英国眼科基因治疗公司Nightstar Therapeutics时获得的。试验失败时,渤健没有透露两项基因疗法未来的安排。
眼部基因疗法可谓是机遇与挑战并存,如果强生/MeiraGTx开发的这款眼部基因疗法成功,两家公司计划 2024 年将其基因疗法提交监管机构批准。
想要解锁更多药企创新药信息吗?查询药融云数据库(https://www.pharnexcloud.com/?zmt-mhwz)掌握药企创新药产品布局、基本信息、研发阶段、最新进展、申报获批情况、临床试验信息、市场规模与前景等信息,可否投入研发!注册立享15天免费试用和虎年首份医药数据大礼包!

<END>





















































 川公网安备51019002008863号
川公网安备51019002008863号 本网站未发布麻醉药品、精神药品、医疗用毒性药品、放射性药品、戒毒药品和医疗机构制剂的产品信息
本网站未发布麻醉药品、精神药品、医疗用毒性药品、放射性药品、戒毒药品和医疗机构制剂的产品信息
收藏
登录后参与评论
暂无评论