
细胞与基因疗法(CGT)是近年新兴的治疗模式。与其他疗法模式不同的是,CGT具有达成“一次治疗、永久治愈”的潜力,使得许多患者有希望能够长期免受病痛所苦。据统计,2024年上半年全球范围内共有8款CGT疗法获批上市,总结如下:

1. Sarepta: Elevidy获FDA完全批准
6月20日,小核酸龙头Sarepta Therapeutics发布公告:美国FDA批准其杜氏肌营养不良(DMD)基因疗法Elevidys扩展适应症,将年龄至少为4岁的患者纳入其中。FDA对可行走的患者授予了传统批准,对于不可行走的患者,则授予加速批准。
根据加速批准途径,Sarepta承诺进行并提交一项随机对照试验的结果,以验证和确认Elevidys在不可行走DMD患者中的临床益处。ENVISION(SRP-9001-303)试验正在进行中,这是一项全球性、随机、双盲、安慰剂对照的3期研究,该试验针对不可行走和年龄较大的可行走DMD患者,旨在作为这一上市后要求的验证试验。
早在2023年6月,美国FDA加速批准DMD基因疗法Elevidys用于治疗4至5岁患有杜氏肌营养不良症的儿科患者,定价为320万美元/剂,这是全球首款获批上市的杜氏肌营养不良AAV基因疗法。如今,Elevidys 获批用于≥4岁DMD患者,无论其是否能够行走,这对DMD患者的治疗来说具有重要意义。
2. Geron:Rytelo
6月6日,Geron公司宣布美国FDA已批准其“first-in-class”寡核苷酸端粒酶抑制剂Rytelo(imetelstat)用于治疗低危骨髓增生异常综合征 (LR-MDS) 患者的输血依赖性贫血。Rytelo是首个获美国FDA批准的端粒酶抑制剂。自1984年端粒酶被发现以来,经过近40年的等待,产业界终于迎来首款端粒酶靶向疗法。Rytelo被行业媒体Evaluate列为今年10大潜在重磅疗法之一。

FDA 批准 RYTELO 是基于《柳叶刀》上发表的IMerge 3期临床试验结果。IMerge 试验达到了其主要终点和关键次要终点,与安慰剂相比,RYTELO 至少连续八周不输注红细胞(RBC-TI)的比率明显更高(RYTELO 39. 8%[95%CI 30.9-49.3];安慰剂 15.0% [7.1-26.6];p<0.001)和至少连续24周RBC-TI比率更高(RYTELO 28.0% [95% CI 20.1-37.0];安慰剂 3.3% [95% CI 0.4-11.5];p<0.001)。在接受 RYTELO 治疗的人群中,RBC-TI 具有持久性和持续性,8 周应答者和 24 周应答者的中位 RBC-TI 持续时间分别约为 1 年和 1.5 年。
随着Rytelo的批准,Geron公司的股价应声上涨了22%。Evaluate预测,到2028年,Rytelo的销售额有望达到7.37亿美元。这一预测反映了市场对Rytelo治疗潜力的认可。Geron公司为Rytelo设定了明确的定价策略,单剂量47毫克的批发采购成本为2,471美元,而188毫克的单剂量采购成本则为9,884美元。剂量的确定将依据患者的体重进行调整。
3. Moderna:mRESVIA
5月31日,Moderna, Inc.(纳斯达克代码:MRNA)宣布,美国食品药品监督管理局(FDA)批准了一种mRNA呼吸道合胞病毒(RSV)疫苗mRESVIA (mRNA -1345),用于保护60岁及以上的成人免受RSV感染引起的下呼吸道疾病。它是目前唯一一种采用预充式注射器接种的RSV疫苗,这也是mRNA疫苗首次被批准用于COVID-19以外的疾病。
此次批准是基于3期临床试验ConquerRSV的阳性数据,这是一项在22个国家约3.7万名60岁或以上成人中开展的全球性研究。中位随访3.7个月的主要分析发现,疫苗对RSV下呼吸道疾病(LRTD)的预防效力为83.7% (95.88% CI 66.0%, 92.2%)。这些结果发表在《新英格兰医学杂志》上。另一项长期分析表明,在中位8.6个月随访期间,对RSV LRTD仍有保护作用。根据报告显示,在3期试验中未发现严重的安全问题。最常见的不良反应是注射部位疼痛、疲劳、头痛、肌痛和关节痛。
4. 辉瑞:BEQVEZ
2024年4月26日,Pfizer(辉瑞)宣布美国FDA已批准其一种基于腺相关病毒(AAV)载体的基因疗法BEQVEZ(fidanacogene elaparvovec-DZKT)上市,用于治疗中度至重度血友病B且对AAV血清型Rh74的中和抗体检测为阴性的成年(18岁及以上)患者。据悉,BEQVEZ的定价为350万美元,与之前获批上市的由UniQure公司开发的B型血友病基因疗法Hemgenix价格一致。

此次获批主要基于III期BENEGENE-2研究(n=45)的积极数据。结果显示,患者接受单剂次BEQVEZ治疗12个月内,年化出血率(ABR)相比标准预防治疗组(接受FIX类药物作为预防替代治疗)显著降低(1.3 vs. 4.43,P<0.0001),达到非劣效标准并且也达到了优效标准。
BEQVEZ目前正在接受欧洲药品管理局 (EMA) 的审查,该疗法最近获得了加拿大监管部门的批准。除BEQVEZ外,辉瑞目前还有两个三期项目正在研究基因疗法,这两个项目针对的人群都有很高的未满足需求:A型血友病和杜氏肌营养不良症。此外,一项3期试验正在研究新型抗组织因子通路抑制剂marstacimab,用于治疗没有因子VIII (FVIII) 或因子IX (FIX) 抑制剂的血友病A或血友病B。目前,FDA和EMA正在分别审查 marstacimab的生物制品许可申请和欧洲市场授权申请。
5. Orchard:Lenmeldy
3月18日,FDA批准了Orchard Therapeutics研发的基因疗法Lenmeldy,用于治疗异染性脑白质营养不良(MLD)儿童患者。定价为425万美元,超过Hemgenix跃升为有史以来最昂贵的药物。Lenmeldy是FDA批准的治疗早发型异染性脑白质营养不良(MLD)儿童患者的唯一疗法,这种基因疗法于2020年在欧盟获批,2022年在英国获批,上市价格为280万英镑(约351万美元,按最新汇率1英镑 ≈ 1.2526美元计算)。

Lenmeldy(atidarsagene autotemcel,原名OTL-200)是利用Orchard的核心技术自体干细胞体外修饰后回输基因疗法研发出来的,旨在使用慢病毒载体将编码芳基硫酸酯酶-A的ARSA转基因导入到MLD患者的自体CD34阳性造血干细胞和祖细胞中,从而通过一次性治疗恢复芳基硫酸酯酶-A的表达,阻止或减缓疾病进展。
此次FDA批准基于37名儿童的数据,进行12年随访(中位时间6.76年),与未经治疗的儿童相比,接受 Lenmeldy 治疗的患者总体生存期显著延长,运动障碍或死亡显著减少。安全性方面,Lenmeldy显示良好的耐受性,无治疗相关严重不良事件或死亡。
6. BMS: Breyanzi
3月14日,百时美施贵宝(Bristol Myers Squibb)宣布美国FDA已加速批准Breyanzi(lisocabtagene maraleucel;liso-cel)。这是一种靶向CD19的CAR-T细胞疗法,用于治疗复发/难治性慢性淋巴细胞白血病(R/R CLL)或小淋巴细胞淋巴瘤(SLL)成人患者,这些患者之前至少接受过两线治疗,其中包括BTK抑制剂和BCL-2抑制剂。新闻稿指出,这款细胞疗法是首款用于复发性或难治性CLL或SLL成人患者的CAR-T细胞疗法。

Breyanzi是一种靶向CD19抗原的自体CAR-T细胞疗法,具有明确的组成和4-1BB共刺激域。它于2021年2月获FDA批准,用于治疗接受过两种或以上系统治疗的复发/难治性大B细胞淋巴瘤(LBCL)成人患者。这款疗法的独特之处在于CAR-T疗法中CD8阳性和CD4阳性T细胞的比例得到控制,从而可以更好地控制细胞疗法的毒副作用。4-1BB信号结构域则增强了CAR-T细胞的扩增和持久性。
根据新闻稿,该适应症是根据缓解率和缓解持续时间加速批准的。该适应症的进一步批准可能取决于确证性试验对临床疗效的验证结果。此次获批基于的TRANSCEND CLL 004试验是一项开放标签、单臂、多中心的临床1/2期试验。数据分析显示试验达成主要终点,20%接受Breyanzi治疗的复发或难治性CLL或SLL患者患者达到完全缓解(CR),安全性已确认。
7. 科济药业:泽沃基奥仑赛注射液
3月1日,科济药业发布公告:国家药品监督管理局(“NMPA”)已批准其BCMA CAR-T产品赛恺泽®(泽沃基奥仑赛注射液)新药上市申请(“NDA”),用于治疗复发或难治性多发性骨髓瘤成人患者,既往经过至少3线治疗后进展(至少使用过一种蛋白酶体抑制剂及免疫调节剂)。泽沃基奥仑赛是国内第五款获批的CAR-T疗法。
3月5日,科济药业披露其CAR-T细胞疗法泽沃基奥仑赛注射液(商品名:赛恺泽)的首发价格为115万元,经与合作方华东医药(000963.SZ)共同预估,该药年终端销售额的峰值预计可达10亿元以上。

赛恺泽®是一种自体BCMA靶向CAR-T细胞产品,它是通过慢病毒转导T细胞产生的。慢病毒编码的CAR包括全人源BCMA特异性单链可变片段(“scFv”),人CD8α铰链结构域、CD8α跨膜结构域、4-1 BB协同刺激结构域以及CD3ζ激活结构域。自研的新全人源scFv具有较高的结合亲和力和稳定性。科济药业正在北美推进1b/2期临床试验(LUMMICAR STUDY 2),以评估赛恺泽®用于治疗复发或难治性多发性骨髓瘤的安全性及疗效。
2023年1月,科济药业与华东医药就赛恺泽®达成在中国大陆地区的商业化合作,科济药业授予华东医药赛恺泽®在中国大陆地区的独家商业化权益。根据协议,华东医药(杭州)向科济药业控股有限公司的全资子公司恺兴生命支付2亿元人民币首付款,以及最高不超过10.25亿元人民币的注册及销售里程碑付款。
8. Iovance:Amtagvi
2月16日,Iovance Biotherapeutics公司宣布,FDA加速批准该公司的肿瘤浸润淋巴细胞(TIL)疗法Amtagvi(lifileucel)上市,用于治疗晚期黑色素瘤,定价51.5万美元。据悉,lifileucel是全球首款获批上市的TIL细胞疗法。

Amtagvi 是一种肿瘤衍生的自体 T 细胞免疫疗法。在治疗前的外科手术中切除患者的一部分肿瘤组织,将患者的T细胞从肿瘤组织中分离出来,进一步制造,然后以单剂量输注的形式返回给同一患者。单剂量的Amtagvi包含7.5亿到72亿个活细胞,从收到肿瘤组织到完成Amtagvi制备大约34天。
Amtagvi 2期临床试验显示:在中位随访时间为27.6个月时,患者客观缓解率(ORR)为31.4%,包含8位患者达完全缓解(CR)与40位患者达部分缓解(PR)。后来,Iovance 4年随访数据显示,最长缓解持续时间为55.8个月。
临床试验安全性数据:
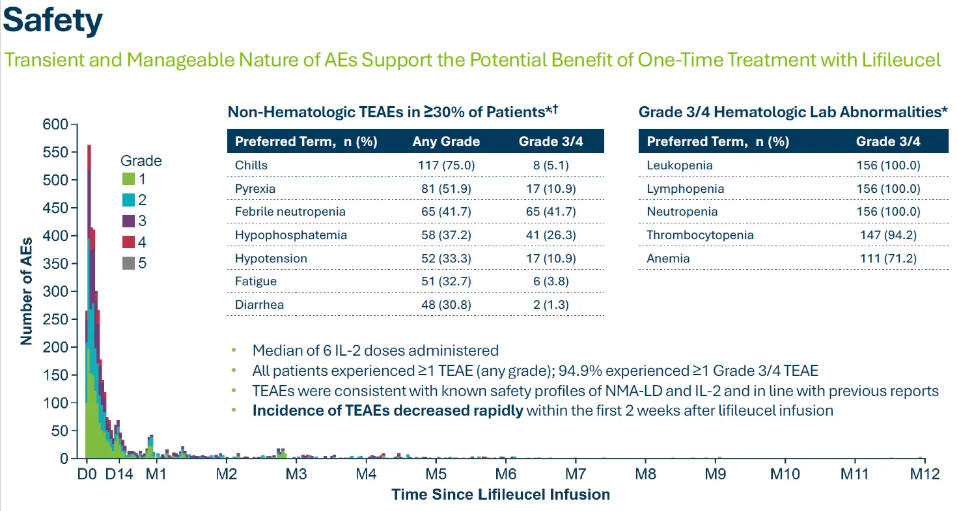
总结
2024年还有5款CGT疗法有望成功获批上市,包括:恒润达生的CAR-T细胞治疗产品润达基奥仑赛注射液、Adaptimmune Therapeutics的TCR T细胞疗法艾基奥仑赛、BioCardia的CardiAMP、辉瑞的新型研究性基因疗法Fidanacogene elaparvovec、Autolus Therapeutics的CAR-T细胞疗法Obecabtagene autoleucel。Rocket Pharmaceuticals的基因疗法Kresladi和Abeona Therapeutics的在研自体细胞疗法Prademagene zamikeracel(pz-cel)分别于6月和4月因CMC问题被FDA拒批,FDA要求提供额外的CMC信息以完成审查。
参考资料:各公司公告
<END>
想要解锁更多药物研发信息吗?查询药融云数据库(vip.pharnexcloud.com/?zmt-mhwz)掌握药物基本信息、市场竞争格局、销售情况与各维度分析、药企研发进展、临床试验情况、申报审批情况、各国上市情况、最新市场动态、市场规模与前景等,以及帮助企业抉择可否投入时提供数据参考!注册立享15天免费试用!























































 川公网安备51019002008863号
川公网安备51019002008863号 本网站未发布麻醉药品、精神药品、医疗用毒性药品、放射性药品、戒毒药品和医疗机构制剂的产品信息
本网站未发布麻醉药品、精神药品、医疗用毒性药品、放射性药品、戒毒药品和医疗机构制剂的产品信息
收藏
登录后参与评论
暂无评论