 2023年11月英国批准了世界第一款 CRISPR-Cas9 基因编辑药物--- exagamglogene autotemcel(exa-cel)(商品名:Casgevy)上市。Casgevy用于治疗12岁和以上镰状细胞病(SCD)伴复发性血管闭塞危象的患者,以及无法获得人类白细胞抗原匹配造血干细胞移植治疗的输血依赖性β-地中海贫血(TDT)患者。Casgevy的上市是CRISPR基因编辑疗法的里程碑!
2023年11月英国批准了世界第一款 CRISPR-Cas9 基因编辑药物--- exagamglogene autotemcel(exa-cel)(商品名:Casgevy)上市。Casgevy用于治疗12岁和以上镰状细胞病(SCD)伴复发性血管闭塞危象的患者,以及无法获得人类白细胞抗原匹配造血干细胞移植治疗的输血依赖性β-地中海贫血(TDT)患者。Casgevy的上市是CRISPR基因编辑疗法的里程碑!
为什么是SCD以及TDT?
SCD是世界上最早发现分子病理的疾病,目前致病机理也最为清晰(单基因遗传病),而且相信你早在中学生物课上就已经听说过它。同TDT,它们都是由血红蛋白遗传密码错误引起的疾病。
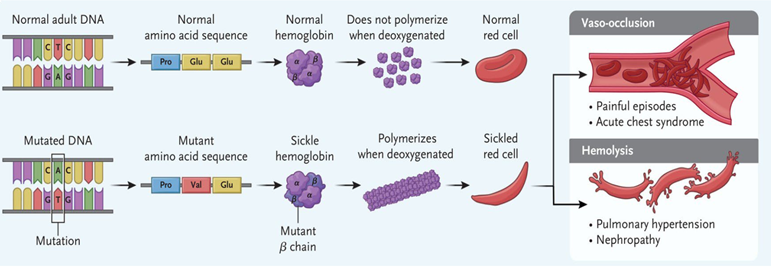
图1:SCD致病机理
作为单基因遗传病,基因工程手段则是为它量身定做的治疗方法。
基因工程操纵DNA或RNA已被用于预防或治疗人类和动物疾病,这种操作包括插入、替换或删除与特殊遗传疾病相关的基因。
迄今为止,即锌指核酸酶(Zinc Finger Nuclease, ZFN)、转录激活因子样效应核酸酶(Transcription-Activator Like Effector Nucleases, TALEN)和成簇规则间隔短回文重复序列CRISPR(Clustered Regularly Interspaced Short Palindromic Repeats, CRISPR)三种技术可用于靶向基因组编辑。
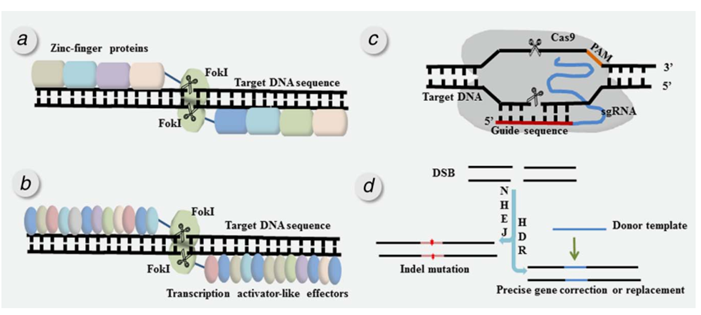
图2:靶向基因组编辑技术
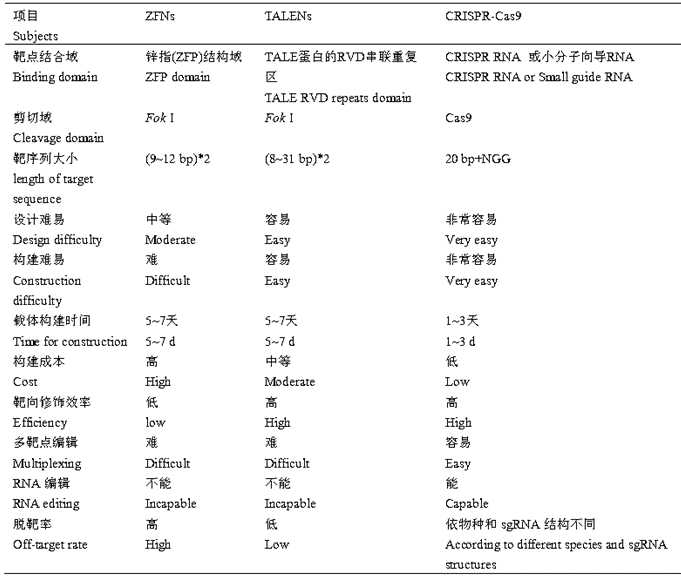
成簇的规则间隔短回文重复序列/ CRISPR相关核酸酶9 (CRISPR‐Cas9)在设计构建、效率成本和修饰效率上较TALENs和ZFNs两种技术更具优势。
表1:ZFNs、TALENs 和 CRISPR-Cas9 技术特点的比较
2012年,Emmanuelle Charpentier(埃马纽埃尔·卡彭蒂耶)和Jennifer A. Doudna(詹妮弗·杜德纳)在Science上发表了CRISPR/Cas9 系统的发现后,仅仅八年后的2020年她们因其发现获得了 2020 年诺贝尔化学奖!不可否认的是,张锋在其中也发挥了不可忽视的作用,为他们伟大的发现和应用致敬!

下面我们来聊一聊CRISPR,Casgevy背后的技术。
CRISPR-Cas系统是原核生物的一种天然免疫系统,当一些细菌在被病毒入侵后,它们能够将病毒的基因片段存储在一个称为 CRISPR 的存储空间中,并保存在它们的 DNA 中。当病毒再次入侵时,细菌可以根据病毒上次保存的片段来识别病毒,之后切断病毒的 DNA 并使其失效。六种类型的CRISPR-Cas系统在主要古细菌和细菌门中的分布如下图。
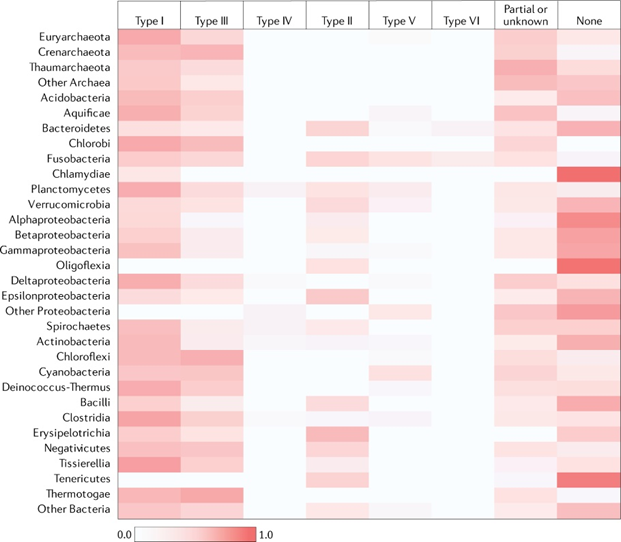
图3: CRISPR-Cas系统在主要古细菌和细菌门中的分布
由于Cas蛋白的序列以及组合差异,CRISPR系统分为两个大类:1 类 CRISPR-Cas 系统(包括Ⅰ型、Ⅲ型、Ⅳ型)具有由多种 Cas 蛋白组成的效应模块,这些蛋白形成 crrNa 结合复合物,并在靶标的结合和加工中共同发挥作用;此外,第 2 类系统具有单个多结构域 crRNA 结合蛋白,其功能类似于第 1 类的整个效应复合物。第 2 类系统由于系统结构简单和效率高而目前广泛应用于基因编辑领域。其中,Ⅱ型的效应蛋白Cas9拥有HNH和RuvC样核酸酶结构两个结构域:它们每个结构域负责切割DNA的一条链;Ⅴ型效应蛋白Cas12包含一个可切割两条链的RuvC样结构域;Ⅵ型效应蛋白Cas13包含两个可靶向切割DNA和RNA HEPN结构域。
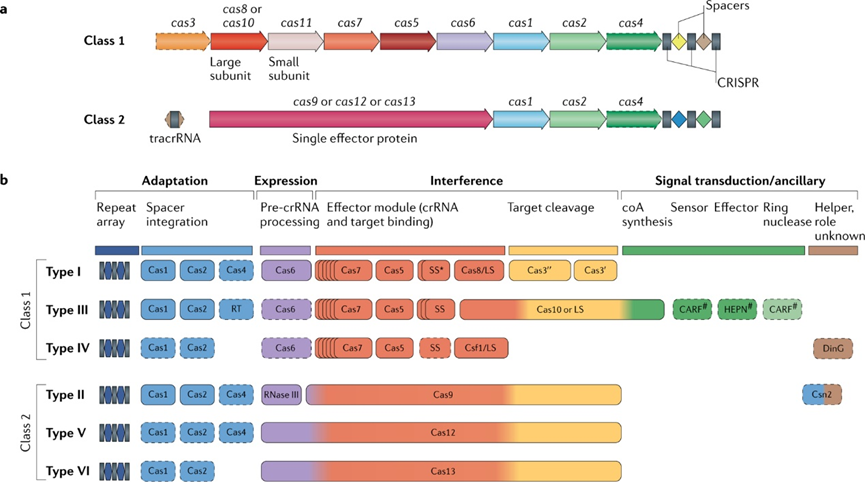
图4:Cas蛋白分类以及六种类型的CRISPR-Cas系统的遗传、结构和功能组织之间的典型关系
不同的CRISPR系统在外源遗传物质入侵后产生相似的三个防御阶段。以目前最为广泛应用的CRISPR/Cas9为例,分为1)适应(间隔区获取):外源遗传物质如噬菌体DNA入侵后,其DNA中一小段(前间隔序列)被整合到CRISPR序列中,这个插入的片段构成了一个新的和特殊的间隔单元;2)表达(CRISPR‐RNA [crRNA]的过程):当噬菌体再次入侵时候,第一阶段的CRISPR序列响应转录出前体CRISPR RNA并被RNaseⅢ加工后成熟为crRNA,并与tracrRNA互补形成双链RNA结构;3)干扰(破坏和切割入侵者DNA或RNA:第二阶段产物与Cas9蛋白结合,其中Cas9蛋白识别特定的的前间隔序列邻近基序(PAM),双链结构与靶序列结合来激活Cas9蛋白的酶切活性,促使靶基因产生双链DNA断裂(Double-stranded DNA breaks,DSB)。在II型CRISPR‐Cas系统中,Cas9包含两个核酸酶结构域,RuvC和HNH结构域。
细菌和古细菌的这种天然适应性免疫可以重新设计,以实现所需的基因组编辑。第二阶段产物目前被简化为单链导向RNA (Single guide RNA,sgRNA),通过修改sgRNA的序列即可将Cas9蛋白引导指定位置来切割目标DNA序列。
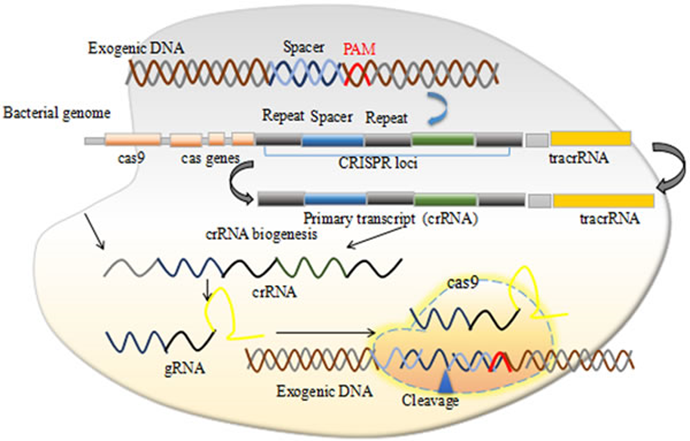
图5:CRISPR/Cas9机制
宿主细胞通过两种不同的机制对这种双链断裂做出反应:1)非同源末端连接(NHEJ)和2)同源定向修复(HDR),产生包括基因敲除、缺失、校正或添加。NHEJ的易出错特性可用于将插入缺失和移码引入基因的编码区。通过无义介导的 mRNA 转录物衰变敲除基因(图(A))。在基因缺失(图(B))中,配对的核酸酶切除编码基因的区域,导致蛋白质过早截断和敲除,其方式比引入移码更有效。基因校正(图(C))和基因添加(图(D))需要外源DNA模板。
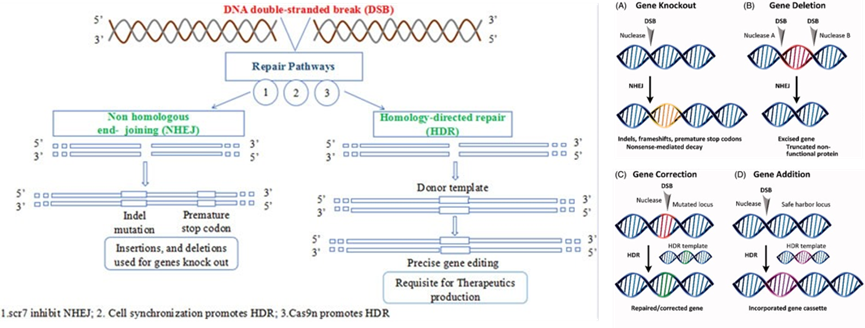
图6:两种DNA修复途径以及产物
即使在存在供体模板DNA的情况下,NHEJ也是从CRISPR / Cas9编辑中观察到的更频繁的修复机制。HDR仅在细胞周期的复制期起作用,通过利用来自姐妹染色单体的同源模板来恢复丢失的遗传信息,NHEJ发生在整个细胞周期中,并且可以通过以非模板依赖的方式将断裂的DNA首尾相连而发生。对此,几种提高HDR效率和抑制NHEJ的方法,包括使用NHEJ的小分子抑制剂、基因沉默、细胞周期同步以及使用缺乏NHEJ成分的细胞系。
CRISPR‐Cas9蛋白的两种重要传递系统,包括病毒传递系统和非病毒传递系统。一般来说,五类病毒载体被用于传递系统,其中逆转录病毒和慢病毒能够整合到宿主基因组中,腺相关病毒(aav)、腺病毒和疱疹病毒为非整合载体。在病毒传递系统中,两种重组病毒(AAV和Lentivirus)比较受欢迎。
显微注射被认为是将CRISPR成分引入细胞的“金标准”,效率接近100%,而且解决了病毒载体递送系统中货物分子量的限制,定量使用改善了脱靶问题,但是受限于体外实验。病毒载体中AAV是一种单链DNA病毒,已广泛用于基因治疗并具有良好的安全性。脂质也可以像病毒颗粒一样,在体外、离体和体内使用,从而可以在各种规模的细胞群上进行广泛的测试。CPP通常直接共价连接到Cas9蛋白上,然后与sgRNA复合并递送至细胞,CPP 目前通常不用于在体内递送组件。除此之外,金纳米粒、纳米复合物(如FuGENE-6)和DNA纳米核(DNAnanoclew)以及新型技术多功能包膜型纳米器件(MENDs)、脂质包被介孔二氧化硅颗粒和无机纳米颗粒也见于递送研究。
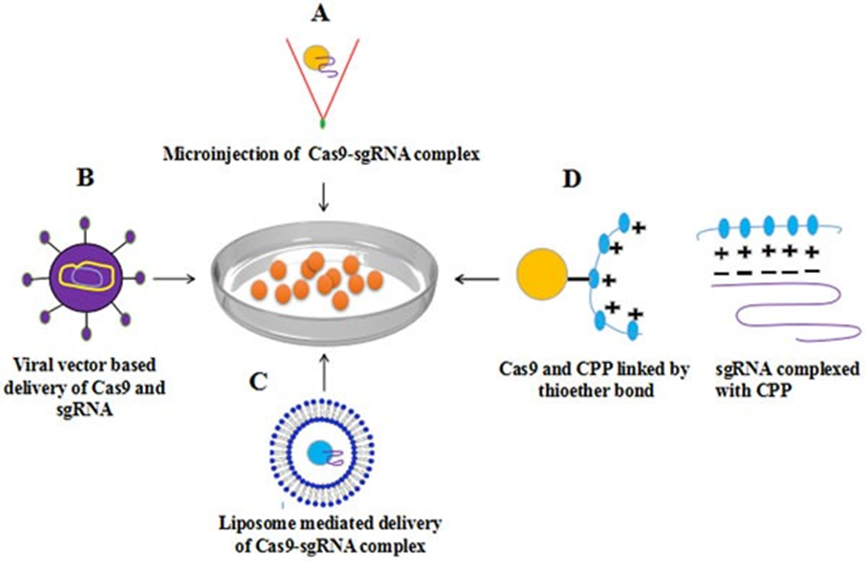
图7:Cas9-sgRNA复合物递送至细胞的方法。A. 显微注射B. 病毒载体(AAV)C.脂质 D.细胞穿透肽(CPP)
CRISPR-Cas9存在包括选择DNA靶位点受限于PAM序列不能对基因的任何位点进行编辑、脱靶效应在内的自身的局限性。
CRISPR - Cas9应用中的挑战
1. 脱靶风险:CRISPR-Cas9系统的一个主要限制是它们的脱靶效应,这可能导致基因组不稳定、基因功能破坏和表观遗传改变。改进策略包括用纯化的重组Cas9蛋白而不是Cas9基因转染细胞可以减少脱靶效应(蛋白被迅速降解,避免了对基因组的持续影响)、选择非靶位置同源性最低的靶序列等。
2. 递送和编辑效率长期以来一直是基因治疗应用的关键。这个问题的解决在于将来开发更有效的递送载体、更强有力的sgRNA和更有效的Cas9。此外,对参与递送过程的病毒载体的免疫反应是CRISPR‐Cas9系统的重要挑战。HDR导致所需的基因修饰,而NHEJ引起不需要的基因,导致不可控的基因破坏。增加HDR率可以提高CRISPR-Cas9介导的基因治疗的效率和可靠性,同时降低基因组毒性效应。
CRISPR - Cas9应用中虽然有很多挑战,中美相关临床研究热度相对比较高,伴随Casgevy的上市在一定程度上提振了研究者士气,尽管其高昂的定价。可以乐观地预计在未来它可能会彻底改变基因治疗研究,并成为人类基因治疗实践的一种方便和通用的工具。
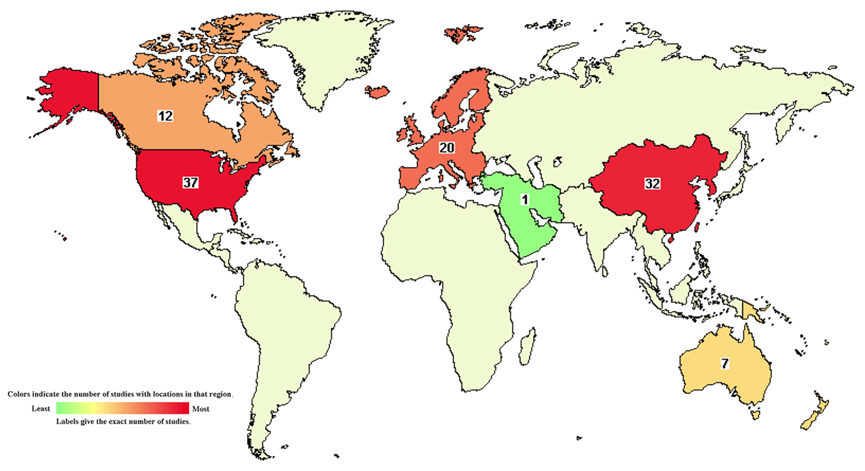
图8:以“CRISPR”为关键词在ClinicTrial上搜索到的临床注册试验
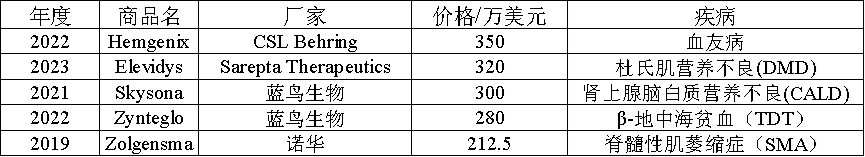
2023年美国最昂贵药物排名TOP10中基因疗法占据半壁江山,Casgevy来看,高昂的定价以及可能对应的受益人群获利可能是厂商需要考虑的一大问题,对患者家人而言,既看到了希望又掺杂着一丝丝绝望, anyway,尊重科学,敬畏生命!
表2:Top5基因疗法价格
参考文献
https://doi.org/10.1056/nejme2119760
https://doi.org/10.1002/ijc.29626
doi: 10.5376/mpb.cn.2016.14.00010
https://doi.org/10.1038/s41579-019-0299-x
https://doi.org/ 10.18632/oncotarget
https://doi.org/10.18632/oncotarget.9646
https://doi.org/10.1080/10717544.2018.1474964
<END>
要解锁更多企业药品研发信息吗?查询药融云数据库(vip.pharnexcloud.com/?zmt-mhwz)掌握药品各国上市情况、药品批文信息、销售情况与各维度分析、市场竞争格局、一致性评价情况、集采中标情况、药企申报审批信息、最新动态与前景等,以及帮助企业抉择可否投入时提供数据参考!注册立享15天免费试用!























































 川公网安备51019002008863号
川公网安备51019002008863号 本网站未发布麻醉药品、精神药品、医疗用毒性药品、放射性药品、戒毒药品和医疗机构制剂的产品信息
本网站未发布麻醉药品、精神药品、医疗用毒性药品、放射性药品、戒毒药品和医疗机构制剂的产品信息
收藏
登录后参与评论
暂无评论