一、底蕴浓厚的盐野义
盐野义制药集团,拥有超过140年的历史,是日本第五大药企,现今因其研发出了新冠口服药,走到了新冠流行病舞台的聚光灯下——该公司曾于2022年11月22日宣布,其口服3CL蛋白酶抑制剂恩赛特韦(ensitrelvir)的紧急使用授权获日本PMDA紧急授权批准上市,用于治疗新型冠状病毒感染。

盐野义& Co., Ltd.(盐野义制药集团)(4507.T)成立于1878年,总部位于大阪市。(截止2023年3月27日,盐野义股价46.04美元/股,市值约136.8亿美元)拥有丰富的药品研发、生产及销售经验,在日本制药领域处于领先地位,其抗感染/抗病毒、中枢神经系统疾病等相关药物拥有较高知名度。
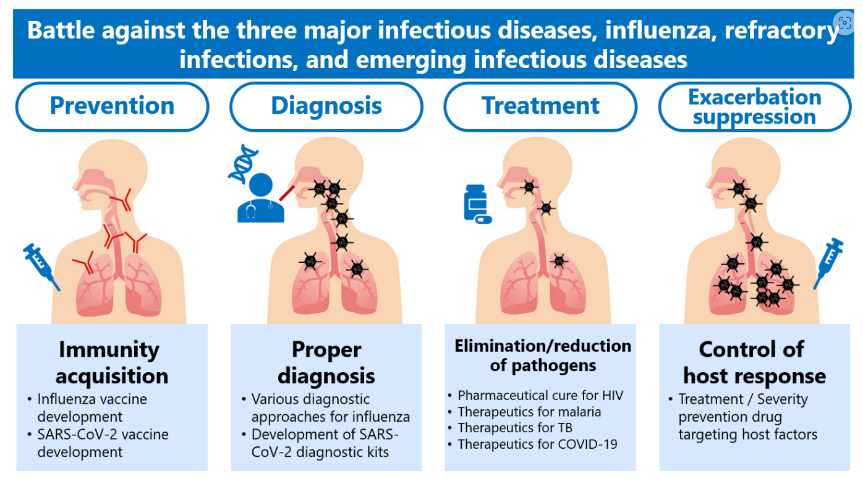
主要业务领域:抗感染/抗病毒、精神障碍和神经系统疾病(痴呆症、发育障碍、精神障碍、疼痛等)、新的增长领域(癌症、疫苗等)。其中,该公司核心治疗领域是传染病和精神神经障碍,在传染病领域具有核心竞争力,一直将“摆脱传染病威胁”作为公司追求的重要目标。
药融圈旗下药融云数据库www.pharnexcloud.com/?mh显示:盐野义在全球范围内广泛开展合作。其合作伙伴按领域划分后图示如下:

二、发展历史中的里程碑事件
1878年,创始人Gisaburo Shiono(以下简称为Gisaburo)在其父亲经营的药品批发业务中学习批发贸易。就在这一年3月17日,也是Gisaburo Shiono年满24岁生日的那天,他在大阪道士町3丁目12号创立了自己的药品批发商,命名为“盐野义三郎商店”。这便是盐野义公司的起源。

1886年,从日本医学和中医向西医转变。盐野义起初主要经营日本和中国汉方药品。随着西方医学在日本逐渐普及,1886年,Gisaburo决定大胆地转向西方医学。当时,西方医学已经通过横滨和神户的外国贸易商进行了分销,但价格很高;在日本的药品批发商对贸易业务不熟悉,以外国贸易商的要高价购买。
Gisaburo很快寻求了一位经验丰富、精通英语的商人的帮助,从海外直接进口药品。因此,他能够以许多患者能够负担的价格出售药品。后来,当其他公司也开始直接进口药品时,他将目标转向了制药产品的内部生产。

1909年,推出第一款新药:Antacidin。Gisaburo次子Chojiro毕业于东京帝国大学医药学部制药专业之后,盐野义开始进行全面的制药研究。当时,该会社的一位监督药剂师从大阪府立医学校的一位儿科首席医师那里得知了一种抗胃酸剂的处方,该处方是从一本德国药学书中引用的。Gisaburo开始制造这种抗酸剂的试验品,并成功地生产出了市场销售的产品。这种新型抗消化不良药物Antacidin是盐野义公司推出的第一款自主创新药物。
1910年,成立盐野义制药所,主要进行新药研制。成功推出抗酸剂Antacidin之后,Gisaburo立志于全面开发新药制造业。为此,药厂“盐野义制药所”在大阪府西成郡(现在的大阪市福岛区)建成。这让盐野义拥有了制药部门,从药品批发商转变为了以研究为基础的制药公司。1910年,这家工厂由Chojiro担任总监开始运营。然而,当时进口药品在制药行业中占据绝对优势。日本的制药公司陷入困境,被迫依赖进口药物成分。在这种情况下,Chojiro邀请了刚从德国留学归来的药理学博士Heizaburo Kondo作为顾问加入运营。1912年,该博士运用洋地黄制剂,成功开发出一款治疗心脏病药物:Digitamin。随着第一次世界大战的爆发,两年后日本停止了海外药品的进口,彼时盐野义通过制造和分销公司的Digitamin药物大赚了一笔。

1943年,该制药所正式更名为盐野义& Co., Ltd.。
1945年,灾难后的恢复:将成为国际性制药企业定为目标。二战日本惨败,Chojiro陷入了破产的困境:海外分销办事处全部丢失,主要工厂和设备被空袭摧毁,也没有储备药物可供运输。Chojiro在聚集员工时说:“消除赤字的唯一途径是每个人在各个层次和岗位上提高技能水平和削减成本,集中资源和努力。”1948年,盐野义公司制定了一个计划,提出三个重点:1.在每项工作中提高质量,2.确定目标并进行充分的进展审查,3.保持工作场所清洁。
1950年,推出止痛药Sedes。Sedes最初于1939年成为处方药。这个回文式的产品名称“Sedes”源自英语单词“sedative”,意为“镇痛剂”。经过多次改进,该药物有了更安全、更有效的药效,1950年,Sedes作为非处方药开始销售。在1976年和1987年,盐野义又分别推出了Sedes A和New Sedes。该药物已提供半个多世纪的止痛治疗。

1953年,推出多种维生素补充剂——Popon-S。由于健康信息的科普传播,以前用作治疗药物的维生素化合物开始被频繁用作健康促进剂,提供诸如从疲劳中恢复和改善身体健康等益处。当时,就销售额和利润而言,这类维生素化合物是盐野义最重要的产品之一。
1959年,盐野义发现并开发的第一个磺胺类抗生素药物——Sinomin上市。两年后,Sinomin凭借其卓越的疗效,开始在世界各地上市。考虑到抗生素相关产品的潜在全球销售增长范围,盐野义又建设了一家生产抗生素的工厂。1952年,盐野义(盐野义)获得了礼来公司发现的一种新抗生素——伊洛霉素(Ilotycin)的独家生产和销售权。随后,头孢类抗生素陆续上市,都大大增加了盐野义的销售额:1966年的Keflin,1967年的Keflodin,1979年的Keflex。
1982年,盐野义推出内部研制的Shiomarin,这是世界上第一种氧头孢烯抗生素。与礼来公司的合作关系使盐野义的研究和制造能力以及销售能力大大受益。1961年,基础研究机构盐野义研究室(现并入盐野义药物研究中心)成立,进行抗生素研究。氟马林和氟莫司分别于1988年和1997年上市,盐野义获得了“抗生素专家”的称号。
1983年,建立Kanegasaki工厂。该工厂配备了经美国FDA等海外监管机构检查和批准的生产技术和质量控制系统GMP,并生产内部抗感染和止痛药物。自此,盐野义拥有3大工厂:Kanegasaki工厂、大阪的Settsu工厂和兵库县的Kuise工厂。

2000年4月-2005年3月,时任盐野义总裁Motozo Shiono推出第一个中期商业计划,旨在进行彻底的结构改革。首先,盐野义剥离了农业化学品、兽药、药品批发等领域的业务;然后,在2001年,在美国成立了一家附属开发公司,旨在专注于领先的治疗领域并加快开发;此外,与英国葛兰素史克(GlaxoSmithKline)成立合资公司,并开始合作开发新药;
瑞舒伐他汀全球销售情况
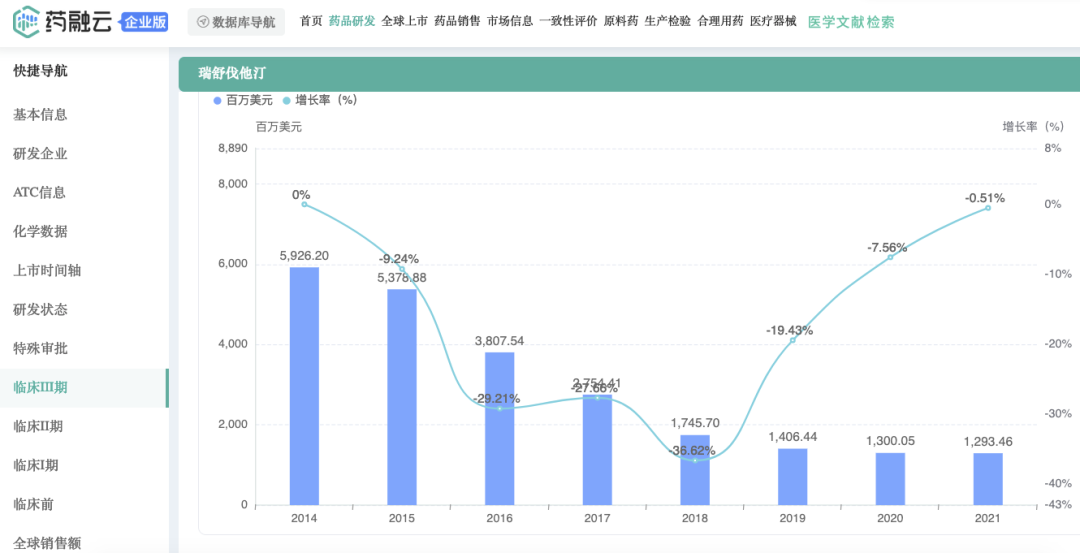
截图来源:药融云全球药物研发数据库
最后,自2003年以来,总部位于英国的阿斯利康(AstraZeneca)获得授权的高脂血症治疗药物可定(Crestor,瑞舒伐他汀)在美国和其他100多个国家上市,为盐野义带来了可观的专利收入。
药物研发信息(部分,完整内容欢迎登陆“药融云数据库www.pharnexcloud.com/?mh”查看)

截图来源:药融云全球药物研发数据库
2005年4月-2010年3月,推出第二个中期商业计划。从Crestor获得的特许权使用费收入被集中投资于三个优先领域的研发:传染病、疼痛和代谢综合征。收购了总部位于美国的Sciele Pharma,Inc.,以简化内部发现的产品的海外销售立足点。因此,盐野义能够在美国这个世界上最大的医药市场建立起自我销售网络。在国内市场,Crestor等战略性产品相继上市,盐野义将重点放在新产品上,并从抗生素等急性病治疗药物转向治疗慢性病的药物。

2010年4月-2014年2月,推出第三次中期商业计划,旨在克服所谓的“Crestor专利悬崖”。2011年,盐野义药物研究中心4(SPRC4)在大阪丰中的一个地点建成,这是一个新的尖端研究设施,它将分散的药物发现研究中心的各功能整合到SPRC中,由现有的三个研究设施和一个新建的研究设施组成。
在美国业务方面,Sciele Pharma,Inc.的业务模式及结构改革因预期于美国上市的抗肥胖候选药物暂停开发而提前进行。该公司于2011年以盐野义公司(盐野义Inc.)的名义重新启动,并于2013年推出了Osphena,这是盐野义公司(盐野义Inc.)申请、批准和推出的第一个全球新化学实体。盐野义于2011年收购了中国制药企业C&O制药科技(控股)有限公司(南京长澳),并于2012年在伦敦成立了附属发展公司盐野义有限公司,这些举措使得盐野义逐步成为一家国际性药企。

2014年4月,第三个中期业务计划提前一年结束,制定了新的中期业务计划“盐野义增长战略2020(SGS2020)”。

2016年5月,更新中期业务计划。根据更新后的计划,盐野义已将业务资源引入拥有强大地位的领域,这意味着该公司将在大约十年内克服“dolutegravir/抗HIV药物专利悬崖”。
更新的SGS2020中的基本策略:增长地区:以日本和美国为重点,同时加强在欧洲和亚洲的实力;增长领域:感染性疾病,疼痛/中枢神经系统疾病。
三、财务状况
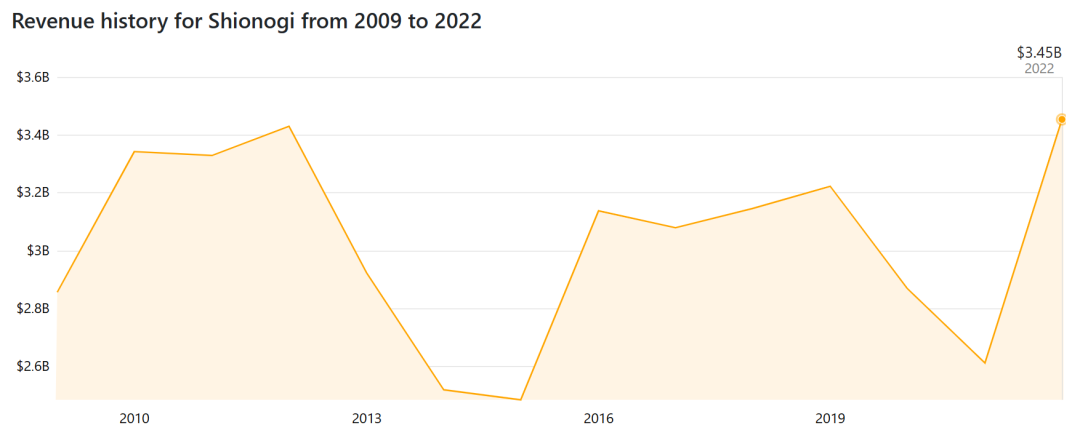
以下是盐野义制药2009年~2022年营收额变化情况:
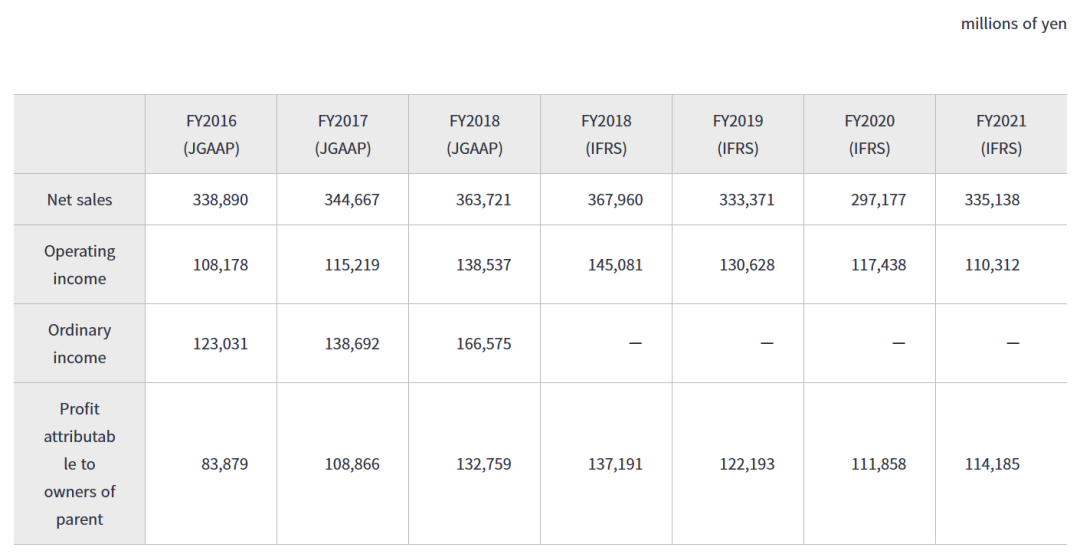
01.2021财年年报
2022年5月11日,盐野义制药公布2021年年度财务报告:全年营收额3351亿日元(25.5亿美元),同比增长12.8%;核心营业利润1106亿日元(8.4亿美元),同比增长17.7%;研发费用730亿日元(5.5亿美元),同比增长34.6%。
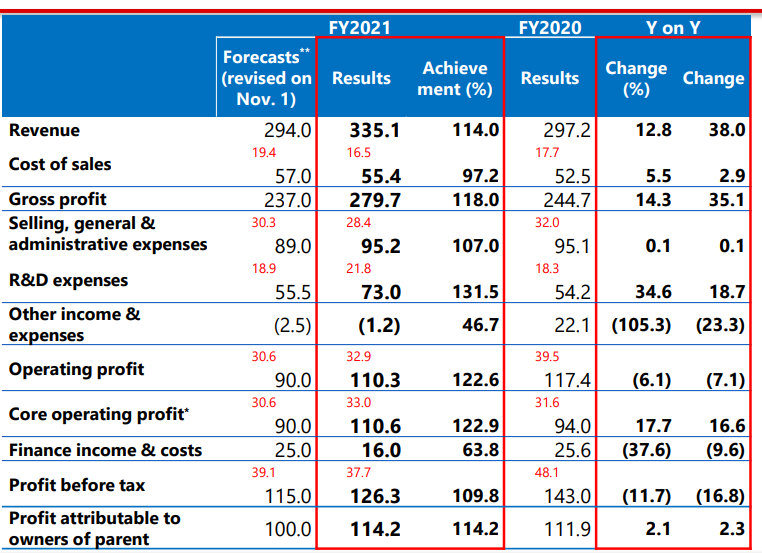
盐野义将公司营收来源分为6大类别:日本国内处方药、海外市场、合同制造(Contract manufacturing)、非处方药和医药部外品、授权费、其他收入来源。2021财年盐野义主要营收来源来自授权费,营收额为1813亿日元(13.8亿美元),同比增长25.3%。
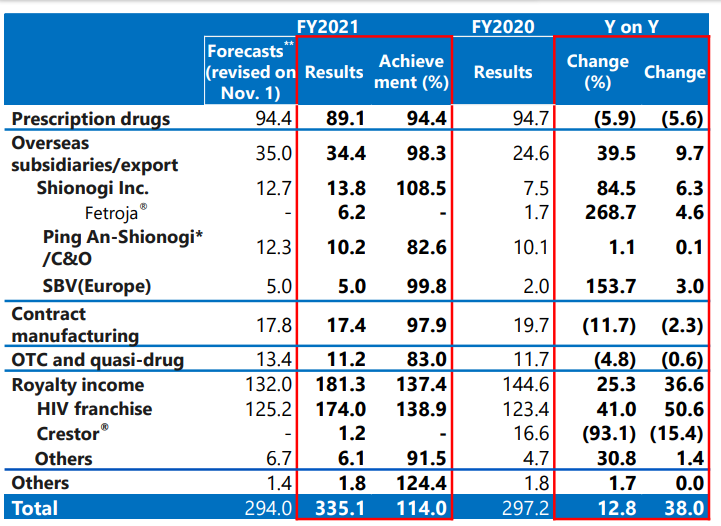
日本国内市场处方药营收情况:
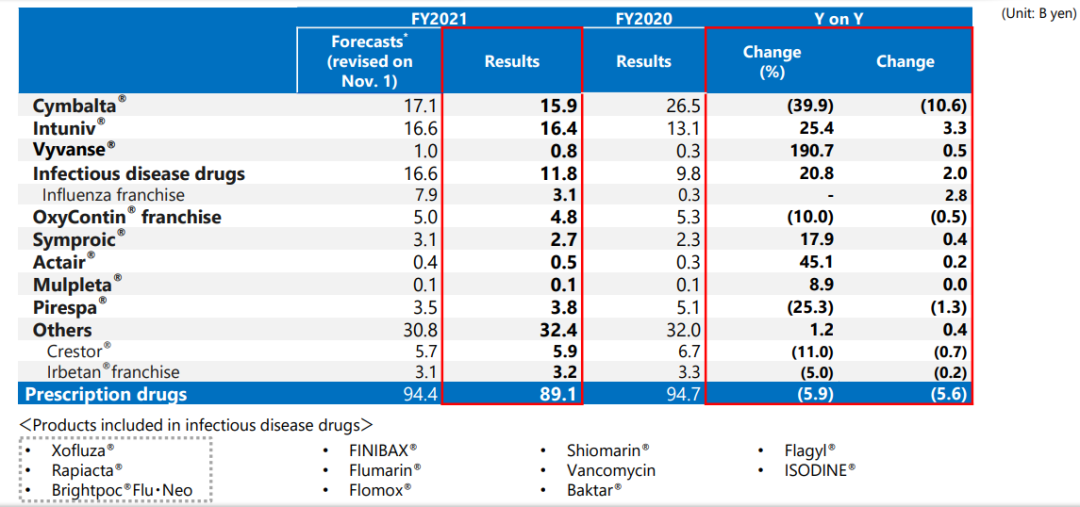
02.2022财年第三季度报
2023年1月30日,盐野义公布2022财年第三季度报。2022财年第三季度营业收入为3383亿日元(25.7亿美元),同比增长54.1%。核心营业利润1440亿日元(10.9亿美元),同比增长132.6;研发费用投入总计748亿日元(5.7亿美元),同比增长55.1%。
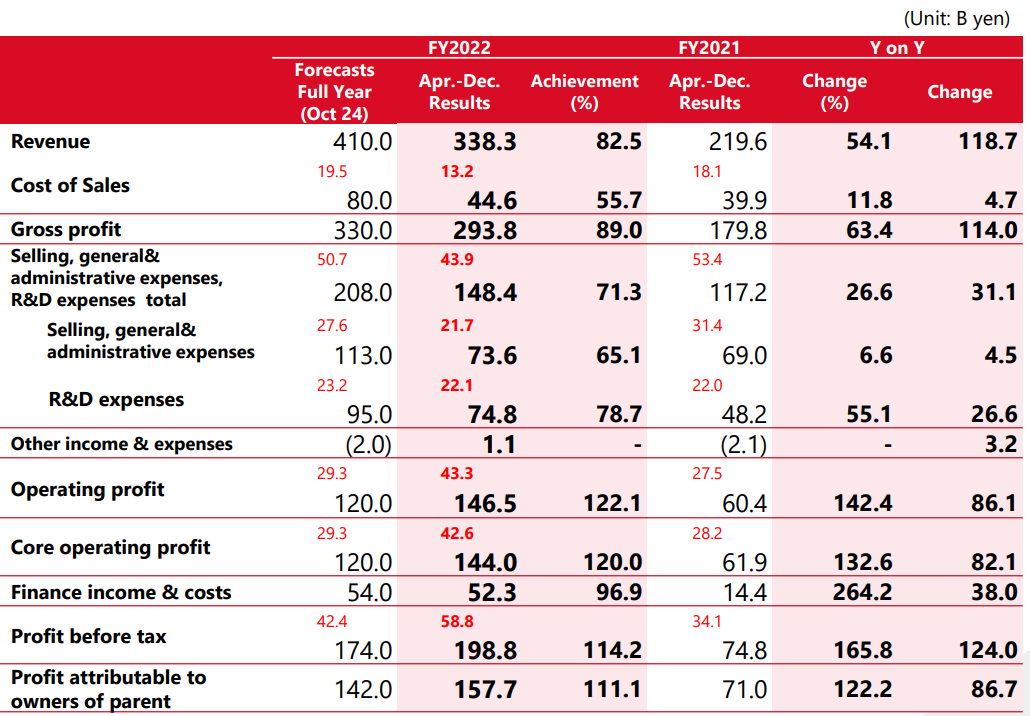
03.2022财年业绩预测
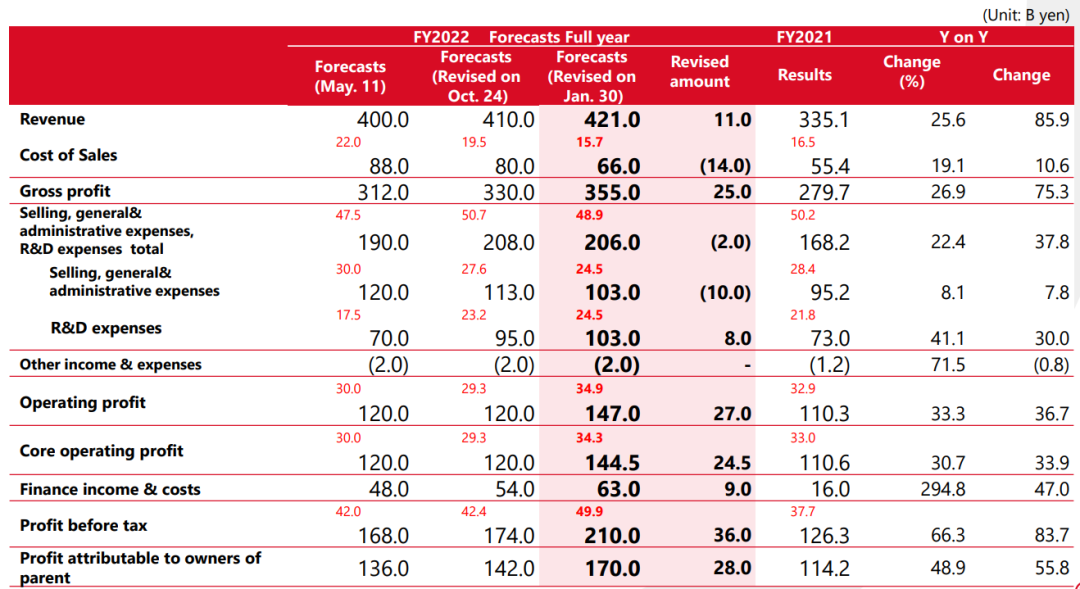
盐野义制药预计,2022财年全年营收同比增长25.6%,达到4210亿日元(32亿美元);核心营业利润达到1470亿日元(11.2亿美元);预计投入研发费用总计2060亿日元(15.7亿美元)。
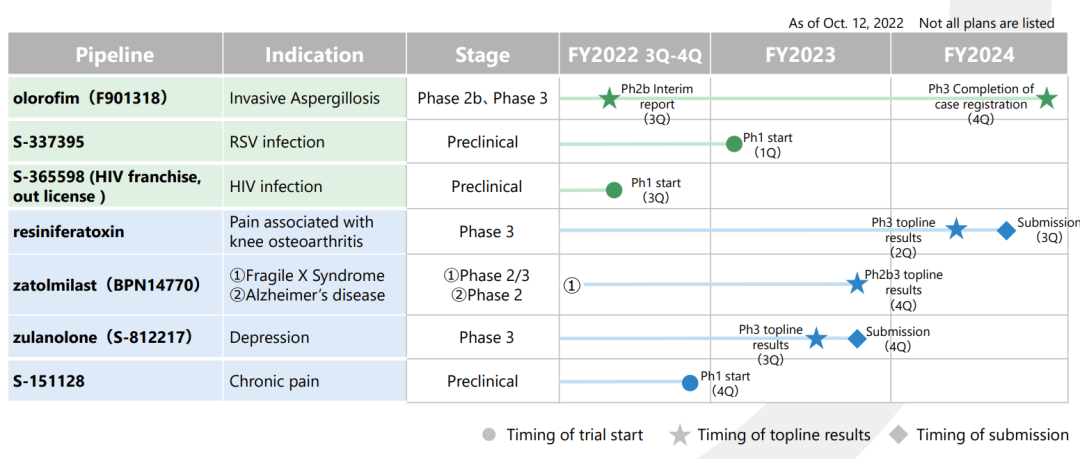
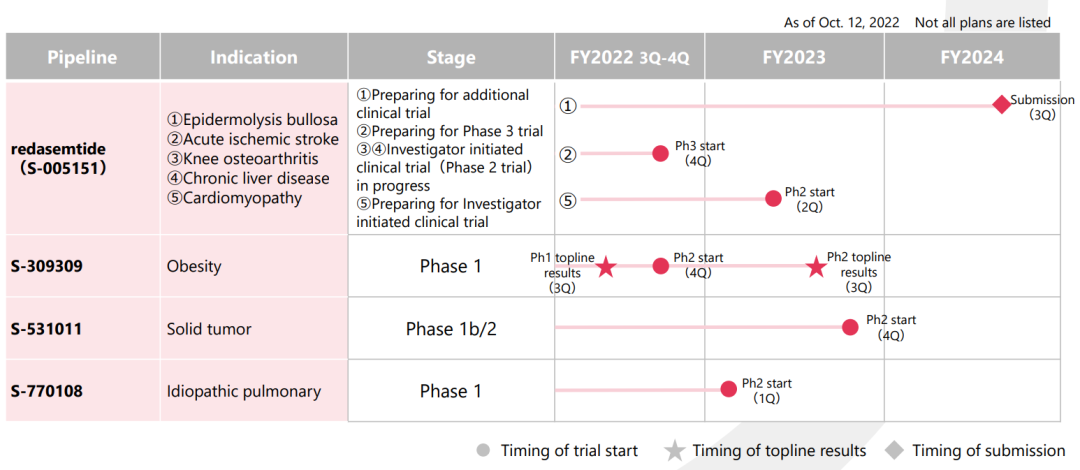
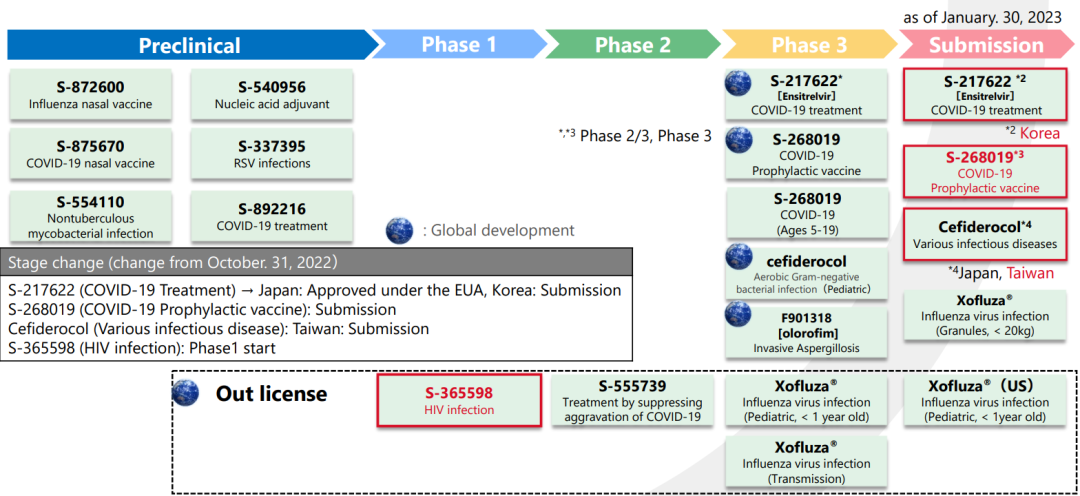
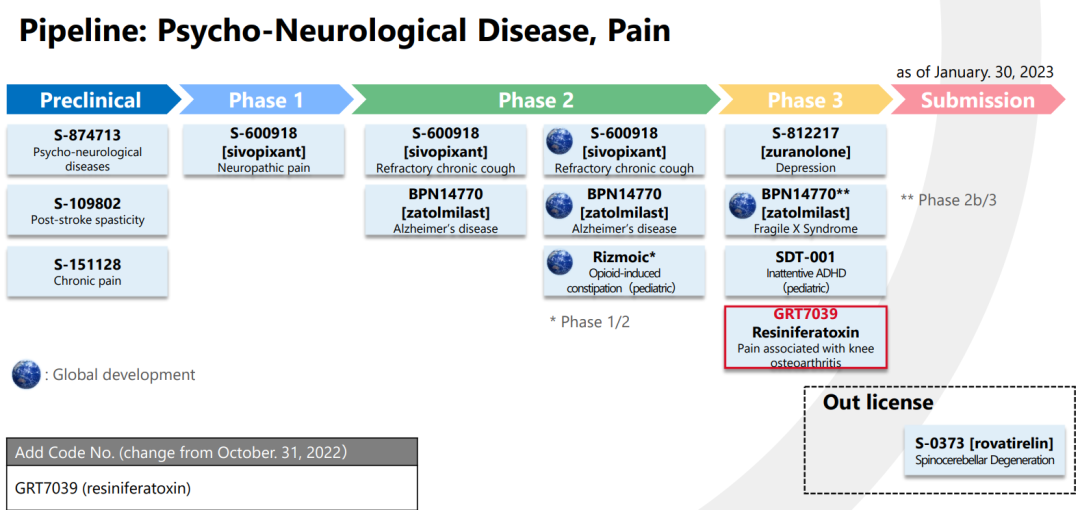
四、产品研发管线
(以下研发管线源自盐野义公司官网,日期截至2023年1月30日)
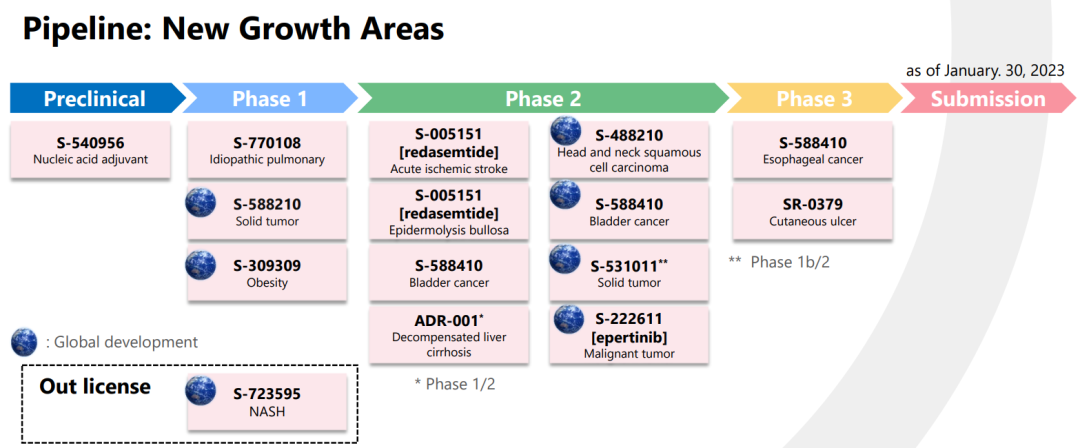
五、快速应对,开发新冠药物
一种新型抗病毒药物已被证实可以将轻至中度COVID-19症状缩短大约一天时间,该药物的制造商声称这种口服药物也可以用于治疗长期COVID-19。
2022年11月22日,3CL蛋白酶抑制剂恩赛特韦(ensitrelvir)的紧急使用授权获日本PMDA紧急授权批准上市,用于治疗新型冠状病毒感染。
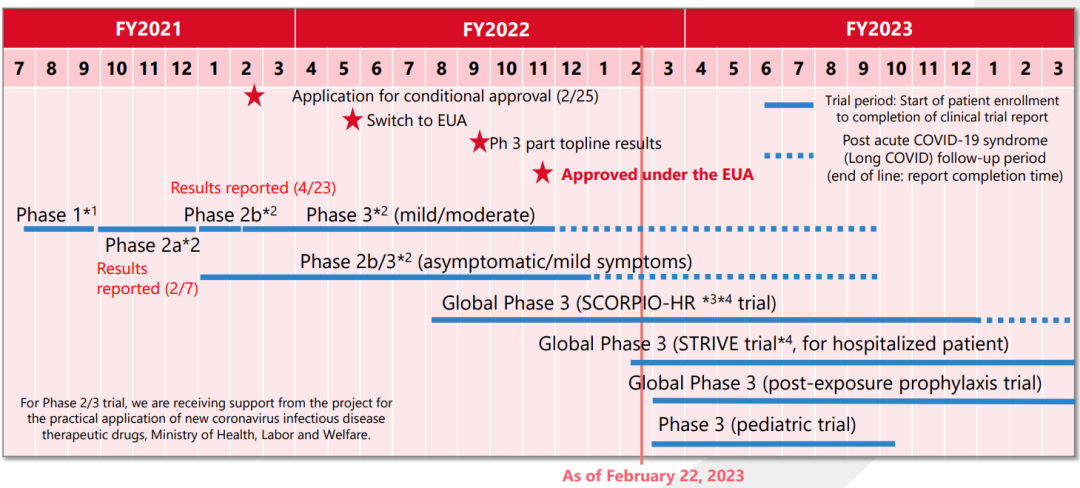
(Xocova®进展时间线)
据悉,由盐野义开发的ensitrelvir(恩赛特韦)(Xocova)是一种3CL蛋白酶抑制剂,是日本首个国产口服COVID治疗药物。该药为片剂,规格为125mg,12岁以上的儿童和成人第1天口服375mg,第2天到第5天口服125mg,每天1次。
ensitrelvir研发现状
截图来源:药融云全球药物研发数据库
Ensitrelvir作为一款口服3CL蛋白酶抑制剂,作用机制与辉瑞Paxlovid相同。SARS-COV-2具有3CL蛋白酶这种病毒增殖所必需的酶,ensitrelvir通过选择性地抑制3CL蛋白酶,从而达到抑制SARS-COV-2增殖的效果。
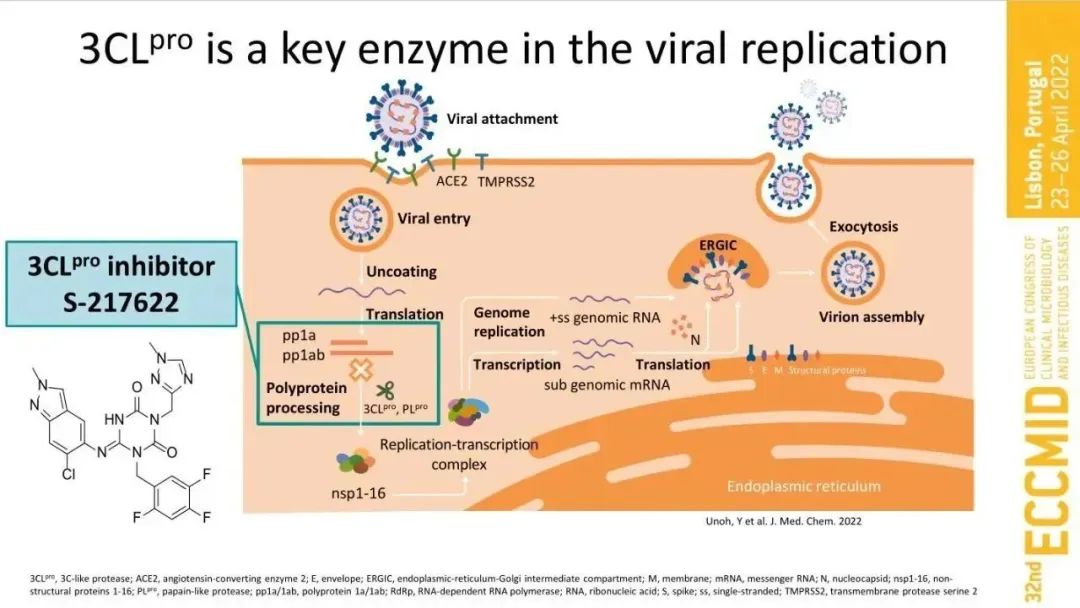
3CL蛋白酶是新型冠状病毒(SARS-CoV-2)增殖所必需的酶,恩赛特韦可以选择性地抑制3CL蛋白酶从而阻断SARS-CoV-2的增殖。恩赛特韦与辉瑞公司的帕罗韦德不同,其不是肝药酶CYP3 A4的底物,因此无需联用肝药酶抑制剂(如利托那韦),可单药使用,口服生物利用度接近100%且药代动力学特性较为优异。
为了评估恩赛特韦在SARS-COV-2感染患者中的药效和安全性,盐野义制药公司开展了一项随机、双盲、安慰剂对照的II/III期床试验(JPRN-jRCT2031210350)。临床研究表明,与安慰剂组相比,使用恩赛特韦的第4天,低剂量组(125mg)和高剂量(250mg)组病毒滴度阳性患者比例分别下降了98.1%和94.6%,另外患者的临床症状显著改善。接受恩赛特韦治疗后,病毒洁除的中位时间缩短了约50h。(此外,一项关于恩赛特韦全球范围的III期、多中心、随机、双盲研究(SCORPIO-HR试验)正在进行中。)
此次批准主要基于ensitrelvir的II期(包括IIa和IIb,共497名受试者)和III期(共1821名受试者)临床数据。II期临床旨在评估ensitrelvir作为COVID-19的治疗药物的疗效和安全性。
IIa期结果显示,在抗病毒方面,与安慰剂组相比,S-217622组能够实现病毒滴度和病毒RNA的迅速下降。IIb期在日本和韩国招募了428名患者,随机接受安慰剂和ensitrelvir的高低两种剂量治疗。
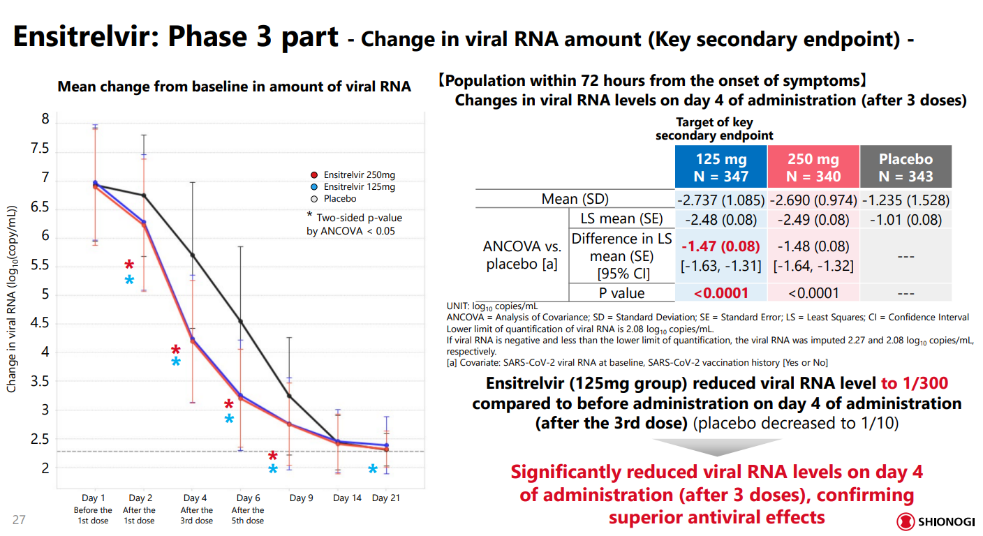
结果显示,ensitrelvir表现出对SARS-CoV-2病毒的快速清除。与安慰剂相比,ensitrelvir在第2、4、6和9天显示病毒RNA显著减少;在第4天(第3剂之后),病毒滴度阳性的患者比例与安慰剂相比减少了约90%;将传染性病毒的脱落时间缩短了1-2天。而在症状改善上面,12种COVID-19症状的总分没有显著差异,但事后分析显示ensitrelvir在5种“呼吸和发烧”症状的综合评分有所改善。
III期临床在日本、韩国和越南共招募了1821名COVID-19轻/中度症状患者,主要评价每天口服一次ensitrelvir(2个剂量组:高剂量和低剂量)相较于安慰剂,持续5天评估的临床症状缓解效果。
在该人群中,与安慰剂相比,接受低剂量ensitrelvir(在日本提交批准的剂量水平)治疗的患者首次缓解五种COVID-19症状(鼻塞或流鼻涕、喉咙痛、咳嗽、发热或发烧、精力不足或疲倦)的中位时间显著缩短:167.9vs192.2小时,24小时差异显示统计学显著性(p=0.04)。
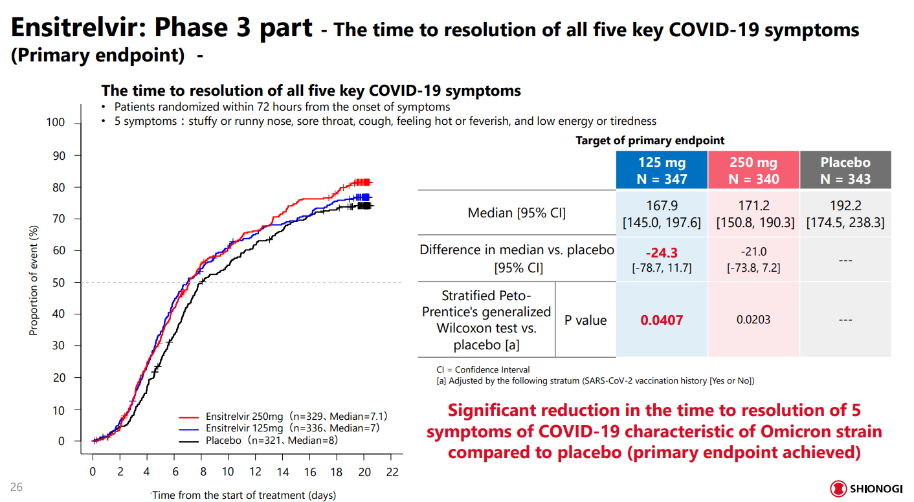
同时,ensitrelvir在第4天(第三次给药后)也显示出病毒RNA载量的显著减少。
其实ensitrelvir的上市之路并不顺利。2022年4月,盐野义宣布不建议孕妇口服使用该药物,因为动物试验发现给药后胎儿异常,有致畸风险。消息一出,舆论哗然,盐野义股价大跌。6月22日,ensitrelvir紧急使用申请被日本PMDA暂缓,称“需要进一步讨论”,更是为其蒙上了一层挥之不去的阴影。数次受挫,ensitrelvir凭借更多数据终于获批。
六、盐野义称Xocova在美国获批后,销售额预计达20亿美元
该公司预计,如果盐野义的COVID-19药物在美国获得批准,其年销售额将轻松达到20亿美元。盐野义将Xocova视为该公司在与大流行相关的治疗领域中最重要的押注之一。
虽然Xocova推向市场的时间比盐野义最初预期的要晚,因为日本监管机构两次要求提供更多数据,但该公司表示,研究的中期结果表明,服用该药物可以减少患者患上长期COVID的可能性。
Teshirogi在接受采访时说:“如果您足够快地和足够锐利地杀死病毒,长期遭受COVID的概率就越低。这是我们的假设,但我们需要证明这一点。”
与此同时,竞争药物也受到密切关注,因为它们可能会产生类似的效果。根据美国退伍军人事务部圣路易斯医疗保健系统的一项研究,辉瑞公司的抗病毒药物Paxlovid可以降低患者发展出许多长期COVID症状的风险。
该公司的首席执行官Teshirogi预计在2024年冬季,该药物将获得美国批准,前提是由美国国家卫生研究院部分资助的III期临床试验成功。“基于辉瑞公司预计2023年COVID-19相关销售额将超过200亿美元的预测,我认为从COVID-19市场中赚取20亿美元并不是非常困难。”他说道。
盐野义近年来将其80%的研发预算投入到冠状病毒治疗方案中。一种基于重组蛋白的COVID-19疫苗已提交日本审批。该疫苗正在为Omicron变种进行改装,同时一种鼻腔吸入版本也正在研究中。但日本几乎所有的COVID疫苗接种都是mRNA类型的。
政府取消了数千万剂阿斯利康和Novavax等非mRNA疫苗的订单,这给盐野义等公司的非mRNA疫苗前景蒙上了一层阴影。该公司对COVID项目的重大投资引起了一些分析师的担忧,认为其主力药品管道正在停滞不前。
“我没有遗憾,”Teshirogi说道,他补充道,股东和公众的期望要求盐野义将其资源投入到抗击COVID上。
参考:
NMPA/CDE;
药融云数据,vip.pharnexcloud.com/?mh;
FDA/EMA/PMDA;
相关公司公开披露(除标注外,正文图片均来自企业官方);
https://www.盐野义.com/global/en/
https://www.盐野义.com/global/en/company/history/museum.html
冯晓茹《恩赛特韦(Ensitrelvir,Xocova)》,中国药物学杂志,第33卷第2期
http://www.bigdeal.cn/plus/news.php?aid=88168
https://www.fiercepharma.com/pharma/盐野义-nabs-japanese-approval-rival-covid-19-antivirals-merck-and-pfizer
https://www.thepharmaletter.com/article/盐野义-presses-on-with-xocova-research-following-japanese-approval
https://mp.weixin.qq.com/s/3za40XAA-Hwfh_WLbivPCw
https://www.businesswire.com/news/home/20230215005658/en/盐野义-Advances-Ensitrelvir-Fumaric-Acid-COVID-19-Antiviral-Clinical-Program
https://www.reuters.com/business/healthcare-pharmaceuticals/盐野义-sees-covid-pill-reaping-2-billion-annual-sales-upon-us-approval-2023-02-27/
UNOH Y,UEHARA S,NAKAHARA K,et al. Discovery ofS-217622 , a noncovalent oral SARS-CoV-2 3CL proteaseinhibitor clinical candidate for treating COVID-19[ J]. J MedChem.等等。
想要解锁更多药企信息吗?查询药融云数据库(vip.pharnexcloud.com/?zmt-mhwz)掌握药企公司基本信息、投融资情况、产品管线分布、药物销售情况与各维度分析、药物研发情况、年度报告、最新进展动态、临床试验信息、市场规模与前景等,以及帮助企业抉择可否投入时提供数据参考!注册立享15天免费试用!

<END>























































 川公网安备51019002008863号
川公网安备51019002008863号 本网站未发布麻醉药品、精神药品、医疗用毒性药品、放射性药品、戒毒药品和医疗机构制剂的产品信息
本网站未发布麻醉药品、精神药品、医疗用毒性药品、放射性药品、戒毒药品和医疗机构制剂的产品信息
收藏
登录后参与评论
暂无评论