苏州瑞博生物技术股份有限公司(简称“瑞博生物“)成立于2007年,是一家致力于开发RNA干扰(RNAi)药物的创新型研发企业,是中国小核酸技术和小核酸制药产业的主要开拓者和领军企业。
瑞博生物公司信息
截图来源:药融云投融资数据库
瑞博生物对标国际小核酸技术的创新前沿,致力于小核酸化学修饰和药物递送技术的迭代研发,建立了自主可控、全技术链整合的小核酸药物研发平台,支持小核酸药物从早期研发到产业化的全生命周期。自主研发的GalNAc小核酸药物递送技术平台RIBO-GalSTARTM具有国际竞争水平的高度特异肝靶向和高效、长效特征。公司多个品种管线已推进至临床试验阶段。同时,瑞博生物非肝靶向小核酸递送技术研究取得了显著进展,将进一步支持公司的可持续创新发展。
01.融资情况
据药融云数据库显示,瑞博生物现已完成至E轮融资,总融资金额近16亿人民币。
- 2016年1月,公司完成人民币1.25亿元的A轮融资;
- 2017年4月,公司完成人民币2.7亿元的B轮融资;
- 2019年12月,公司完成人民币2.03亿元的C1轮融资;
- 2020年3月,公司完成4.7亿元人民币的C2轮融资;
- 2020年9月,公司完成了2.5亿元人民币的C+轮融资;
- 2022年7月,公司完成了4000万美元的E1轮融资。
瑞博生物投融资情况
截图来源:药融云投融资数据库
02.研发管线
基于核心技术平台,瑞博生物披露了针对心血管和代谢性疾病、肝病、罕见病及其他、眼科疾病不同适应症的26个在研管线。
瑞博生物在研管线
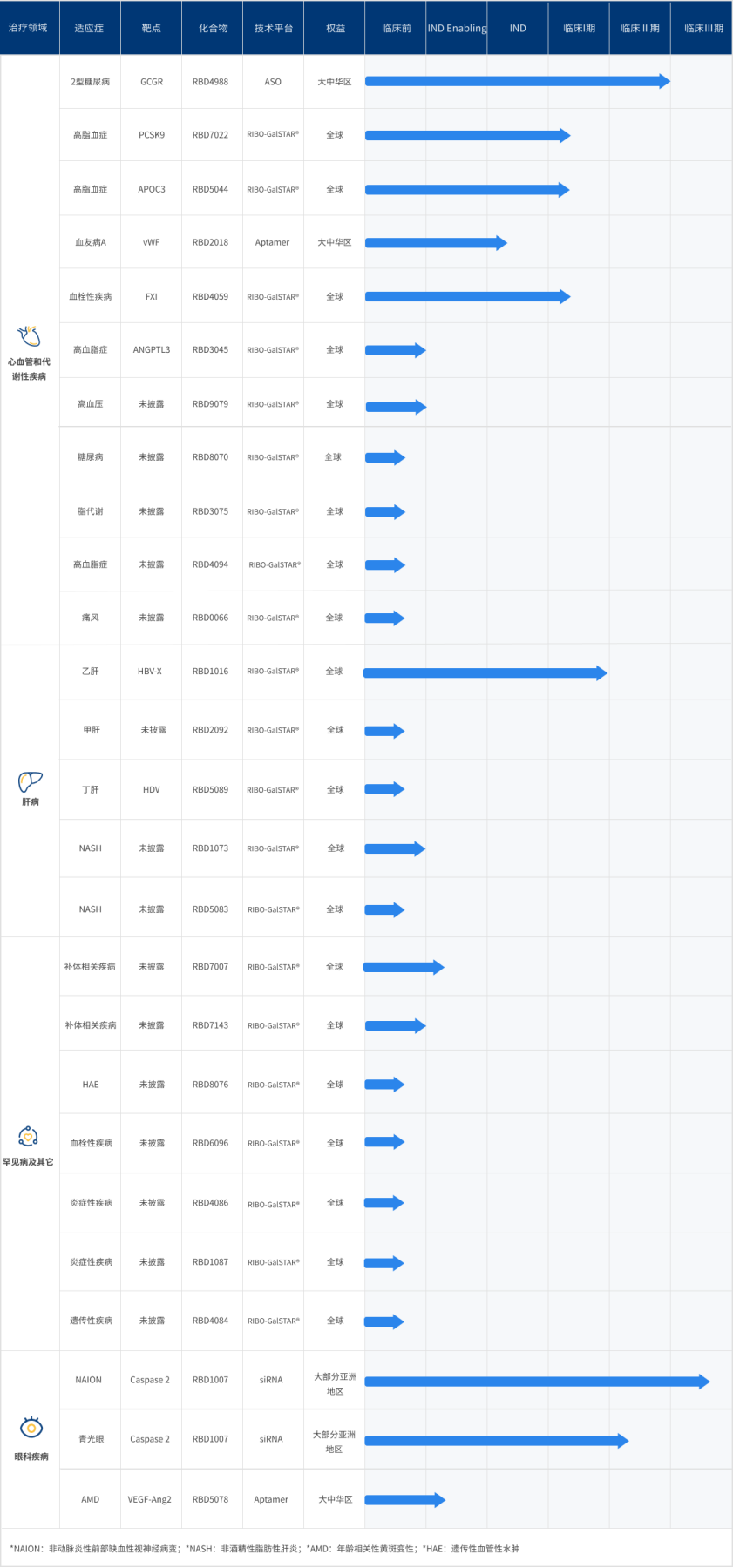
图片来源:瑞博生物官网
关键产品
RBD7022:一种针对高血脂症的GalNAc缀合的siRNA药物,通过抑制PCSK9(前蛋白转化酶枯草溶菌素9)表达,减少LDL-R(低密度脂蛋白受体)溶酶体降解,增加肝细胞表面LDL-R数量,实现降低血液中LDL-C(低密度脂蛋白胆固醇)水平的目标。首次人体临床试验申请已在中国获批。
RBD5044:一种针对高甘油三酯血症的GalNAc缀合的siRNA药物,可以抑制肝细胞APOC3(载脂蛋白C3)表达,上调脂蛋白脂肪酶和肝细胞受体介导的残余颗粒摄取,促进富甘油三酯脂蛋白(TRLs)上甘油三酯(TGs)的水解,实现降低血液中TG水平的目标。非临床研究和IND申请正在进行中。
RBD1016:一种针对乙肝的GalNAc缀合的siRNA药物,可以覆盖中国以及欧美乙肝患者中占绝大多数的A-E基因型乙肝患者;非临床研究显示可以高效、长效降低血清和肝组织HBsAg,单次给药对HBsAg抑制可持续近6个月;是目前全球唯一单药实现临床前动物血清学转换的药物,提示RBD1016将具有Best-In-Class的潜力,如在临床试验中得到确认,则有望实现乙肝患者的功能性治愈。在澳洲已完成临床Ia期研究,在中国香港的的Ib期临床研究正在进行中。II期临床试验在准备中。
作为瑞博生物自主研发的GalNAc-siRNA创新药,RBD1016在临床研究中获得的良好的安全性和预期的药代特征,是对瑞博生物建立的基于GalNAc-siRNA肝靶向递送技术和小核酸药物研发平台的有力验证。瑞博生物预期将有更多GalNAc-siRNA产品进入临床开发阶段。
RBD1007:一种靶向Caspases 2视神经保护的siRNA药物,通过RNAi抑制靶基因的表达,阻止视网膜神经节细胞(RGC)凋亡和继发的神经轴突退化,从而防止视力和视野进一步恶化,达到保护视力的治疗效果。首个开发的临床适应症为尚无临床标准治疗的非动脉炎性前部缺血性视神经病变(NAION),RBD1007有望成为 First-In-Class的视神经保护药物。目前全球已经完成1个临床I期研究和1个Ⅱ/Ⅲ期国际多中心临床研究(其中包括34例中国受试者),临床试验数据分析结果支持针对具有极大未满足临床需求的NAION亚组患者人群开展III期确证性临床研究,IND申请正在准备中。计划以后将陆续开展针对开角型青光眼适应症和其它伴有视神经病变需要视神经保护多种眼科疾病的临床研究。
RBD4988:一种针对2型糖尿病的反义核酸药物,有望成为第一个作用于胰高血糖素受体(GCGR)的药物,目前无同类靶点的品种上市。该产品可通过双重作用机制发挥降糖作用,即在降低肝葡萄糖生成量的同时,又可升高GLP-1产生胰腺保护功能。本品有望满足对仅能通过对胰岛素通路进行干预但疗效不佳患者的临床需求。目前全球已经完成1个临床Ⅰ期研究和3个Ⅱ期研究,在中国展开针对2型糖尿病的两项Ⅱ期临床试验已于近期顺利完成。
RBD2018:一种靶向血管性血友病因子(vWF)的核酸适配体,拟开发的适应症为血友病A。药物分子与vWF特异性结合,阻止vWF和其携载的FVIII的清除,延长FVIII的半衰期,同时提高FVIII活性。本品国外合作方已经完成临床试验I期和IIa,结果显示良好安全性和有效性。瑞博拥有产品大中华区开发、生产和商业化权益,计划启动针对血友病A的临床试验。
03.技术平台
1、小核酸序列设计平台
公司自主研发了小核酸序列设计平台,并通过长期的小核酸设计和验证实践不断对该平台进行升级优化。小核酸序列设计平台对 50 余项参数进行全面分析,综合考虑序列保守性、同源性、免疫原性、脱靶等因素,可快速大量针对 siRNA序列实现跨物种序列比对和同源性分析,从而提供特异性高、有潜在活性的优质小核酸序列。同时,公司建立了与小核酸药物设计平台匹配的小核酸高通量筛选(HTS,High throughput screening)平台,可以高效获得先导化合物,快速推进小核酸候选化合物的产生。
该平台设计团队具有二十余年的小核酸技术研究经验,对小核酸分子的有效性、特异性、稳定性、成药性均有深入的研究。以此为基础,通过强有力的生物信息学手段形成了功能全面的设计平台。
2、小核酸药物递送技术平台
小核酸药物主要的技术难点在于递送技术、稳定化修饰和药学研究等,其中小核酸递送技术是制约全球产业发展的瓶颈技术。公司自主研发了 GalNAc 肝靶向递送技术,实现与全球领先企业并跑的技术水平;另一方面,公司通过与 LTC公司合作,掌握并推进了基于脂质体的小核酸递送技术,形成了公司在递送技术上的技术储备。此外,公司建立了评价不同小核酸递送技术的研究平台,并持续投入研究力量开发针对肺靶向、中枢神经靶向、局部给药等其他组织和器官的小核酸递送手段,以保持公司在小核酸药物递送技术方面的先进性。
相比于脂质体等其他递送技术,GalNAc 代表了当前主流的小核酸递送技术,具有更优的特异性、高效性、长效性和安全性。全球仅有为数不多的公司掌握了GalNAc 递送技术,公司研发的 SR016 是我国首款自主研发、申报 IND 的采用GalNAc 肝靶向递送技术的 siRNA 新药。
公司 GalNAc 递送技术的先进性体现在以下四个方面:(1)特异性(2)高效性(3)长效性(4)安全性
3、小核酸稳定化修饰平台
未经修饰的小核酸极易降解,伴有不同程度的脱靶效应和/或免疫原性。小核酸修饰对小核酸的活性有不同程度的影响。公司基于 siRNA 降解机制的系统研究,分析了各种不同的 siRNA 修饰组合,评估了百余种不同的核酸稳定性化学修饰方式,针对不同活性与脱靶规律建立和优选了多种修饰策略,可显著增强小核酸药物的稳定性,实现其对体内靶基因的高活性抑制和持久药效维持,单次给药后药效可持续数月;同时有效削弱或消除 siRNA 脱靶效应和/或免疫原性,提高了靶点特异性,从而避免因 siRNA 脱靶引发的体内毒性。公司自主研发形成了独特的小核酸稳定化修饰平台(RSC),可保证所开发的小核酸药物活性高、稳定性好、特异性强、安全性优,目前公司单剂量小核酸药物达到靶基因数月的沉默,同时在食蟹猴 NOAEL 高达 400 mg/kg,充分体现出高安全性。
4、小核酸药物生物分析平台
生物基质(如血浆、尿液、组织等)中药物浓度的测定是开发小核酸药物的重要环节,目前我国尚无小核酸生物样品分析的标准方法和指导原则。公司率先建立了高敏感度、高特异性、可重复性的小核酸检测方法,开发了 ELISA、荧光分析、紫外分析、质谱分析、qPCR 分析等方法,可检测小核酸全长序列及代谢产物,均可应用于鼠、猴以及人药代动力学研究中的定量检测,能够方便快捷地检测细胞、动物组织、临床样本等复杂基质中的小核酸浓度,特异性好、灵敏度高,极大地支持了小核酸药物的非临床和临床药代动力学研究。
5、小核酸药学研究平台
根据小核酸药物的特性以及创新药研发各阶段的特点,公司建立了完备的小核酸创新药的药学研究平台。公司通过采用系统研发的理念和方法,对小核酸原料药和制剂进行了系统的生产工艺开发和质量研究,满足药物发现早期研究、临床前研究,临床试验申报和临床研究各阶段对小核酸药物的药学要求。针对小核酸原料药的质量属性和固相合成生产工艺特点,公司开展了小核酸原料药的生产工艺研究、中试开发和放大生产,并对多批次生产的工艺参数,物料和产品属性进行分析,制定了小核酸原料药生产工艺和质量控制策略,对物料(包括核苷单体、固相载体、纯化填料、试剂和溶剂等)、中间体的质量以及工艺过程进行了有效的控制,保证了原料药的质量。公司已建成并投入使用国内首个符合 GMP 要求的中试规模小核酸固相合成和纯化生产设施。目前已具备单批生产百克级、年产 5 公斤小核酸的中试研发生产能力。公司已经成功完成多个不同化学修饰小核酸品种原料药开发和临床批次的生产。
根据小核酸原料药的性质,公司开展了制剂处方的开发和关键工艺参数的研究,建立生产工艺和质量控制策略。通过向 CMO 生产基地的技术转移和 GMP制剂批次的生产,实施对物料(原料药、辅料、包材等)和中间体的质量以及GMP 生产过程的控制策略,从而确立对制剂的关键质量属性的保障。公司已经成功完成多个小核酸注射剂品种的开发和 GMP 临床批次的生产。
6、小核酸单体研发平台
核苷单体是小核酸药物研发生产和其他应用的重要关键物料。非天然核苷单体的引入可以起到增强靶向性、维持或提升活性、增强稳定性和防止脱靶等改善小核酸成药性的作用。公司持续探索新的非天然核苷单体研发,不断优化分子设计与筛选的研发流程,以获得有自主知识产权的单体,解决现有单体种类不能满足的小核酸药物开发的上述成药性需求。核苷单体的质量与成本是小核酸药物商业化的关键因素,公司掌握了单体生产过程中杂质控制、成本降低及质量控制等形成多项关键技术,在单体生产和质量控制上具备深厚的工艺开发和生产基础,已开发了近 50 种不同修饰的核苷单体的生产工艺。
04.最新进展
2023年2月,瑞博生物宣布,反义寡核苷酸(ASO)药物ISIS449884注射液针对2型糖尿病的两项2期临床试验顺利完成,两项临床研究均达到主要研究终点。
2023年2月,瑞博生物自主研发的抗血栓小核酸药物(RBD4059注射液)已在澳大利亚获得HREC批准,启动首次人体临床试验。
2022年1月,RBD1016首次人体临床试验显示RBD1016具有良好的安全性和耐受性。
参考资料:
[1] 药融云数据库
[2] 瑞博生物官网、招股书
想要解锁更多药企信息吗?查询药融云数据库(vip.pharnexcloud.com/?zmt-mhwz)掌握药企公司基本信息、投融资情况、产品管线分布、药物销售情况与各维度分析、药物研发情况、年度报告、最新进展动态、临床试验信息、市场规模与前景等,以及帮助企业抉择可否投入时提供数据参考!注册立享15天免费试用!

<END>























































 川公网安备51019002008863号
川公网安备51019002008863号 本网站未发布麻醉药品、精神药品、医疗用毒性药品、放射性药品、戒毒药品和医疗机构制剂的产品信息
本网站未发布麻醉药品、精神药品、医疗用毒性药品、放射性药品、戒毒药品和医疗机构制剂的产品信息
收藏
登录后参与评论
暂无评论