
“Apicture is worth a thousand words, well, then a movie is worth thousands of pictures. ”如果说一张照片胜过千言万语,那么一部电影胜过千张照片。这是Relay Therapeutics的董事会主席Alexis Borisy对自家公司评论。
Relay是一家以分子动力学模拟见长的AI药物发现公司,旨在将蛋白质结构和运动的深刻理解应用于药物发现。该公司将基因组数据、计算科学以及实验科学深度融合,致力于改变药物发现的过程。

随着2003年人类基因组计划的完成,人们对遗传变异、蛋白质功能障碍和疾病病理学之间联系的理解不断进步;且得益于计算能力和实验技术的更新迭代,科学界对疾病的分子理解呈指数增长,开创了当前的精准医学时代。精准医学旨在对经过遗传学验证的靶点(即可能与疾病生物学机制有关的遗传变异)进行特异性和有效的药物治疗,即靶向治疗。
然而迄今为止,一些靶蛋白一直难以使用传统的方法进行药物开发,例如基于结构的药物设计(SBDD)。随着结构生物学的发展,从20世纪后期开始,SBDD成为了一种重要的药物研发策略。不过,SBDD虽然非常适合解决一些药物发现问题,例如正构位点激酶抑制剂,但它对蛋白质片段静态图像的依赖限制了准确理解蛋白质在自然状态下的动态行为的能力。蛋白质具有特定的氨基酸序列以及独特的分子结构,且不断运动。静态的、刚性的晶体结构不能准确地代表蛋白质在其生物学背景下的动态性质,这在一定程度上阻碍了药物的设计。
于是在基因组数据激增、实验技术快速发展、计算能力和速度飞速进步的新世纪,Relay Therapeutics应运而生。这家诞生于2016年的AI药物发现公司正在将行业内对于蛋白质靶点的理解从过去的静态视图转变为基于蛋白质运动的动态视图,形成一种新的范式,并将这些基于蛋白质运动的新见解应用于药物发现和设计,该公司称之为基于运动的药物设计(Motion Based Drug DesignTM,MBDD)。

DynamoTM药物发现平台
Relay Therapeutics的DynamoTM药物发现平台集成了一系列广泛且定制的前沿实验和计算方法,与公司的专家团队经验相结合,将蛋白质运动作为药物发现和设计的核心,并不断整合新的实验和计算技术以赋予平台更多可能性。
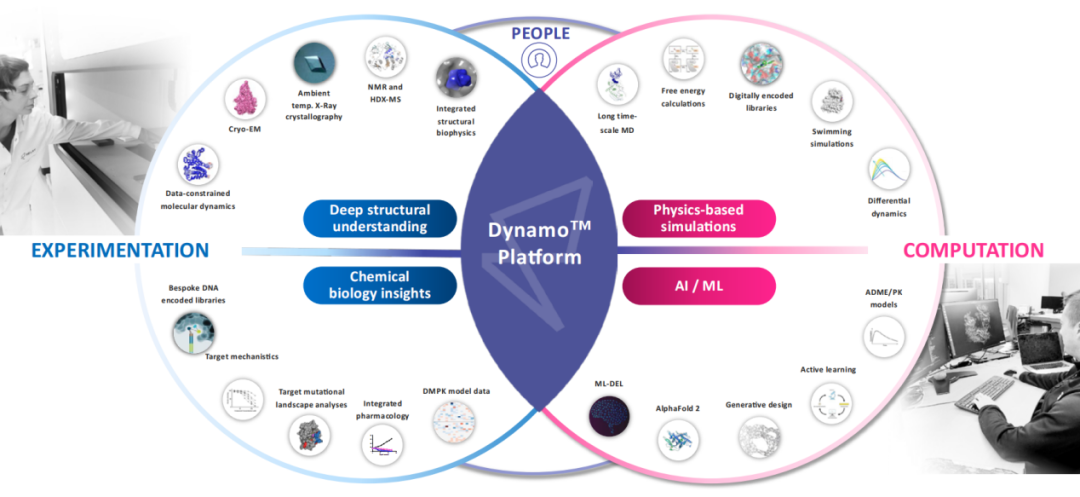
该平台的实验技术提供对结构生物学和化学生物学的深刻理解,包括冷冻电镜(CryoEM)、室温X射线晶体衍射、核磁共振(NMR)和氢氘交换质谱(HDX-MS)、数据约束下的分子动力学、定制DNA编码文库、DMPK模型数据等;计算技术提供基于物理的分子动力学模拟和人工智能/机器学习能力,包括长时间尺度分子动力学(MD)模拟、自由能计算、ADME/PK模型、主动学习、AlphaFold2等。
2021年4月,Relay Therapeutics斥资万美元收购AI药物发现公司ZebiAI,该公司是将大规模实验性DNA编码文库应用于机器学习药物发现(ML-DEL)的先驱,此次收购将增强DynamoTM平台的潜力。除此之外,ZebiAI的股东有资格获得8500万美元的里程碑付款。
Anton 2超级计算机&天才计算机科学家:
其中,最为关键的当属Anton 2超级计算机的部署,用于对蛋白质进行分子动力学模拟,该部署源自Relay Therapeutics从2016年8月开始与D.E. Shaw Research建立的合作,该公司是一家在David E.Shaw博士科学领导下运营的计算生物化学研究公司。据了解,Anton超级计算机执行分子动力学(MD)模拟的速度比当时最快的通用超级计算机快100倍,其非凡的性能及其对科学和制药研究的重要贡献使其两度获得高性能计算领域的最高荣誉Gordon Bell奖。
而David E.Shaw博士则是计算机领域顶尖的“天才”级人物。他是斯坦福大学计算机博士,不到30岁就进入哥伦比亚大学任教,并开展大规模并行计算研究。之后他投身华尔街,加入摩根士丹利,利用计算机技术进行量化交易。1988年,David E. Shaw博士创办了以自己名字命名的对冲基金DE Shaw & Co,采用专有算法进行证券交易,赚得盆满钵满。DE Shaw & Co.曾被《财富》杂志誉为“华尔街最引人入胜、最神秘的力量”,而David E. Shaw博士本人也因在高频量化交易方面的先驱作用在1996年被《财富》杂志称为“King Quant”(量化投资之王)。
后来,也许是内心的“极客”(狂热于技术)本质使他从金融行业重新回归科学界。2001年,David E. Shaw博士开始转向计算生物化学的全职科学研究,特别是蛋白质的分子动力学模拟,并创办了前文提及的计算生物化学研究公司D.E. Shaw Research。2007年,第一代Anton超级计算机问世。据了解,D.E. Shaw Research也是Relay Therapeutics的投资者之一,而David E.Shaw博士则是Relay的联合创始人之一,同时他也是AI药物发现龙头Schrödinger最早的投资人。Relay的每个项目都有D.E. Shaw Research科学家的参与,尤其是在开发基于动力学的假设和识别先导化合物的药物发现阶段。

▲David E.Shaw博士
DynamoTM药物发现平台在三个关键阶段加速新药研发进程:
■ 靶点调制假设(Modulation Hypothesis):
首先通过蛋白质工程合成全长靶蛋白;再利用一系列蛋白质可视化方法,如冷冻电镜、室温X射线晶体衍射等,获得靶蛋白动态构象的丰富实验数据;然后将实验数据导入计算平台,以生成全长蛋白质在长的、生物学相关的时间尺度上的分子动力学模拟,从而确定潜在的结合口袋和靶点。
■ 苗头化合物识别(Hit Identification):
计算和实验能力的整合使得该平台能够设计以生理相关活动为基础、配体为中心的计算筛选。并将这些筛选数据输入机器学习组件,以快速识别药物发现过程中的苗头化合物。
■ 先导化合物优化(Lead Optimization):
将先进的机器学习模型和分子动力学模拟与药物化学、结构生物学、酶学和生物物理学能力紧密结合,以预测和设计能实现最理想特性的化合物,包括效力、选择性、生物利用度和类药性质。

开发策略:
作为一家AI药物发现公司,Relay拥有清晰的开发策略,针对已经过验证但过去难以成药的靶点开展药物发现工作:目标靶点是已知的疾病驱动因素、可利用公司的DynamoTM平台进行开发、具有明确的患者筛选策略、预期可快速进入临床概念验证。
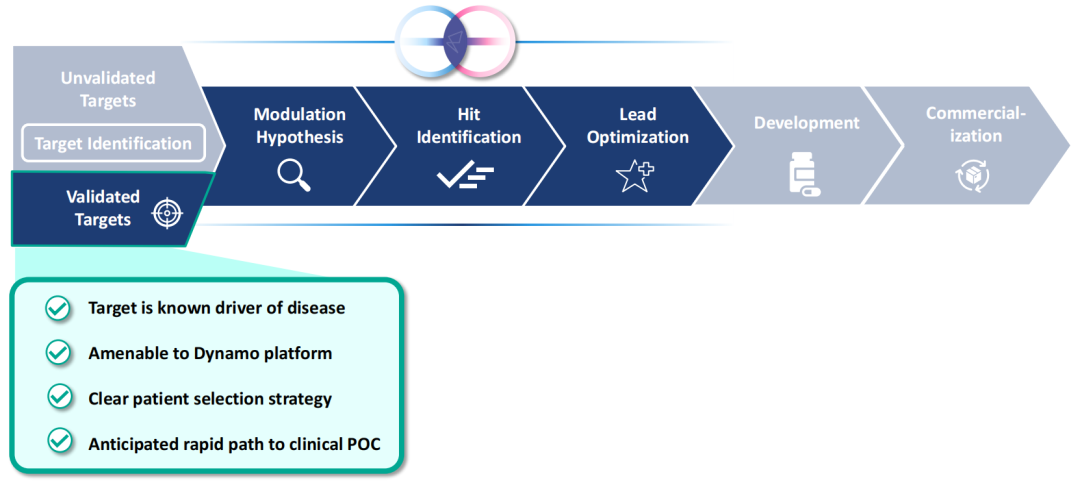
产品管线与计划
虽然Relay认为公司的DynamoTM平台有潜力适用于广泛的疾病相关蛋白质靶点,但公司目前专注于精准医学靶点,特别是针对肿瘤和遗传病的小分子疗法。
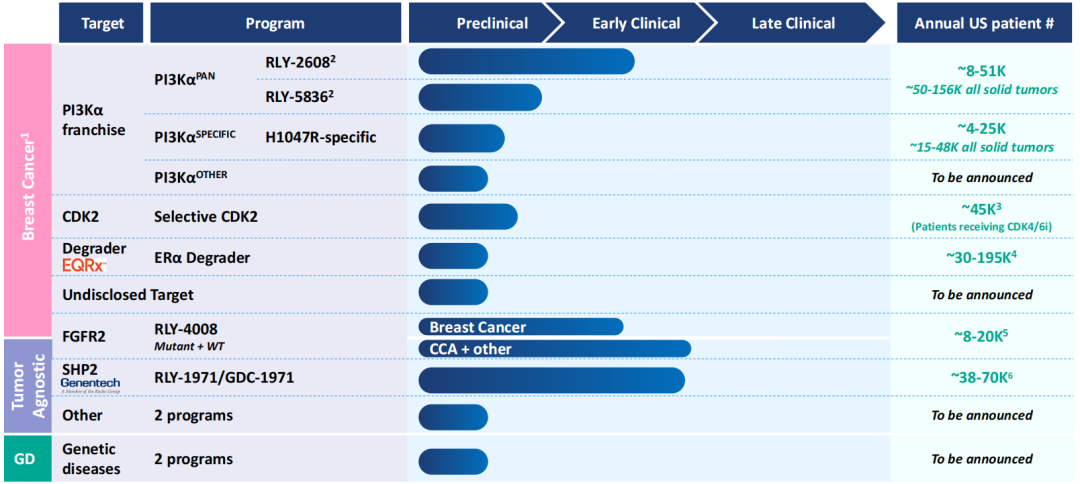
目前Relay拥有三款处于临床开发阶段的产品:RLY-4008和RLY-2608是公司Innovator产品组合(针对先前未解决的药物发现问题进行挑战)的一部分,以及RLY-1971是Challenger产品组合(针对已获批但存在不足之处的疗法发起挑战)的一部分。
FGFR2抑制剂RLY-4008:
RLY-4008是一种选择性成纤维细胞生长因子受体2(FGFR2)口服小分子抑制剂。FGFR2是一种在某些癌症中经常发生突变的受体酪氨酸激酶,是FGFR家族的四个成员之一,这组蛋白具有高度相似的蛋白质序列和特性。当前一些非选择性泛FGFR抑制剂已在携带FGFR2基因融合的肝内胆管癌(CCA)患者中证明了临床概念验证,但由于这些疗法同时对FGFR1和FGFR4具有抑制性,会不可避免地引起高磷酸血症和腹泻等副作用。
药融云数据(vip.pharnexcloud.com/?zmt-mhwz)显示,2022年1月,美国FDA授予RLY-4008治疗胆管癌(CCA)的孤儿药称号。根据Relay与FDA的讨论,公司推进了推荐剂量每日一次70mg针对未经泛FGFR抑制剂治疗的FGFR2基因融合胆管癌(CCA)的单臂试验,以支持可能的加速批准。
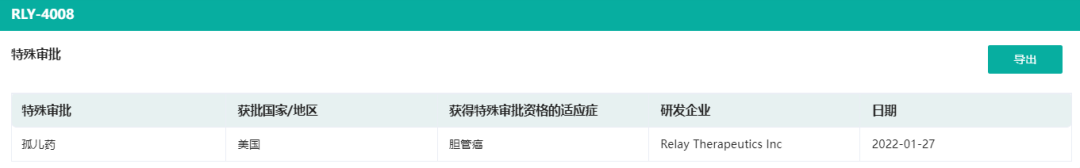
▲截图自药融云中国药品审评数据库
2022年9月,Relay在ESMO大会上公布了RLY-4008的1/2期ReFocus试验的积极中期数据。截至2022年8月1日,在接受2期推荐剂量(70mgQD)的17例未经泛FGFR抑制剂治疗的、携带FGFR2基因融合的胆管癌(CCA)患者中,客观缓解率(ORR)达到88.2%(15/17),疾病控制率(DCR)达100%,其中有一例患者接近完全缓解,并进行了治愈性切除手术;在所有剂量的FGFR2基因融合CCA患者中,ORR为63.2%;安全性数据与先前的分析一致,未观察到高磷酸血症和腹泻的显著脱靶毒性,未观察到4级或5级不良事件,大多数紧急不良事件是低级别、可监测、可管理,以及基本可逆的。
据披露,未经泛FGFR抑制剂治疗的、携带FGFR2基因融合的胆管癌(CCA)患者队列预计将于2023年下半年完成入组;来自非CCA扩展队列的初始数据预计将于2023年公布;全部剂量递增数据预计将在2023年上半年末发布。
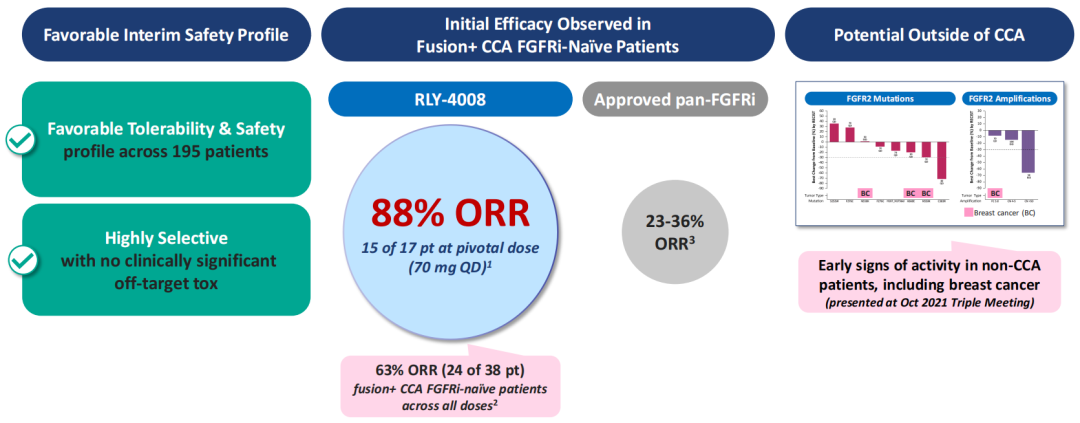
高选择性FGFR2抑制剂RLY-4008的设计正是分子动力学模拟技术的价值体现。由于FGFR1和FGFR2蛋白的静态结构具有高度相似性,当前已获批的FGFR抑制剂均不具备FGFR2亚型选择性。而Relay通过长时间尺度的分子动力学模拟发现了FGFR1和FGFR2蛋白结构的动态差异:二者的蛋白结构上都存在一个规律地上下开合的片段,但该片段在FGFR1蛋白上开合的频率却明显高于FGFR2,导致小分子药物在该位置与FGFR1结合后又脱落下来,而FGFR2却可与小分子药物在该位置紧密结合,从而实现对FGFR2的抑制。

Relay就是基于这种蛋白质结构的动态差异,设计出了对FGFR2蛋白具有高选择性的小分子抑制剂。体外试验显示,RLY-4008对FGFR2的选择性比FGFR1高200倍以上,RLY-4008有潜力成为首个针对FGFR2的高选择性小分子抑制剂。
2022年9月12日,肿瘤基因检测先驱Foundation Medicine与Relay Therapeutics宣布合作开发针对在研的FGFR2抑制剂RLY-4008的伴随诊断产品FoundationOne®CDx。
PI3Kα抑制剂RLY-2608及乳腺癌产品组合:
RLY-2608是首个在研的变构、泛突变(H1047X、E542X和E545X)、选择性PI3Kα抑制剂。PI3Kα信号通路与多种与癌症相关的细胞功能(包括细胞生长、增殖和存活)有关,是癌症中最常见的突变激酶。传统上,PI3Kα抑制剂的开发主要集中在活性位点或正构位点,但受限于对突变型PI3Kα与野生型PI3Kα缺乏选择性,导致治疗窗口较窄。Relay首次成功构建出突变型和野生型PI3Ka的全长蛋白结构,并通过长时间尺度的分子动力学模拟,发现了突变型PI3Ka蛋白上的一个新的变构结合口袋,从而设计出泛PI3Kα突变体选择性抑制剂。

体外试验显示出RLY-2608对突变型PI3Kα的高选择性以及抗肿瘤活性,同时减少了对血糖稳态的影响。在临床前模型中,RLY-2608与标准治疗方案相结合促进了ER+/HER2-乳腺肿瘤的消退。2021年12月,Relay启动了RLY-2608的首次人体临床试验。2022年4月,公司启动了该试验剂量递增部分的第二组,旨在评估RLY-2608与氟维司群联合治疗HR+/HER2–、PI3Kα突变型、局部晚期或转移性乳腺癌患者的疗效。初步临床数据预计将在2023年上半年进行更新。
Relay围绕乳腺癌布局了针对PI3Kα、CDK2、ERα等靶点的多个产品,除了RLY-2608之外,公司还于2022年6月宣布了HR+/HER2-乳腺癌产品组合中3个处于药物发现阶段的项目,包括:
- 选择性细胞周期蛋白依赖性激酶2(CDK2)抑制剂(预计将于2023年第四季度或2024年初推进临床);
- 雌激素受体α(ERα)降解剂(预计将于2023年确定一款候选药物),2021年8月,Relay与美国制药公司EQRx达成战略合作,针对已验证的肿瘤靶点开发和商业化新药,双方将共同承担药物的发现、开发和商业化成本以及平分销售净利润。该项目便是Relay与EQRx合作的一部分;
- 以及一款具有独特选择性和化学性质的泛突变型PI3Kα抑制剂RLY-5836。

Relay乳腺癌产品组合
SHP2抑制剂RLY-1971/GDC-1971:
RLY-1971是一款靶向SHP2的口服小分子、强效、选择性抑制剂,可与SHP2结合并稳定其非活性构象。SHP2可转导受体酪氨酸激酶(RTK)下游信号,通过RAS途径促进癌细胞存活和生长,同时SHP2在癌细胞对靶向治疗产生耐药性的方式中发挥关键作用。在过去,SHP2一直被认为是“不可成药”靶点,但随着近年来的研究进展,SHP2逐渐成为新药开发的前沿靶点之一。Relay认为,SHP2的抑制剂可作为单一疗法治疗携带特定突变的癌症,并阻断癌细胞耐药的共同途径。
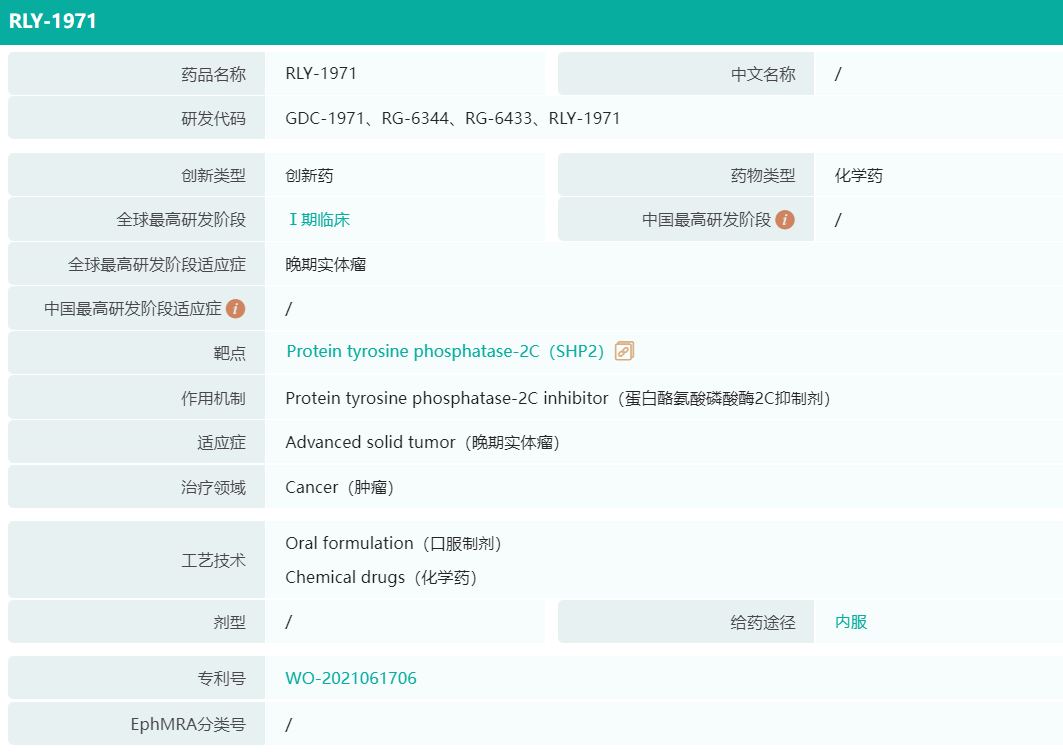
▲截图自药融云全球药物研发数据库
2020年第一季度,公司启动了RLY-1971的1期临床试验,用于治疗晚期实体瘤。2020年12月,Relay与罗氏旗下基因泰克就RLY-1971的开发和商业化签订了全球许可和合作协议。根据协议条款,截至2021年底,Relay已从基因泰克获得了7500万美元的预付款,以及2000万美元的里程碑付款,并有资格获得额外500万美元的近期付款。此外,Relay有可能获得高达6.95亿美元的里程碑付款以及全球净销售额的分成。2021年7月,基因泰克在1b期试验中启动了RLY-1971与其在研的KRASG12C抑制剂GDC-6036联用的队列。此外,RLY-1971与PD-L1抑制剂Tecentriq(阿替利珠单抗,atezolizumab)联用的试验已于2022年8月启动。
除了上述候选产品外,Relay还拥有超过5个处于药物发现阶段的项目,涵盖精准肿瘤学和遗传疾病。
财务状况
截至2022年6月30日,Relay Therapeutics拥有现金、现金等价物和投资额为8.38亿美元,足以支持公司到2025年的运营和资本支出。由于当前Relay的产品均处于在研状态,其运营收入主要来源于合作授权等,支出主要在于研发费用(包括资产收购支出)和一般及行政开支等。
下图为2021年全年Relay Therapeutics经营概况:
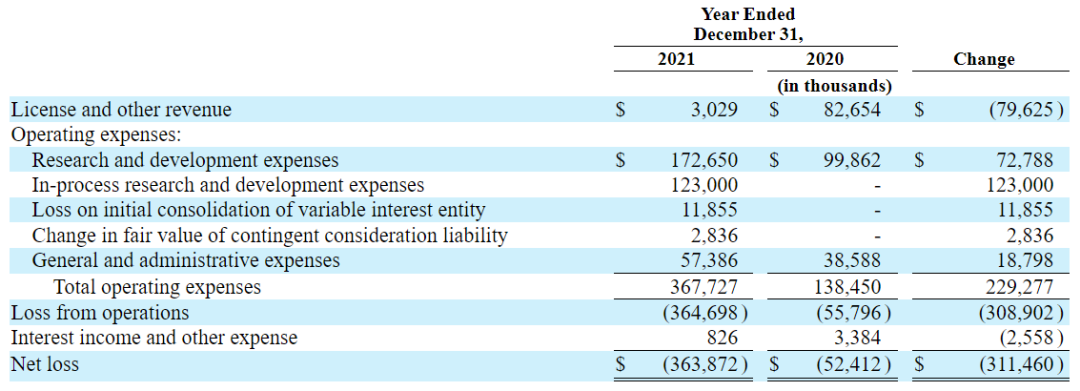
Relay在2020年已确认完成与基因泰克合作相关的8500万美元预付款收入,2021年公司仅从基因泰克获得300万美元的研发服务费用,且是公司全年主要收入。2021年公司研发费用为1.727亿美元,主要受员工增加、外部研发费用和临床试验费用增加的影响;一般及行政开支为5740万美元,主要是由于员工成本增加;全年净亏损为3.639亿美元,摊薄每股净亏损3.82美元,净亏损增加主要与2021年收购ZebiAI相关的一次性费用1.349亿美元有关。
下图为2022年上半年Relay Therapeutics经营概况:

公司2022年上半年无合作授权相关收入;研发费用为6050万美元,主要受员工增加、临床试验费用增加和临床前项目相关成本影响;一般及行政开支为1750万美元,主要是由于员工成本增加;上半年净亏损7680万美元,摊薄每股净亏损0.71美元。
9月8日,受公司披露RLY-4008积极临床数据影响,Relay当日股价上涨超23%,但在9月13日,公司股价急跌16.56%。9月12日,Relay宣布增发价值约3亿美元的普通股。

▲截图自雪球
此文仅用于向医疗卫生专业人士提供科学信息,不代表平台立场
参考:
NMPA/CDE;
药融云数据库,vip.pharnexcloud.com/?zmt-mhwz;
FDA/EMA/PMDA;
相关公司公开披露(正文图片除标注外,均来自企业官方);
https://relaytx.com/;
https://www.deshawresearch.com/;
https://www.schrodinger.com/;
AConversation with DavidShaw,https://queue.acm.org/detail.cfm?id=1614441;
Anton, ASpecial-Purpose Machine For Molecular DynamicsSimulation,https://cacm.acm.org/magazines/2008/7/5372-anton-a-special-purpose-machine-for-molecular-dynamics-simulation/fulltext;
https://ir.relaytx.com/news-releases/news-release-details/late-breaking-data-presented-esmo-congress-2022-demonstrate;
Relay提高其IPO发行价格和规模,预期募资近4亿美元,https://mp.weixin.qq.com/s/jTes6Z42saZ71ahL7sSn2w;
一文知悉:分子动力学模拟在高选择性抑制剂新药开发如何发挥作用?https://mp.weixin.qq.com/s/AV2ccJGOviG7r5blVGvNdg;
整合基因组、实验、计算开发新药的集大成者Relay,https://mp.weixin.qq.com/s/xfKdMInvtgg2acPj90zflw;等等。
<END>






















































 川公网安备51019002008863号
川公网安备51019002008863号 本网站未发布麻醉药品、精神药品、医疗用毒性药品、放射性药品、戒毒药品和医疗机构制剂的产品信息
本网站未发布麻醉药品、精神药品、医疗用毒性药品、放射性药品、戒毒药品和医疗机构制剂的产品信息
收藏
登录后参与评论
暂无评论