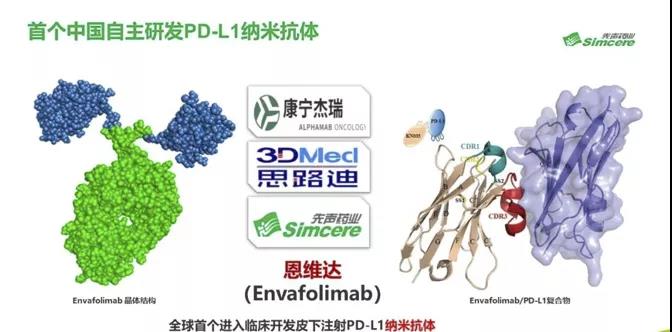
据药融云数据库显示,2021年11月24日,由康宁杰瑞生物制药研发、先声药业与思路迪医药三方战略合作的PD-L1单域抗体恩维达®(恩沃利单抗注射液)正式获得中国国家药品监督管理局(NMPA)批准上市(批准文号:国药准字S20210046),成为获准上市的皮下注射PD-L1抗体药物(此前获批为通过优先审批渠道)。
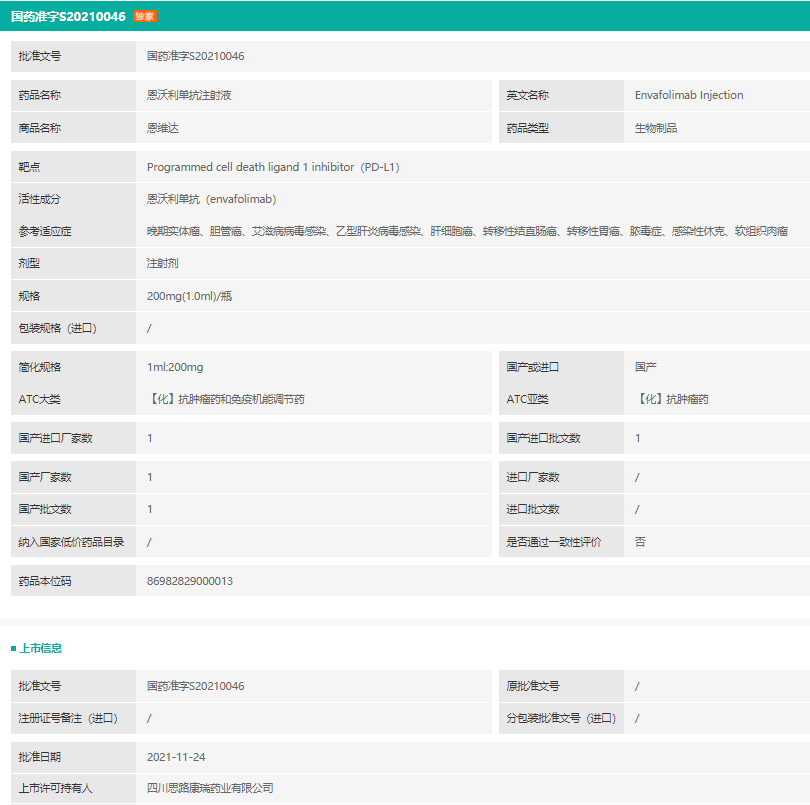
截图来源:中国药品批文数据库
据悉,恩沃利单抗属PD-L1单域抗体Fc融合蛋白,由sdAb和Fc段组成,由于sdAb的形式使然,KN035的分子量是完整抗体分子量的一半,这使其具有增强的穿透性,同时具有完整的抗原结合能力。Fc-介导的效应功能在恩沃利单抗中削弱,以限制其接触免疫系统并避免意外的不良免疫反应。

研发中考虑到肿瘤患者多次治疗与长时间给药的痛苦,及静脉萎缩或静脉输液不耐受的患者的临床需求,康宁杰瑞另辟蹊径探索新的抗体形态,并在稳定性、高粘度、工程化等方面重重突破,成功开发出皮下注射PD-L1抑制剂。

【通用名(商品名)】:恩沃利单抗注射液(恩维达®)
【规格】:200mg/1.0ml/瓶/盒
【适应症】:适用于不可切除或转移性微卫星高度不稳定(MSI-H)或错配修复基因缺陷型(dMMR)的成人晚期实体瘤患者的治疗,包括既往经过氟尿嘧啶类、奥沙利铂和伊立替康治疗后出现疾病进展的晚期结直肠癌患者以及既往治疗后出现疾病进展且无满意替代治疗方案的其他晚期实体瘤患者。
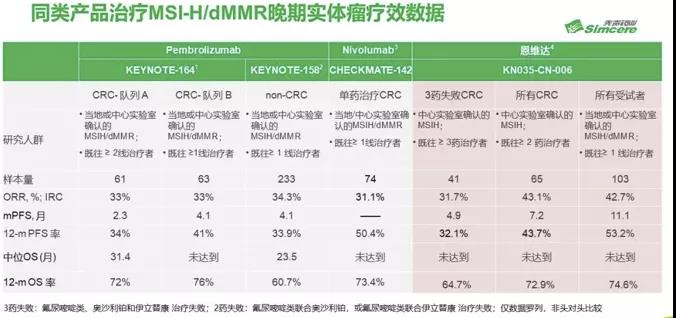
恩沃利单抗国内临床II期研究的结果显示,恩沃利单抗单药(150 mg QW皮下注射给药)用于103例MSI-H/dMMR实体瘤患者二线以上治疗的客观缓解率(ORR)为44.7%,其中包括了65例结直肠癌患者,ORR达到43.1%。总人群中位无进展生存期(PFS)为11.1个月,1年总生存(OS)率为73.6%。恩沃利单抗的国内II期临床研究的安全性数据显示,103例MSI-H/dMMR实体瘤患者中,16例患者(15.5%)发生3-4级与药物相关治疗期间不良事件(TEAE),无研究药物相关5级TEAE。

据药融云数据库最新查询显示,恩沃利单抗单价为:5980元/瓶。最新消息显示的【患者PAP援助政策】:买4支申请援助4支,再买8支申请援助至PD。符合条件的患者约合7.2万/2年。
此外,值得注意的是,其余市场上几家国产企业(信达生物、君实生物、百济神州、恒瑞医药)目前进入2021国家医保目录价格非常可观,总体在3.78-5.12万/年。
参考:
NMPA/CDE;
药融云数据,www.pharnexcloud.com;
FDA/EMA/PMDA;
相关公司公开披露;
www.alphamabonc.com;等等。
<END>





















































 川公网安备51019002008863号
川公网安备51019002008863号 本网站未发布麻醉药品、精神药品、医疗用毒性药品、放射性药品、戒毒药品和医疗机构制剂的产品信息
本网站未发布麻醉药品、精神药品、医疗用毒性药品、放射性药品、戒毒药品和医疗机构制剂的产品信息
收藏
登录后参与评论
暂无评论