肝癌作为全球高发恶性肿瘤,药物研发与市场格局持续迭代。摩熵咨询最新发布的《肝癌药物市场研究专题报告》全景式展现了肝癌药物竞争格局、核心品种表现及未来趋势,结合全球研发管线、医保政策、临床试验数据等多维度分析,是洞悉肝癌药物市场全貌的重要指南。
本文基于该报告部分核心内容,通过深度解析肝癌药物市场的变革逻辑与增长机遇,为读者呈现一个清晰详尽的市场图景,助力各界把握市场脉搏,抢占发展先机。
一、肝癌药物市场竞争格局分析
(一)肝癌靶向药物:从“老药独大”到“仿创混战”,竞争激烈
据摩熵医药数据库统计,截止2024年12月,全球已获批上市的肝癌小分子靶向药包括索拉非尼与瑞戈非尼(拜耳)、卡博替尼(Exelixis)、阿帕替尼(恒瑞医药)、雷莫芦单抗(礼来)、仑伐替尼(卫材)、多纳非尼(泽璟生物)。
上期内容我们剖析了索拉非尼、瑞戈非尼、阿帕替尼等肝癌小分子靶向药的市场表现及竞争态势。随着专利到期,仿制药对索拉非尼和瑞戈非尼原研药的市场份额冲击明显,销售额大幅下降。下面,我们将继续对仑伐替尼、多纳非尼等药物进行详细市场分析。
1. 仑伐替尼:全球第二款肝癌一线疗法,销售额峰值曾达28亿元
仑伐替尼(lenvatinib)是一种口服多种激酶抑制剂,可以选择性抑制多种激酶的活性,包括血管内皮生长因子受体(VEGFR1、VEGFR2和VEGFR3),以及成纤维细胞生长因子受体(FGFR1、FGFR2、FGFR3和FGFR4),此外还有致病性血管生成、肿瘤生长和癌症进展相关受体酪氨酸激酶,如血小板衍生生长因子受体α(PDGFRα)、KIT和RET。
仑伐替尼由卫材药业研发,2018年获FDA批准用于晚期HCC系统治疗,是继索拉非尼之后十多年来首次获批用于晚期HCC一线治疗的新药,同年也在中国获批上市。
仑伐替尼肝细胞癌全球研发进度查询(部分)
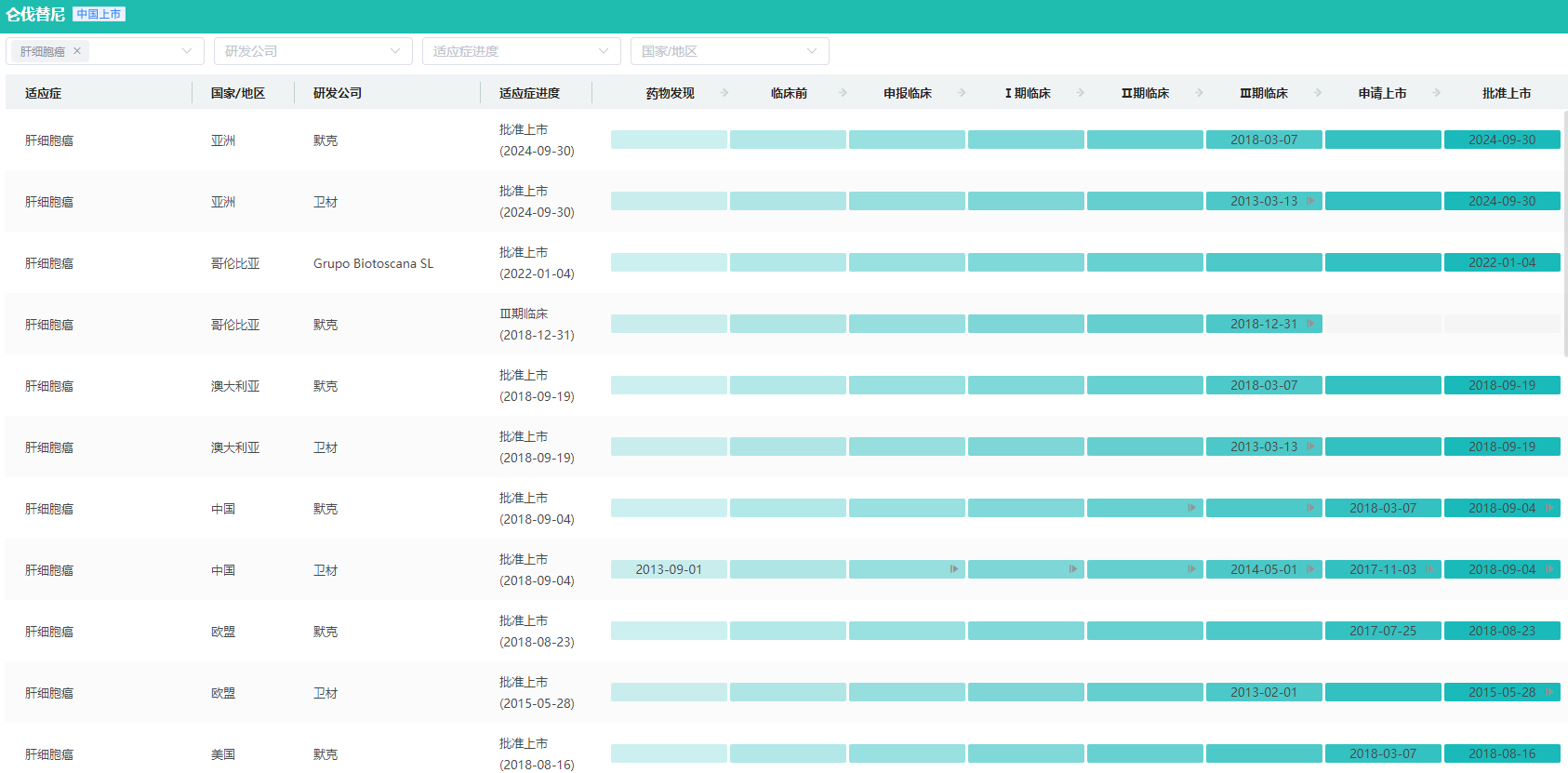
图片来源:摩熵医药全球药物研发数据库
仑伐替尼作为单药,已经在日本、美国、欧洲、中国等国家和地区获批用于一线治疗甲状腺癌和肝细胞癌,在日本也被批准用于治疗胸腺癌。仑伐替尼与依维莫司联合疗法已经在美国、欧洲和亚洲等地被批准用于二线治疗肾细胞癌;与抗PD-1单抗帕博利珠单抗组成的联合疗法已经在多地获批用于一线治疗肾细胞癌、既往经过全身治疗的子宫内膜癌等。
摩熵医药数据库显示,仑伐替尼在2020年首次纳入医保,2021年放量明显,全年销售额达16.56亿元,并在2022年达到销售额峰值近28亿元,2023年和2024上半年由于竞争加剧,销售额有下降趋势。
























































 川公网安备51019002008863号
川公网安备51019002008863号 本网站未发布麻醉药品、精神药品、医疗用毒性药品、放射性药品、戒毒药品和医疗机构制剂的产品信息
本网站未发布麻醉药品、精神药品、医疗用毒性药品、放射性药品、戒毒药品和医疗机构制剂的产品信息
收藏
登录后参与评论
暂无评论