1.5.1 本周全球TOP10创新药研发进展
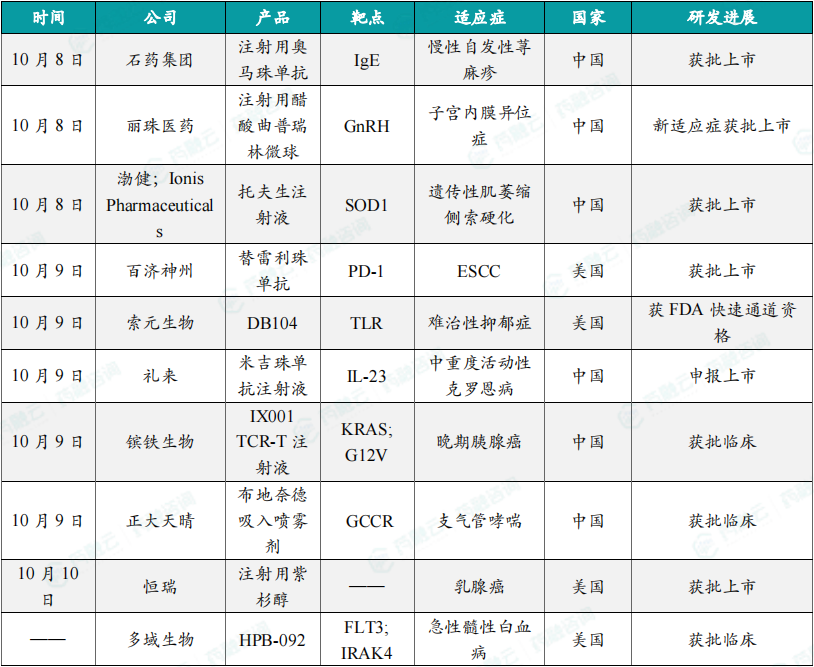
(1)石药集团注射用奥马珠单抗生物类似药获批上市
10月8日,石药集团以注册分类3.3类申报的注射用奥马珠单抗生物类似药上市申请已获得上市批准。根据石药集团早先新闻稿,该产品是人免疫球蛋白E(IgE)人源化单克隆抗体,适用于H1抗组胺药治疗后仍有症状的成人和青少年(12岁及以上)慢性自发性荨麻疹患者。作为一款IgE人源化单克隆抗体,奥马珠单抗可通过降低游离IgE水平、下调高亲和力IgE受体和限制肥大细胞的脱颗粒化,减少过敏性炎症级联反应中多种介导因子的释放;它还能降低IgE介导的哮喘患者的哮喘加重率。奥马珠单抗原研产品已在中国获批用于治疗过敏性哮喘、慢性自发性荨麻疹等适应症。
(2)丽珠医药注射用醋酸曲普瑞林微球新适应症获批上市
10月8日,丽珠医药注射用醋酸曲普瑞林微球的新适应症上市申请已获得批准。根据丽珠医药此前公开资料,该产品是每月一次肌肉注射的一种促性腺激素释放激素(GnRH)激动剂,本次获批的适应症为治疗子宫内膜异位症。公开资料显示,针对GnRH靶点开发的治疗内异症药物有注射用GnRH激动剂及口服GnRH拮抗剂。GnRH激动剂为注射剂,可显著降低血雌激素水平,强效减轻内异症相关疼痛症状,一定程度缩小内异症病灶,曾被《子宫膜异位症长期管理中国专家共识》认为是内异症药物治疗的“金标准”,至今仍被认为是内异症药物治疗最有效的方法之一。
(3)渤健和Ionis Pharmaceuticals联合开发的托夫生注射液获批上市
10月8日,渤健公司5.1类新药托夫生注射液的上市申请已获得批准。公开资料显示,该药是渤健和Ionis Pharmaceuticals联合开发的一款反义寡核苷酸(ASO)疗法,已经获美国FDA批准治疗遗传性肌萎缩侧索硬化(ALS)。该药还入选了今年8月公布的2024年度盖伦奖(Prix Galien USA Awards)“最佳罕见病产品奖”的候选名单。托夫生注射液(tofersen)是一种反义寡核苷酸药物,正在开发用于治疗SOD1-ALS。该药可以与编码SOD1的mRNA结合,造成其被核糖核酸酶RNase-H降解,进而减少突变的SOD1蛋白生成。
(4)百济神州替雷利珠单抗在美国获批上市
10月9日,百济神州宣布TEVIMBRA®(替雷利珠单抗,中文商品名:百泽安®)在美国正式商业化上市,用于治疗既往接受过系统化疗(不含PD-1/L1抑制剂)后不可切除或转移性食管鳞状细胞癌(ESCC)的成人患者。替雷利珠单抗在今年早前已获得美国FDA批准。该批准基于RATIONALE 302试验结果,该试验在意向性治疗(ITT)人群中达到了主要终点。据百济神州新闻稿介绍,FDA目前还在对TEVIMBRA®用于局部晚期不可切除或转移性ESCC患者的一线治疗,以及用于局部晚期不可切除或转移性胃或胃食管结合部(G/GEJ)腺癌患者的一线治疗进行审评。
(5)索元生物创新药DB104(liafensine)获FDA快速通道资格
10月9日,索元生物宣布其潜在“first-in-class”创新药DB104(liafensine)用于难治性抑郁症(TRD)获美国FDA授予快速通道资格。快速通道资格是FDA专门授予用于治疗严重疾病和解决未满足医疗需求的新药的资格认定,获得该资格的新药有望获得政策支持,加快获批上市。Liafensine是一款潜在“first-in-class”三重再摄取抑制剂,可同时抑制在抑郁症中起重要作用的5-羟色胺、去甲肾上腺素和多巴胺的再摄取。索元生物利用其特有的DGM™生物标志物大数据/AI发现平台,发现了可以预测DB104疗效的全新生物标志物DGM4,并用于指导ENLIGHTEN研究国际多中心临床试验。
(6)礼来突破性抗体新药米吉珠单抗注射液在中国申报上市
10月9日,礼来公司(Eli Lilly and Company)申报的米吉珠单抗注射液以及其皮下注射剂型上市申请获得受理。公开资料显示,这应该是礼来研发的IL-23抑制剂mirikizumab。该产品此前曾被中国NMPA纳入突破性治疗品种,拟开发用于治疗中重度活动性克罗恩病成人患者。其针对克罗恩病的适应症尚未在全球范围内获得监管机构批准。Mirikizumab是一款人源化IgG4单克隆抗体,可与IL-23的p19亚基结合,阻断IL-23介导的炎症反应。作为一种炎性细胞因子,IL-23参与了多个炎症相关的生理过程,被认为与许多免疫介导的慢性疾病有关,也因此成为了许多自身免疫性疾病的治疗靶点。
(7)镔铁生物TCR-T细胞疗法IX001 TCR-T注射液获批临床
10月9日,CDE官网公示镔铁生物1类新药IX001 TCR-T注射液获批临床试验默示许可,拟开发适应症为基因型为HLA-A*11:01,肿瘤抗原KRAS G12V表达为阳性的晚期胰腺癌。胰腺癌因为致死率高且难以治疗,被称为“癌症之王”。根据镔铁生物公开资料,这是该公司首个申报注册临床试验的在研产品,是一款针对KRAS G12V突变TCR-T细胞疗法。在KRAS G12C抑制剂诞生之后,科学家们也将目标和兴趣转向其它KRAS突变体。研究发现,KRAS G12V是胰腺癌中最常见的突变类型,这为科学家攻破”癌症之王“提供了突破口。
(8)正大天晴布地奈德吸入喷雾剂获批临床
10月9日,正大天晴以注册分类2.2类改良型新药申报的布地奈德吸入喷雾剂获批临床,适用于需使用糖皮质激素维持治疗以控制基础炎症的支气管哮喘患者。公开资料显示,布地奈德是一种糖皮质激素,它的多种配方类型已经被用于治疗哮喘、慢性阻塞性肺病、过敏性鼻炎和鼻息肉等炎症性疾病。从作用机制来看,糖皮质激素通过多种途径发挥抗炎作用,从作用机制来看,它不仅作用于炎症细胞,而且可以抑制腺体分泌,减少炎症渗出,减少痰液产生,针对哮喘和慢阻肺患者有着突出效果。
(9)恒瑞医药白蛋白紫杉醇仿制药在美国获批上市
10月10日,恒瑞医药发布公告称该公司注射用紫杉醇(白蛋白结合型)ANDA(简略新药申请,即美国仿制药申请)已获得FDA批准,是首家在美国获得该品种仿制药批准的厂家。恒瑞医药公告介绍,该公司研发的注射用紫杉醇(白蛋白结合型)已于2018年在中国获批上市,用于治疗联合化疗失败的转移性乳腺癌或辅助化疗后6个月内复发的乳腺癌;2024年获批第2个适应症,用于联合吉西他滨作为转移性胰腺癌的一线治疗。本次注射用紫杉醇(白蛋白结合型)获得美国FDA批准文号,标志着公司具备了在美国市场销售该药品的资格。
(10)多域生物FLT3/IRAK4双靶点抑制剂HPB-092在美国获批临床
近日,杭州多域生物技术有限公司(简称多域生物,Polymed Biopharma)宣布其FLT3/IRAK4双靶点抑制剂HPB-092的临床研究申请获美国FDA批准,即将开展用于治疗急性髓性白血病(AML)的1期临床研究。多域生物在新闻稿指出,在临床前研究中,其FLT3/IRAK4双靶点抑制剂HPB-092活性指标与安全性显著优于目前已获批的同靶点药物。HPB-092还具有IRAK4抑制活性,已有临床数据证明抑制IRAK4活性可以治疗RNA剪切体突变的AML和骨髓增生异常综合征(MDS,myelodysplastic syndrome)。因此,HPB-092有望扩大已获批的FLT3抑制剂的治疗人群,以及更持久的疗效和更好的安全性。
1.5.2本周全球TOP10积极/失败临床结果


(1)辉瑞公布小分子组合疗法的3期临床数据
10月11日,辉瑞(Pfizer)公布TALAPRO-2临床3期研究的预定顶线分析积极结果。分析显示,与活性对照药物相比,其多腺苷二磷酸核糖聚合酶(PARP)抑制剂Talzenna(talazoparib)与雄激素受体途径抑制剂(ARPI)Xtandi(恩扎卢胺,enzalutamide)组合疗法可在临床和统计学上显著改善转移性去势抵抗性前列腺癌(mCRPC)患者的总生存期(OS)。结果显示,与Xtandi单药相比,Talzenna与Xtandi组合疗法在所有患者(队列1)以及同源重组修复(HRR)基因突变的mCRPC患者(队列2)中的最终OS均有统计学和临床意义上的改善。Talzenna与Xtandi联合疗法于2023年6月获得美国FDA批准,用于治疗同源重组修复基因突变的mCRPC成年患者。该联合疗法也于今年1月获得欧盟委员会批准,用于治疗临床上不适合化疗的mCRPC成年患者。
(2)Immatics公布在研T细胞受体T细胞疗法IMA203的1b期临床数据
10月11日,Immatics公布其在研T细胞受体T细胞(TCR-T)疗法IMA203用以治疗转移性黑色素瘤患者的最新1b期临床数据。IMA203是由Immatics专有ACTengine平台所开发的TCR-T细胞疗法,靶向由HLA-A*02呈递的黑素瘤抗原PRAME。分析显示,在所有28名黑色素瘤患者中,IMA203的客观缓解率(ORR)达62%,确认ORR为54%,中位DOR为12.1个月,疾病控制率(DCR)达92%,88%的患者肿瘤缩小。患者的中位无进展生存期(PFS)为6.0个月,与之前公布的1a期剂量递增试验中的结果(中位PFS为2.6个月)相比更为有利,患者的中位OS尚未达到。值得一提的是,该1b期试验中大约一半的患者获得了深度缓解(肿瘤缩小50%以上)。
(3)Capricor Therapeutics公布细胞疗法deramiocel的2期临床数据
10月12日,Capricor Therapeutics公布细胞疗法deramiocel(CAP-1002)的HOPE-2开放标签扩展(OLE)试验的2期临床数据,HOPE-2试验对象为不能行动的晚期杜氏肌营养不良(DMD)病患。OLE试验的分析显示,接受其主打细胞疗法deramiocel治疗患者的心脏和骨骼肌功能在三年期间趋于稳定。在第12个月时,总共分析了20位病患的研究数据(含12位安慰剂组与8位试验组病患),其结果发表在《柳叶刀》期刊上。该试验达成其主要终点,即在测试上肢功能的指标PUL 1.2上,接受CAP-1002治疗的病患有显著疗效(2.6分差异,P=0.014)。
(4)Aurigene Oncology公布Ribrecabtagene autoleucel(DRL-1801)的1期临床数据
近日,Aurigene Oncology公司宣布其新型BCMA靶向自体CAR-T细胞疗法Ribrecabtagene autoleucel(DRL-1801)用于治疗复发/难治性多发性骨髓瘤的1期临床试验中首批8名患者的初步结果。所有患者都接受过大量的前期治疗,中位治疗线数为5.5线。大多数患者此前也曾接受过移植手术,并在移植后出现疾病进展。结果显示,100%的患者获得了临床缓解,其中有5名(62.5%)患者获得了严格的完全缓解(CR)。安全性方面,所有患者均未出现高级别的细胞因子释放综合征(CRS)或神经毒性。
(5)Diakonos Oncology公布树突状细胞疫苗DOC1021的1期临床中期数据
近日,Diakonos Oncology公司公布了其树突状细胞疫苗DOC1021用于治疗胶质母细胞瘤患者的1期开放标签试验的中期分析结果。此次公布的结果显示,15例患有挑战性肿瘤、MGMT未甲基化(通常预后不良)患者中有14例存活超过12个月。目前,中位随访时间为16个月,中位OS尚未达到。Kaplan-Meier(KM)分析将接受DOC1021治疗的患者与接受完整SOC的年龄匹配历史对照组患者进行比较,两组在统计学上具有差异(p=0.03)。KM预测接受DOC1021治疗的患者的OS为19.7个月,而接受SOC的未甲基化GBM患者的预期OS为12.7个月。安全性方面,没有剂量限制性毒性或令人担忧的严重不良事件(SAE)。
(6)Vincerx Pharma公布抗体偶联药物VIP943的1期临床结果
近日,Vincerx Pharma公司公布了其抗体偶联药物(ADC)VIP943治疗复发/难治性急性髓系白血病(AML)、高危骨髓增生异常综合征(HR-MDS)和B细胞急性淋巴细胞白血病(B-ALL)的1期临床试验的结果。该1期剂量递增研究共招募了22名患者,他们很少对单一疗法产生应答。9名患者(6名AML患者和3名HR-MDS患者)至少接受了3次有效剂量的VIP943治疗。截至目前,1名复发性AML患者获得了完全缓解伴血液学不完全恢复(CRi),1名HR-MDS患者获得了完全缓解伴较少血液学恢复(CRL)。截至2024年8月的数据,VIP943显示出良好的安全性和耐受性,没有报告剂量限制性毒性,SAE与预期一致。
(7)Viking Therapeutics公布TRβ小分子激动剂VK0214的1b期临床结果
近日,Viking Therapeutics公司公布了其新型甲状腺激素受体β(TRβ)小分子激动剂VK0214在X-连锁肾上腺白质营养不良(X-ALD)患者中进行的1b期临床试验的积极数据。临床前研究表明,甲状腺激素受体β型可以调节ABCD2相关基因的表达,ABCD2能够编码一种称为肾上腺脑白质营养不良相关蛋白(ADLRP)的代偿转运体,通过增加ABCD2表达可以使特定脂肪酸水平恢复正常。此次公布的研究结果表明,在为期28天的研究期间,VK0214每天用药一次的安全性和耐受性良好。此外,与安慰剂相比,接受VK0214治疗患者血浆中的超长链脂肪酸(VLCFAs)和其他血脂水平明显降低。
(8)Kazia Therapeutics公布paxalisib联用放射疗法的1期临床数据
近日,Kazia Therapeutics公司公布其口服PI3K/mTOR双抑制剂paxalisib联用放射疗法治疗PI3K通路突变实体瘤脑转移(BM)或软脑膜转移(LM)患者的1期临床试验的数据。此次公布的结果显示,paxalisib联用放疗总体耐受性良好。研究中最常报告的不良反应是恶心、呕吐和高血糖。接受45 mg paxalisib联用放疗患者中有67%获得了部分缓解(PR),接受最大耐受剂量治疗的患者中有超过三分之二的人获得了颅内缓解,这与单独使用全脑放疗的历史缓解率相比毫不逊色。
(9)Enliven Therapeutics公布小分子激酶抑制剂ELVN-001的1期临床数据
近日,Enliven Therapeutics公司公布其小分子激酶抑制剂ELVN-001治疗复发/难治性或对现有酪氨酸激酶抑制剂(TKI)不耐受的慢性髓系白血病(CML)患者的1期临床试验的积极数据。ELVN-001还具有针对耐药性最强的BCR-ABL1耐药突变体T315I和其他已知耐药突变体的活性。截至2024年6月25日的数据,ELVN-001的耐受性保持良好,没有患者减少剂量,未报告≥3级治疗相关的非血液学毒性反应。第24周时,患者的初始累积主要分子缓解(MMR)率为44%(8/18),与已获批的BCR-ABL1酪氨酸激酶抑制剂在1期临床试验中的数据相比具有优势。
(10)Repare Therapeutics公布camonsertib联合疗法的1期临床数据
近日,Repare Therapeutics公司公布了潜在”best-in-class”口服小分子ATR抑制剂camonsertib结合姑息性放疗,治疗携带ATM突变转移性肿瘤的1期临床试验数据。此次公布的结果显示,2个月时,致病性ATM突变组有2例CR、5例PR和4例疾病稳定(SD)患者,而VUS组有1例PR和4例SD患者。6个月时,在9名可评估患者中,致病性ATM突变组有2例CR、4例PR和1例SD患者,而VUS组有1例SD和1例疾病进展患者。该早期临床数据表明camonsertib联合放疗治疗有可能对携带致病性ATM突变的肿瘤患者进行放射增敏,从而获得更高的临床益处。
同期事件:
1. 2024年第41周10.07-10.13国内创新药/改良型新药申请临床/获批临床/申请上市/获批上市数据分析
2. 2024年第41周10.07-10.13国内仿制药/生物类似物申报/审批数据分析
3. 2024年第41周10.07-10.13国内医药大健康行业政策法规汇总
4. 2024年第41周10.07-10.13全球医药大健康行业投融资数据
以上内容均来自{摩熵咨询医药行业观察周报(2024.10.07-2024.10.13)},如需查看或下载完整版报告,可点击!
<END>
想要解锁更多药物研发信息吗?查询摩熵医药数据库(vip.pharnexcloud.com/?zmt-mhwz)掌握药物基本信息、市场竞争格局、销售情况与各维度分析、药企研发进展、临床试验情况、申报审批情况、各国上市情况、最新市场动态、市场规模与前景等,以及帮助企业抉择可否投入时提供数据参考!注册立享15天免费试用!



















































 浙公网安备33011002015279
浙公网安备33011002015279 本网站未发布麻醉药品、精神药品、医疗用毒性药品、放射性药品、戒毒药品和医疗机构制剂的产品信息
本网站未发布麻醉药品、精神药品、医疗用毒性药品、放射性药品、戒毒药品和医疗机构制剂的产品信息
收藏
登录后参与评论
暂无评论