-
 时讯直接投入的研发费用约为人民币1,722.34万元,丽珠医药拿下注射用丹曲林钠国内首仿,适应症为用于预防及治疗恶性高热。丽珠医药2024-03-14医药
时讯直接投入的研发费用约为人民币1,722.34万元,丽珠医药拿下注射用丹曲林钠国内首仿,适应症为用于预防及治疗恶性高热。丽珠医药2024-03-14医药 -
 医药洞见3月9日,仙琚制药公告,近日收到国家药品监督管理局核准签发的关于非那雄胺片的《药品补充申请批准通知书》,公司非那雄胺片通过仿制药质量和疗效一致性评价。新浪医药新闻2024-03-14医药
医药洞见3月9日,仙琚制药公告,近日收到国家药品监督管理局核准签发的关于非那雄胺片的《药品补充申请批准通知书》,公司非那雄胺片通过仿制药质量和疗效一致性评价。新浪医药新闻2024-03-14医药 -
 医药洞见3月18日,恩华药业公告,公司于近日收到国家药监局核准签发的关于“阿立哌唑片”的《药品补充申请批准通知书》,批准该药品通过仿制药质量和疗效一致性评价。新浪医药新闻2024-03-14医药
医药洞见3月18日,恩华药业公告,公司于近日收到国家药监局核准签发的关于“阿立哌唑片”的《药品补充申请批准通知书》,批准该药品通过仿制药质量和疗效一致性评价。新浪医药新闻2024-03-14医药 -
 医药洞见药融云数据查询显示:2021.03.12-2021.03.18期间药审中心受理总量为151个,涉及品种109个,14个1类新药申请临床获CDE受理, 新增9个按仿制药质量和疗效一致性评价品种申报的受理号,37个品种通过(含视同通过)一致性评价,1款1类新药获批上市:国内首款埃博霉素类新药获批。摩熵医药(原药融云)2024-03-14医药
医药洞见药融云数据查询显示:2021.03.12-2021.03.18期间药审中心受理总量为151个,涉及品种109个,14个1类新药申请临床获CDE受理, 新增9个按仿制药质量和疗效一致性评价品种申报的受理号,37个品种通过(含视同通过)一致性评价,1款1类新药获批上市:国内首款埃博霉素类新药获批。摩熵医药(原药融云)2024-03-14医药 -
 医药洞见
医药洞见 -
 医药洞见
医药洞见 -
 深度分析2021年4月1日-4月11日,CDE新公示临床试验共计74项。从药品类型来看,化学药物共计54项,生物制品18项,中药/天然药物2项。摩熵医药(原药融云)2024-03-14临床试验
深度分析2021年4月1日-4月11日,CDE新公示临床试验共计74项。从药品类型来看,化学药物共计54项,生物制品18项,中药/天然药物2项。摩熵医药(原药融云)2024-03-14临床试验 -
 时讯4月13日,国家药监局发布公告称,桂附地黄颗粒由处方药转化为非处方药。相关药品上市许可持有人在2021年7月6日前,依据《药品注册管理办法》等有关规定提出修订药品说明书的补充申请报省级药品监督管理部门备案,并将说明书修订的内容及时通知相关医疗机构、药品经营企业等单位。国家药品监督管理局2024-03-14国家药监局
时讯4月13日,国家药监局发布公告称,桂附地黄颗粒由处方药转化为非处方药。相关药品上市许可持有人在2021年7月6日前,依据《药品注册管理办法》等有关规定提出修订药品说明书的补充申请报省级药品监督管理部门备案,并将说明书修订的内容及时通知相关医疗机构、药品经营企业等单位。国家药品监督管理局2024-03-14国家药监局 -
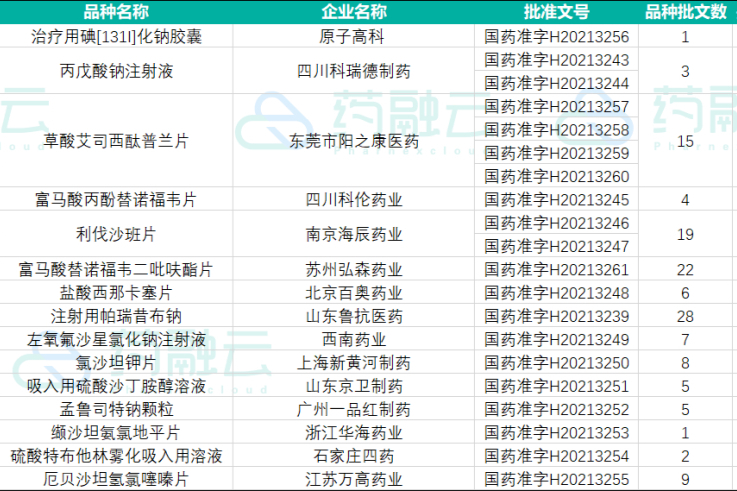 时讯2021年04月12日,国家药监局发布36个药品批准证明文件待领取信息,其中20个视同通过一致性评价,包含1个首家过评品种。摩熵医药(原药融云)2024-03-14一致性评价
时讯2021年04月12日,国家药监局发布36个药品批准证明文件待领取信息,其中20个视同通过一致性评价,包含1个首家过评品种。摩熵医药(原药融云)2024-03-14一致性评价 -
 时讯2021年04月13日,国家药监局发布10个药品批准证明文件待领取信息,其中3个通过一致性评价,包含1个首家过评品种。摩熵医药(原药融云)2024-03-14一致性评价
时讯2021年04月13日,国家药监局发布10个药品批准证明文件待领取信息,其中3个通过一致性评价,包含1个首家过评品种。摩熵医药(原药融云)2024-03-14一致性评价
添加收藏


































 浙公网安备33011002015279
浙公网安备33011002015279 本网站未发布麻醉药品、精神药品、医疗用毒性药品、放射性药品、戒毒药品和医疗机构制剂的产品信息
本网站未发布麻醉药品、精神药品、医疗用毒性药品、放射性药品、戒毒药品和医疗机构制剂的产品信息