

18983288589(微信同号)

18983288589(微信同号)

18908392210(微信同号)

18980413049


2024-05-29
赣药监规〔2024〕5号
其他
江西省
现行有效
2024-05-29
江西省药品监督管理局
江西省药品批发(零售连锁)企业量化分级
监督管理办法(试行)
第一条 为加强药品批发(零售连锁)企业(以下简称“企业”)质量安全和风险意识,督促企业落实主体责任,合理配置监管资源,提升监管效能,根据《中华人民共和国药品管理法》及其实施条例、《药品经营和使用质量监督管理办法》及《药品经营质量管理规范》等规定,结合我省实际,制定本办法。
第二条 本办法中的量化分级监督管理,是指省药品监督管理局(以下简称“省局”)根据企业责任意识、监管情况、社会影响等因素,依据本办法对企业质量安全风险等级评定,并根据评定结果确定监管频次和方式的管理办法。
第三条 本办法适用于对江西省行政区域内依法持有《药品经营许可证》的药品批发(零售连锁)企业质量安全风险量化分级监管。
第四条 企业量化分级管理应当遵循客观公正、科学规范、量化评价、动态管理的原则。
第五条 省局负责制定企业质量安全风险分级指标,组织全省企业量化分级管理工作。省局有关处室、各直属单位根据监管职责,及时归集企业质量安全风险量化分级管理相关基础数据,于每年12月20日前汇总至省局药品经营处。
第六条 省药品检查员中心、樟树药监局负责督促企业按时提交真实、完整的质量安全风险量化分级自评信息,承担企业自评信息核对工作。
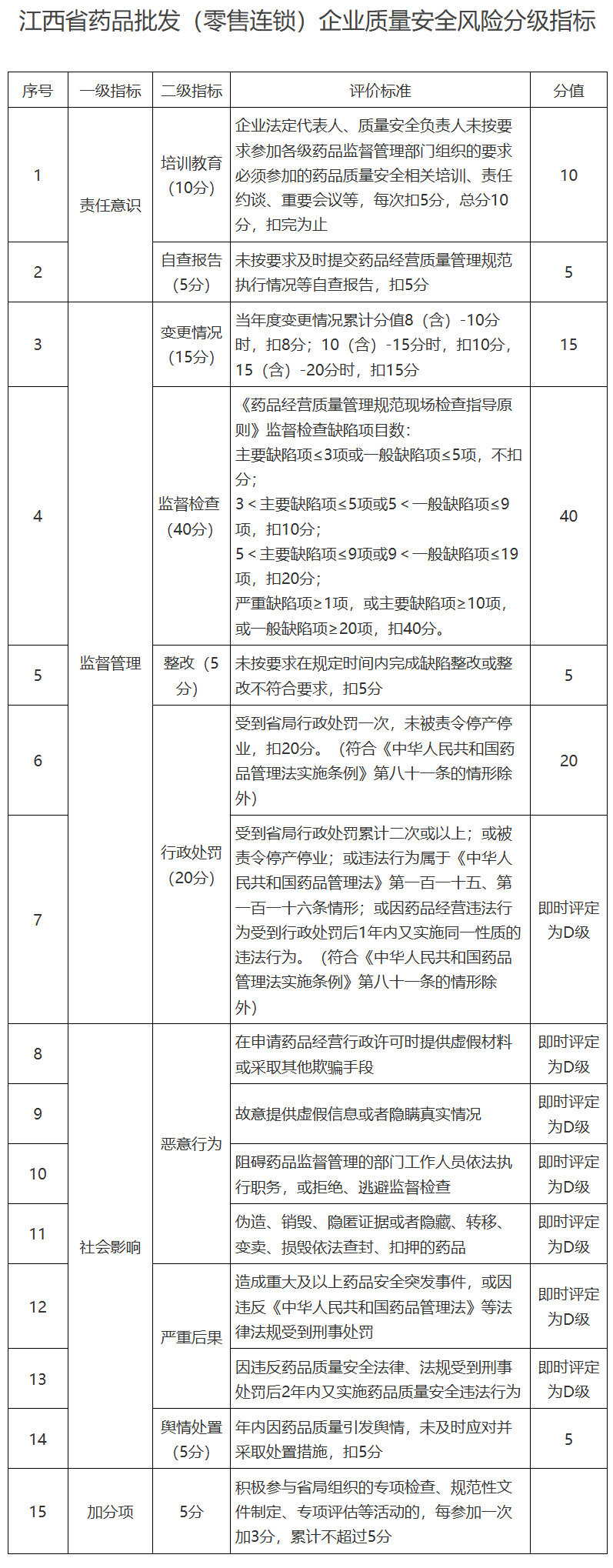
第七条 省局结合企业主体责任落实情况、监管情况等对企业开展质量安全风险等级划分,制定《江西省药品批发(零售连锁)企业质量安全风险分级指标》(附件1),设置责任意识、监管情况、社会影响等三个一级指标,一级指标下设若干二级指标,根据监管实际可以适时调整。
第八条 企业质量安全风险分级总分为100分,设置四个等级,分值越低,认为企业药品质量安全风险越高:
(一)A级(风险低):85分(含)及以上;
(二)B级(风险一般):75分(含)至85分;
(三)C级(风险较高):60分(含)至75分;
(四)D级(风险高):60分以下。
新开办企业初始监管级别为C级。
符合《江西省药品批发(零售连锁)企业质量安全风险分级指标》中行政处罚、恶意行为、严重后果等规定情形的,应当即时评定为D级。
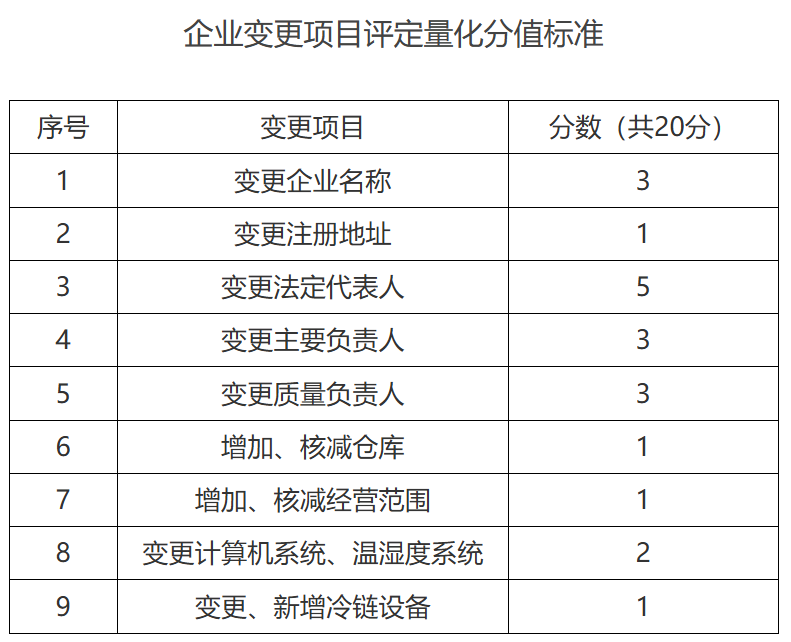
第九条 企业频繁变更项目,视为存在质量风险。变更情况按变更频次和项目量化分值,累计评分(变更项分值详见附件2)。企业一个计分周期内变更多个项目、多次变更同一项目的,需累计分值。
第十条 企业质量安全风险量化分级每年评定一次,以本年度12月31日起往前追溯一年为一个评定年度,在评定年度6月30日后取得药品经营许可证的企业,不参加当年评定,在次期间的评定信息计入下一评定年度。
企业量化分级评定分为自评、信息核对、初评、结果告知和异议申请、异议处理和终评五个阶段。
(一)自评。企业应当于每年1月1日至1月15日期间提交上一评定年度的自评信息并附真实性承诺。
(二)信息核对。省药品检查员中心、樟树药监局于每年1月31日前完成企业自评信息核对。
(三)初评。省局于每年2月15日前形成初评分级结果。
(四)结果告知和异议申请。省药品检查员中心、樟树药监局应于每年2月20日前将初评分级结果告知企业,企业对分级结果有异议的,应当在收到告知结果的7个工作日内向省局提出异议申请,并提供相应说明及证据材料。
(五)异议处理和终评。省局应当在收到企业异议申请后的7个工作日内组织复核,并作出维持或调整分级结果的终评结论。
被即时评定为D级的,省药品检查员中心、樟树药监局应当在评定后5个工作日内将分级结果告知企业,有关异议申请、处理等按照前款规定办理。
第十一条 企业量化分级所依据的行政处罚或者其他行政处理决定被撤销、确认违法或者无效,可能影响到分级结果的,企业可以向省局提出申请,省局应当依据本办法予以相应调整。
第十二条 除投诉举报、专项检查、案件线索转办交办外,省局有关处室、直属单位应当根据企业量化等级结果合理确定、动态调整监督检查频次和方式,实施差异化分级监管:
(一)对A级企业实行适度宽松的监管,主要采取企业自查的模式进行监管,本年度可不安排监督检查;
(二)对B级企业实行一般监管,主要采取常规检查的模式进行监管,本年度安排监督检查0-1次;
(三)对C级企业实行重点监管,主要采取常规检查或飞行检查的模式进行监管,本年度安排监督检查1-2次;
(四)对D级监管企业实行严格监管,主要采取飞行检查的模式进行监管,本年度安排监督检查2-3次。
省局有关处室、直属单位可结合本区域内工作实际,适当增加检查频次。
第十三条 对具有麻醉药品和第一类精神药品、药品类易制毒化学品、冷藏冷冻药品、血液制品、细胞治疗类生物制品、第二类精神药品、医疗用毒性药品经营范围的药品经营企业,应不少于《药品经营和使用质量监督管理办法》第六十条第一款、第二款规定的检查频次,对其他企业实行三年内全覆盖检查。
第十四条 本办法自发布之日起施行。
附件:1.江西省药品批发(零售连锁)企业质量安全风险分级指标
2.企业变更项目评定量化分值标准
附件1
附件2

摩熵医药2025-01-08

摩熵医药2024-12-17
Pharma CMC2024-10-15
摩熵医药(原药融云)2024-08-21
数屿医械2024-06-24
数屿医械2024-06-13
数屿医械2024-05-30
摩熵医药(原药融云)2024-05-27
药事纵横2024-02-28
药通社2023-12-26
2025-01-14
2025-01-09
2025-01-09
2025-01-09
2025-01-09
2025-01-09
2025-01-09
2025-01-08
2025-01-08
2025-01-08
2025-01-08
2025-01-08
2025-01-07
2025-01-07
2025-01-06
2024-06-27
2024-05-29
2024-05-29
2024-04-25
2024-04-12
2024-02-26
2024-01-26
2023-10-20
2023-09-20
2023-02-06
2022-11-18
2022-10-14
2025-01-08
2024-12-16
2024-10-22
2024-07-30
2024-07-29
2024-06-27
2024-05-30
2024-05-30
2024-05-29
2024-05-29
2024-05-10
2024-04-29
2024-04-25
2024-04-12
2024-04-12