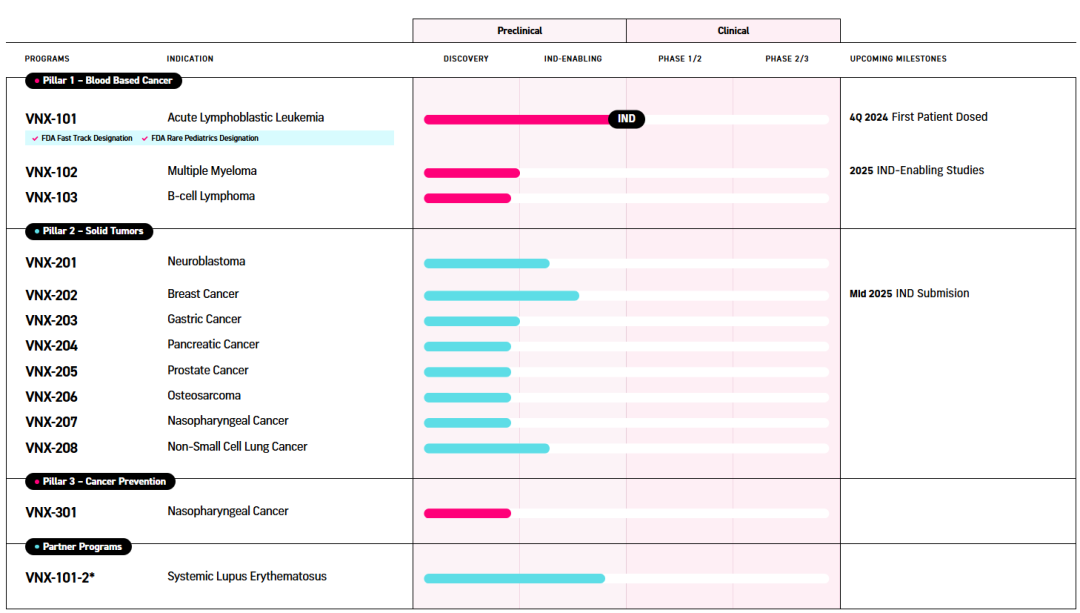
9月12日,加利福尼亚州圣地亚哥,Vironexis Biotherapeutics专注于通过开创AAV递送的T细胞免疫疗法来改变癌症治疗的未来,宣布完成2600万美元种子轮融资,推出了其TransJoin™AAV基因治疗平台和一系列用于血液瘤、实体瘤转移预防和癌症疫苗的十多种候选产品。种子融资由Drive Capital和Future Ventures领投,Moonshots Capital和Capital Factory跟投。该公司已获得美国FDA对其首个用于治疗CD19+急性淋巴细胞白血病的候选基因治疗产品VNX-101的研究性新药(IND)申请的批准。Vironexis预计将于2024年第四季度启动VNX-101的1/2期试验的患者登记,这将标志着AAV递送的癌症免疫疗法的首次临床试验。VNX-101已获得美国FDA的快速通道认证和罕见儿科疾病认证。
Vironexis联合创始人兼首席执行官Samit Varma表示:“我们很高兴能够秘密推出Vironexi,并展示我们在推进AAV递送的T细胞免疫疗法方面取得的显著进展。我们的新技术建立在T细胞免疫疗法的基础上,同时克服了现有方法(如CAR-T和双特异性抗体)的关键缺点和挑战。我们相信,我们有机会大幅提高这些药物类别的安全性、有效性和耐用性,同时简化生产,显著减轻患者的治疗负担。我们对执行的关注在短短三年内就产生了一个庞大的管线和一个临床准备的领导计划。我们正在尽快改变癌症患者治疗的未来。”TransJoin使患者的身体能够表达一种工程转基因,将全身的T细胞重定向到肿瘤细胞。这项专有技术只需要一剂,并提供了一个连接T细胞和肿瘤细胞的桥梁,以促进长期、连续的T细胞介导的肿瘤杀伤。TransJoin的基础技术获得了美国国家儿童医院的许可。2022年,由儿科血液学/肿瘤学/骨和骨髓移植科主任Timothy Cripe博士领导的研究在《科学进展》上发表,描述了TransJoin技术。Cripe博士是Vironexis的联合创始人之一,Varma先生是一位经验丰富的生物技术和基因治疗公司企业家,Brian Kaspar博士是一位著名的基因治疗科学家创立的AveXis被诺华收购。Cripe博士表示:“AAV是一种经过验证的递送技术,自2017年以来已获得多项批准。认识到AAV递送对治疗罕见疾病的关键影响,我们认为其能够长期、连续表达治疗性蛋白的独特能力可能是克服与CAR-T等第一代T细胞免疫疗法相关的无数挑战的缺失环节。我们随后在临床前环境中证明了这种方法的潜力。现在看到这项技术如何在临床环境中转化,真是令人兴奋。我们的最终目标是帮助更广泛的患者群体实现T细胞免疫疗法的巨大益处。”Vironexis正在从FDA获得其第二个项目VNX-202的IND前准备,作为预防转移性HER2+癌症(包括癌症和其他肿瘤类型)的治疗方法,并计划在2025年开始在1/2期临床试验中给患者用药。该公司目前的其他候选产品包括治疗BCMA/GPRC5D+多发性骨髓瘤、CD19/20+B细胞淋巴瘤;预防GD2+神经母细胞瘤、HER2+癌症胃癌、PSMA+和MSLN+癌症、B7H3+骨肉瘤和GP350+转移癌症的治疗;针对GP350+鼻咽癌的癌症疫苗;以及针对CD19+系统性红斑狼疮的治疗,Vironexis计划与之合作进一步开发。
Drive Capital合伙人Molly Bonakdarpour表示:“作为一项投资组合,Vironexis提供了突破性技术、令人印象深刻的临床前数据、巨大的患者影响潜力,以及一个拥有深厚相关专业知识和公司组建、战略思维和成功执行的良好记录的创始团队的理想组合。Vironexis在很短的时间内取得了显著的生产力。我们期待着它即将过渡到临床阶段的公司。”Future Ventures联合创始人Steve Jurvetson表示:“我们不仅被TransJoin技术的新颖性所吸引,还被其广泛的适用性所吸引。它涵盖了血液瘤的治疗、实体瘤转移预防、癌症疫苗以及免疫障碍。这个平台的多功能性确实非常突出,Vironexis团队在快速构建探索这些机会的管线方面取得了非凡的进展。”关注下方公众号,带你看世界!

<END>
*版权声明:本网站所转载的文章,均来自互联网,旨在传递更多信息。鉴于互联网的开放性和文章创作的复杂性,我们无法保证所转载的所有文章均已获得原作者的明确授权。如果您是原作者或拥有相关权益,请与我们联系,我们将立即删除未经授权的文章。本网站转载文章仅为方便读者查阅和了解相关信息,并不代表我们认同其观点和内容。读者应自行判断和鉴别转载文章的真实性、合法性和有效性。

















收藏
登录后参与评论