
近日,百时美施贵宝(BMS)首席医疗官Samit Hirawat表示,在今年6月因同位素短缺而被迫暂停试验后,该公司已恢复其主要放射性药物RYZ101 3期试验的招募工作,但目前已将3期试验的结果读出从2025年推迟到2026年。

BMS以41亿美元杀入核药领域
2023年12月26日,BMS宣布将以62.50美元/股的现金价格收购三年即上市的核药超新星RayzeBio,总股本价值约41亿美元,BMS将获得RayzeBio基于α核素的差异化放射性药物技术平台和多款在研创新产品,包括RYZ101、RYZ801等创新靶向核药,自此BMS正式进入核药赛道。
仅仅3年时间RayzeBio已布局了多条核药管线,其主要管线RYZ101已进入三期临床,于去年5月底开始首例患者给药,用于治疗胃肠胰神经内分泌肿瘤。同时,RYZ101也在进行一项针对表达SSTR的晚期小细胞肺癌患者的1期临床试验研究。
RYZ101是一款靶向放射性治疗药物,可以向过表达生长抑素受体(SSTR)的肿瘤递送强效α粒子放射性同位素锕-225。RYZ101以诺华的Lutathera®作对标,Lutathera为β核素Lu-177,RYZ101核素为杀伤力更强、射程更短的α核素Ac-225。FDA尚未批准基于锕的放射性药物,如果RYZ101的Ⅲ期临床能获得成功,将有望成为第一个获批的锕-225放射性药物疗法。
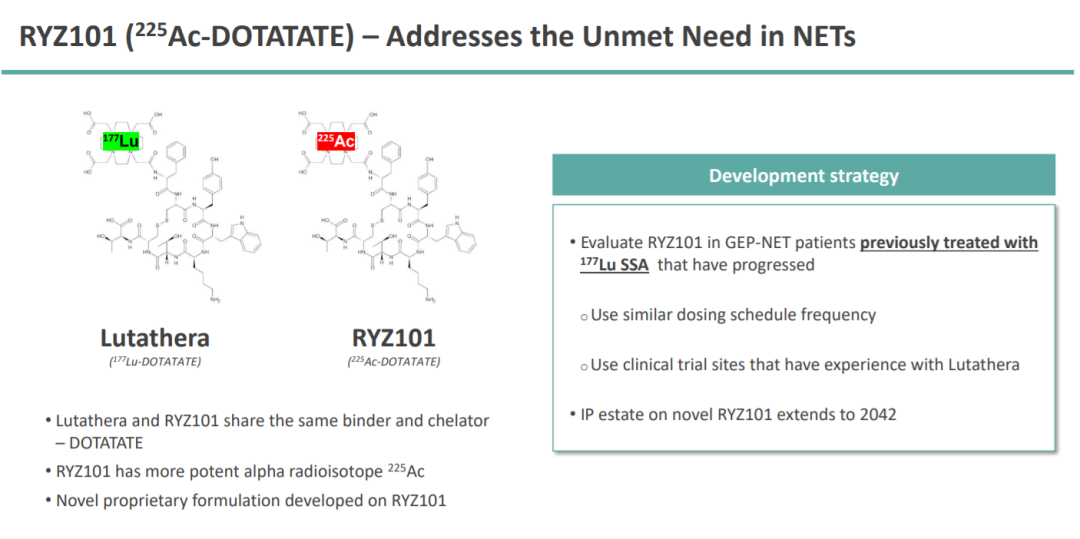
图源:公司官网
RayzeBio招股说明书披露公司最直接的竞争对手,主要是基于α放射同位素的药物开发类公司,如:Bayer、Novartis、Actinium、Fusion Pharmaceuticals、POINT Biopharma等。它们的α放射性同位素集中在Ra-223、Pb-212和 Ac-225。
同位素短缺,3期试验被迫暂停
今年6月,BMS表示暂停了核药RYZ101的3期试验的新患者招募,原因是同位素供应短缺问题。当时,百时美施贵宝表示计划在第三季度恢复新患者入组。该研究包括美国、巴西、比利时、加拿大、法国、荷兰和西班牙。
这是一项3期全球、随机、对照、开放标签试验,预计纳入288个患者,比较RYZ101治疗和标准治疗方法(SOC)用于既往接受过177Lu-SSA治疗后病情进展、无法手术、晚期、SSTR+、分化良好的胃肠胰神经内分泌肿瘤(GEP-NET)受试者。
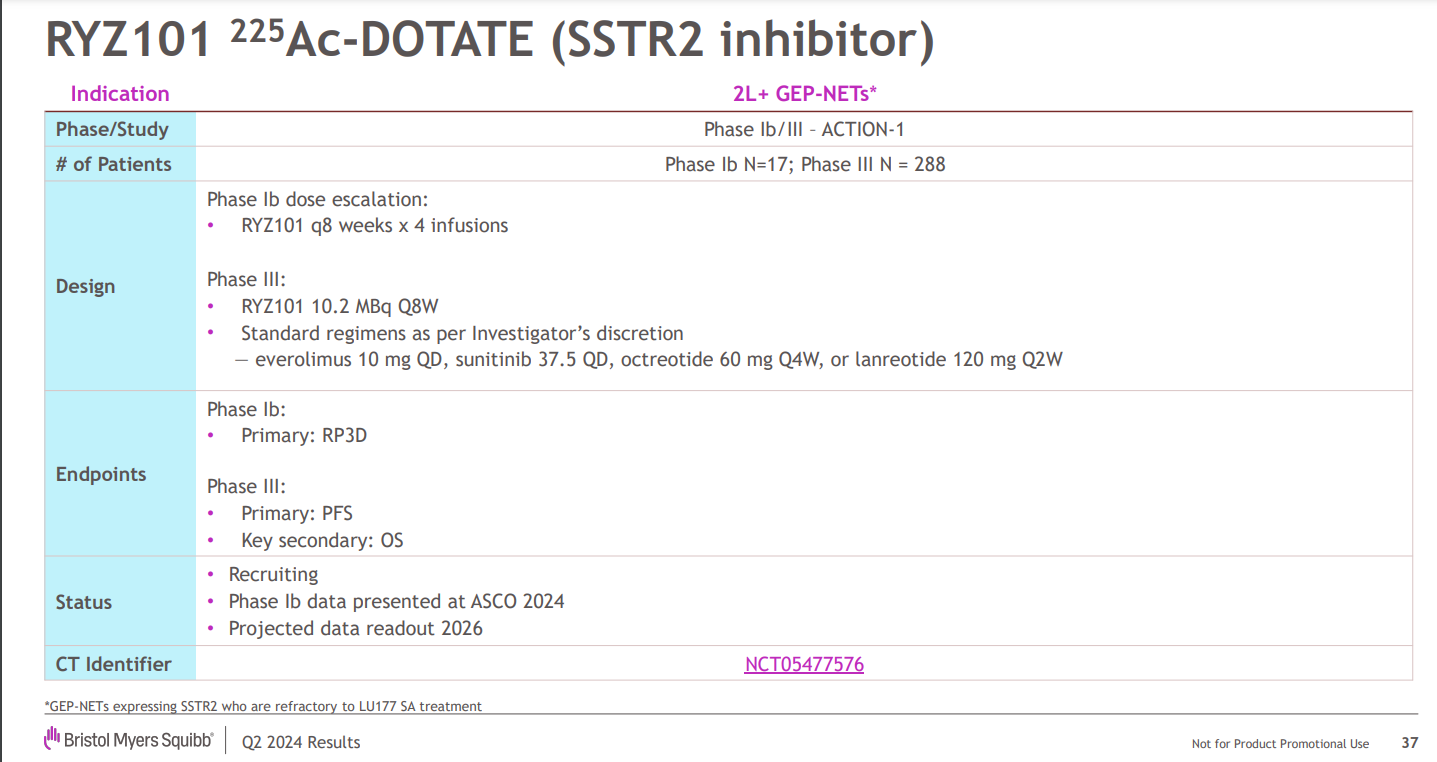
图源:2024 Q2财报
在同位素短缺期间,针对小细胞肺癌患者进行的RYZ101 1b期试验仍在继续招募,预计将在2025年获得剂量探索数据。
Ac-225是一种非常稀有的同位素,由于临床试验供应不足,此类放射性药物进入市场可能会遇到瓶颈。目前公司正在迅速推进 Ac225的现场生产,并预计能够在2025年第一季度通过内部生产来补充持续的临床供应。BMS表示该公司正在印第安纳州建立一个GMP制造工厂,这可能有助于支撑未来锕225同位素的供应,但目前仍依赖第三方。
这不仅是BMS独自的困境,而是核药行业的共同困境。同位素供应短缺是核药行业面临的最大挑战之一。连全球核药龙头诺华也曾遭遇过此问题,去年上半年诺华RDC产品Pluvicto的商业供应告急,需求超出预期,导致美国多家医疗机构的患者剂量供应被推迟。同位素的稳定供应是行业发展的基础。事实上全球范围内仅有少数几个国家具备医用同位素生产能力,且产能有限,在未来保证放射性同位素原料按合理价格稳定供应成为新进入者的重大挑战。
财务状况
7月26日,BMS公布2024年H1业绩,上半年总营收240.66亿美,同比增长7%;该公司销售成本为61.99亿美元,同比增长14%;研发投入55.94亿美元,同比增长22%。其中Q2营收为122.01亿美元,同比增长9%。由于其投资组合的整体表现出色,财报发出后其股价上涨了9%。
截至2024年6月30日,公司账上现金及等价物62.93亿美元。
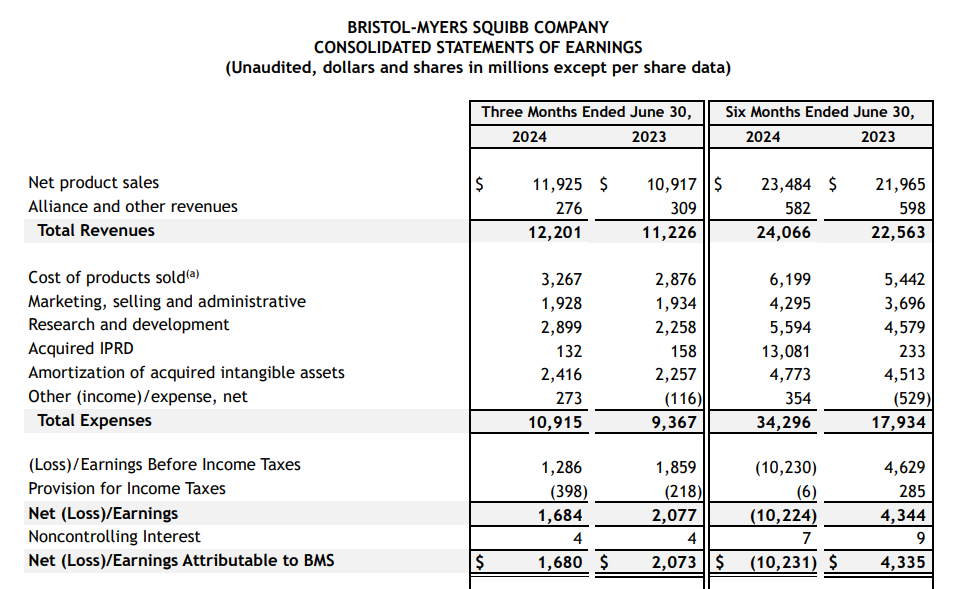
图源:2024 Q2财报
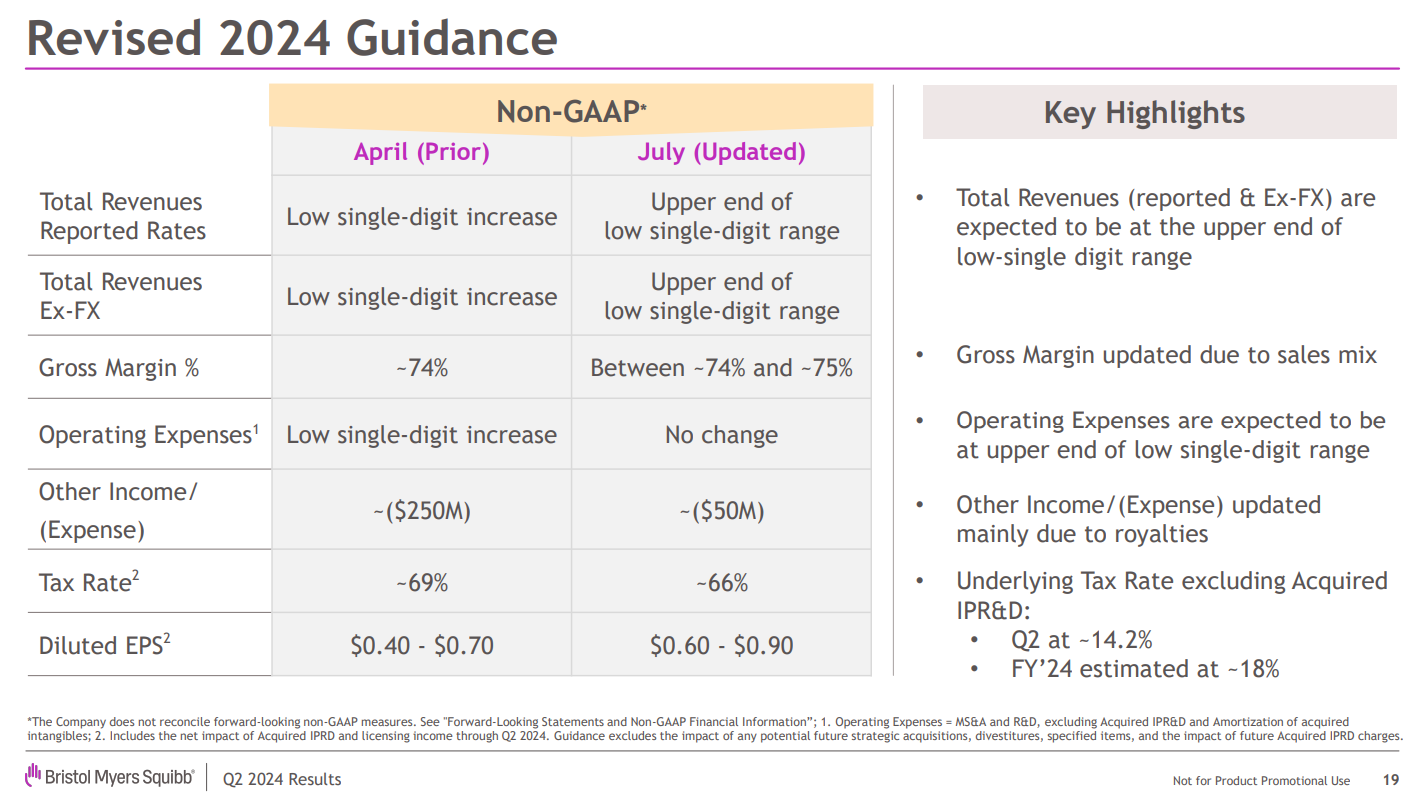
百时美施贵宝还小幅提高了2024年收入财务指引,将营收增长率由此前预测的低个位数增长调整为低个位数范围的上限。
锕[225Ac]标记核药研发进展
据统计,全球已有22项锕[225Ac]标记核药进入临床。锕[225Ac]的适应症有前列腺癌、神经内分泌肿瘤、乳腺癌等,目前中国企业开展了2项基于锕[225Ac]的核药管线,海外有22项锕[225Ac]核药管线进入临床,其中有8个管线处于临床II期,14个管线处于临床I期,还没有进入III期临床的管线。据悉,艾博兹医药的RYZ101是全球首个进入临床阶段的锕[225Ac]偶联靶向核药,旨在将高效放射性同位素锕[225Ac]递送至表达SSTR2的肿瘤部位。
目前,诺华、强生和礼来都正在进行锕[225Ac]标记核药的一期研究。阿斯利康计划收购的Fusion Pharmaceuticals正在进行锕[225Ac]标记核药治疗前列腺癌的二期研究。
MNC抢滩布局核药市场
最近几个季度,大型制药商在放射性制药初创公司上投入了数十亿美元,建立了多种合作伙伴关系和收购。
除了百时美施贵宝去年12月收购RayzeBio之外,礼来(Eli Lilly)、诺华 (Novartis) 和阿斯利康 (AstraZeneca) 近几个月都进行了数十亿美元或更大的收购。比如今年3月19日,阿斯利康以交易总额约24亿美元收购Fusion Pharmaceuticals,将其一款基于Ac-225同位素的2期临床核心产品FPI-2265收入囊中。今年5月,礼来斥资11.6亿美元与Aktis Oncology达成多靶点发现合作协议,利用Aktis的新型微型蛋白技术平台生产肿瘤放射性药物;诺华宣布将以17.5亿美元收购Mariana Oncology,该公司利用α和β放射性核素开发放射性药物。
核药融资情况
随着诺华Pluvicto的成功,加上国家政策的支持,核药赛道开始受到资本追捧,2024年以来全球核药市场投融资也呈现出火热态势。2024年上半年约有11家核药企业获得融资,融资金额超37亿元。
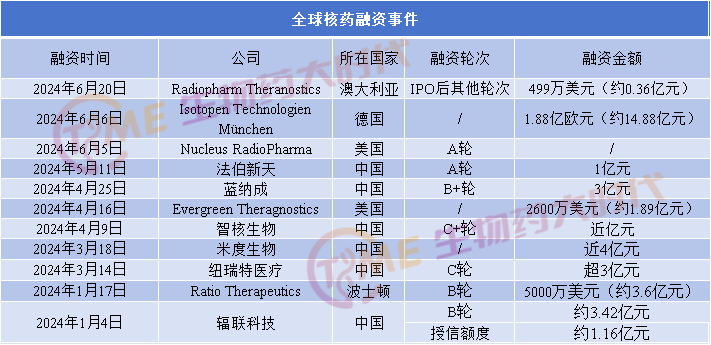
今年下半年,Telix Pharmaceuticals成功发行了价值6.5亿澳元(约合31亿人民币)的可转债创下2024年核药领域最高金额融资记录,这笔资金将为公司提供财务灵活性,以用于进行具有战略意义的并购交易,并继续投资于全球供应链和生产制造。7月,专注于可视化诊疗一体靶向放射性核素疗法(TRT)的生物技术公司晶核生物宣布完成近亿元A轮融资,资金将主要用于JH02的全球临床I/II期试验、68Ga-JH03/177Lu-JH04的中美IND申报及临床开发,以及后续多个创新性管线临床前研究和国际合作。
参考资料:
[1]https://endpts.com
[2]https://mp.weixin.qq.com/s/T6fLmVvt1wJUjFVZn-9J0w
<END>
想要解锁更多药物研发信息吗?查询药融云数据库(vip.pharnexcloud.com/?zmt-mhwz)掌握药物基本信息、市场竞争格局、销售情况与各维度分析、药企研发进展、临床试验情况、申报审批情况、各国上市情况、最新市场动态、市场规模与前景等,以及帮助企业抉择可否投入时提供数据参考!注册立享15天免费试用!























































 川公网安备51019002008863号
川公网安备51019002008863号 本网站未发布麻醉药品、精神药品、医疗用毒性药品、放射性药品、戒毒药品和医疗机构制剂的产品信息
本网站未发布麻醉药品、精神药品、医疗用毒性药品、放射性药品、戒毒药品和医疗机构制剂的产品信息
收藏
登录后参与评论
暂无评论