
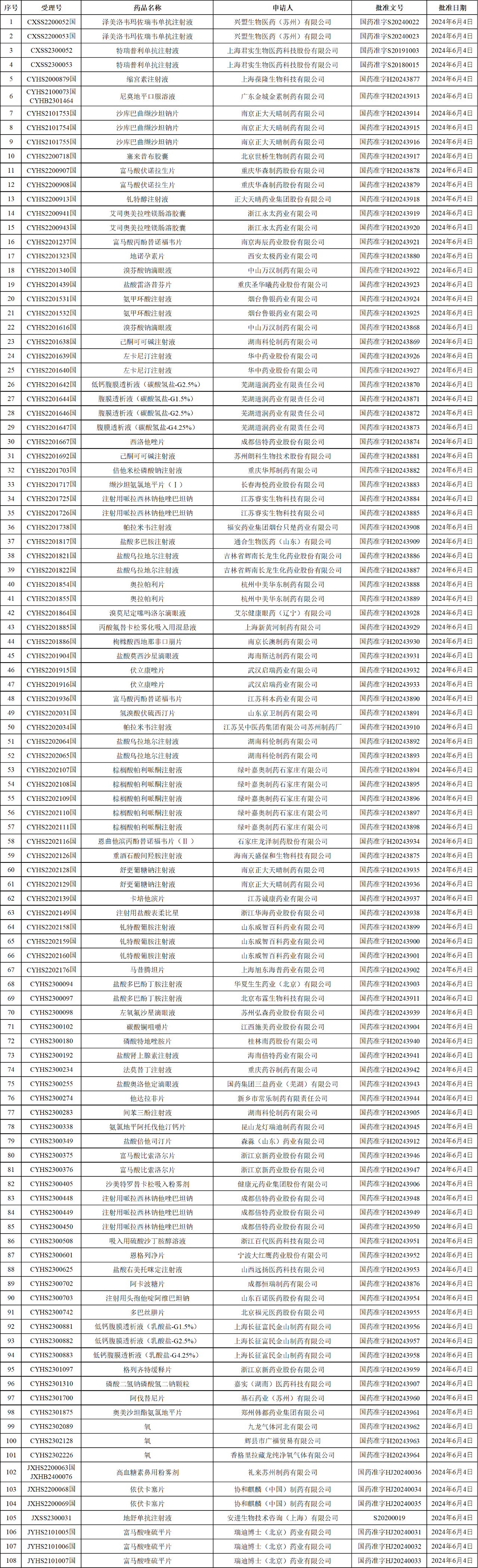
昨日,NMPA发布2024年06月12日药品批准证明文件送达信息,本批次共有108个上市申请受理号获批。
其中:
兴盟生物医药(苏州)有限公司的泽美洛韦玛佐瑞韦单抗注射液获批上市。据公开资料显示,该药是一款抗狂犬病病毒单克隆抗体组合制剂——单抗鸡尾酒疗法产品,主要用于成人狂犬病病毒暴露者的被动免疫。
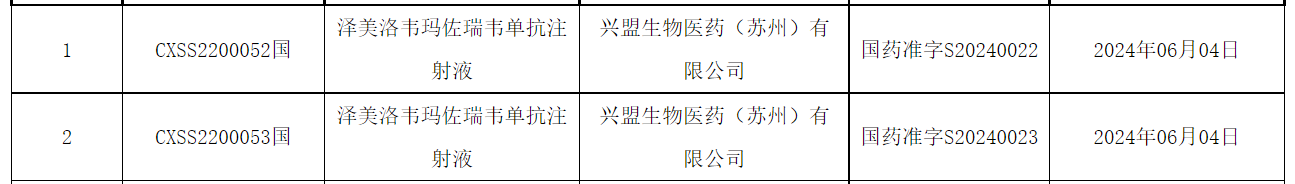
君实生物的特瑞普利单抗新适应症获批,联合依托泊苷和铂类用于广泛期小细胞肺癌一线治疗。
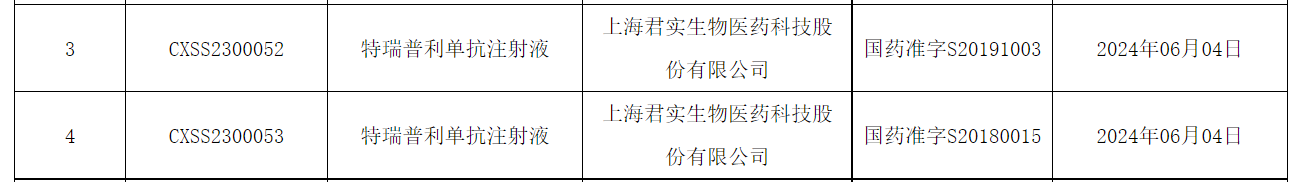
根据公开资料显示,特瑞普利单抗此前已在中国内地获批8项适应症,涵盖黑色素瘤、鼻咽癌、尿路上皮癌、食管鳞癌、非小细胞肺癌、肾癌等,其用于PD-L1阳性的初治转移或复发转移性三阴性乳腺癌的新适应症上市申请也正在审评中。
礼来申报的5.1类新药高血糖素鼻用粉雾剂获批上市。该药是一款经过鼻喷给药的高血糖素鼻用粉雾剂,本次获批的适应症为用于4岁及以上糖尿病患者严重低血糖治疗。

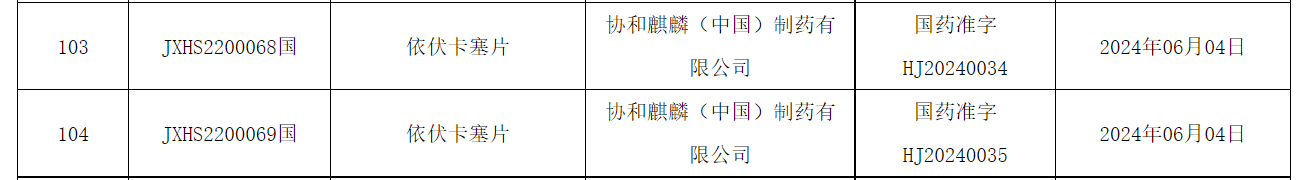
协和麒麟(中国)申报的5.1类新药依伏卡塞片获批上市。根据公开资料显示,依伏卡塞(evocalcet)属于一种新型拟钙剂,本次在中国获批用于治疗继发性甲状旁腺功能亢进症(SHPT)。
安进的地舒单抗注射液新适应症获批上市,具体适应症尚未披露。

除上述新药外,另有多款仿制药获批,如:南京正大天晴制药的沙库巴曲缬沙坦钠片、舒更葡糖钠注射液;重庆华森制药的富马酸伏诺拉生片;长春海悦药业的缬沙坦氨氯地平片(Ⅰ);杭州中美华东制药的奥拉帕利片;绿叶嘉奥制药的棕榈酸帕利哌酮注射液;浙江京新药业的格列齐特缓释片;基石药业的阿伐替尼片等。
<END>
想要解锁更多药物研发信息吗?查询药融云数据库(vip.pharnexcloud.com/?zmt-mhwz)掌握药物基本信息、市场竞争格局、销售情况与各维度分析、药企研发进展、临床试验情况、申报审批情况、各国上市情况、最新市场动态、市场规模与前景等,以及帮助企业抉择可否投入时提供数据参考!注册立享15天免费试用!




































![医药高地:核药!恒瑞医药镥[177Lu]氧奥曲肽注射液获批临床](https://oss-personal-public.bcpmdata.com/images/covers/202302/09/e3938ad9f1d23e2fd043611c4a98c02a.png)


















 川公网安备51019002008863号
川公网安备51019002008863号 本网站未发布麻醉药品、精神药品、医疗用毒性药品、放射性药品、戒毒药品和医疗机构制剂的产品信息
本网站未发布麻醉药品、精神药品、医疗用毒性药品、放射性药品、戒毒药品和医疗机构制剂的产品信息
收藏
登录后参与评论
暂无评论