
Neumora Therapeutics 公司周一宣布,美国食品及药物管理局(FDA)已暂停其精神分裂症候选药物 NMRA-266的I期临床试验,因其近期获得的临床前数据显示该药会引发兔子抽搐。(相关阅读:新锐!5亿美元A轮融资,Neumora Therapeutics推出脑疾病精准医学新时代)

目前已有约30名患者参加了NMRA-266的I期递增剂量研究,其中没有人出现抽搐症状。未来公司将与FDA合作,找到解决临床搁置问题的最佳方法。
即便如此,受此消息影响,Neumora的股价仍在周一盘前交易中下跌了18%。

NMRA-266是M4毒蕈碱受体的正性变构调节剂(PAM),激活后可抑制大脑中神经递质乙酰胆碱的释放。在精神分裂症中,这些 M4 受体调节的回路被破坏,从而产生该疾病特有的阳性、阴性和认知症状。
Neumora 在上个月发布的 2023 年第四季度和全年财报中表示,公司计划在2024 年中期报告NMRA-266 的I期数据。该公司还希望在今年下半年启动该候选药物的 Ib期试验,预计在2025年获得初步结果。然而,在本周一的临床搁置之后,Neumora公司之前的指导就不再适用了。
Neumora 将专注于开发其他管线资产,包括主导项目navacaprant,这是一种口服高选择性κ阿片受体(KOR)拮抗剂,目前正处于III期开发阶段,是治疗重度抑郁障碍的单一疗法,目前navacaprant正处于三期临床阶段,双相情感障碍的II期临床适应症也在开展中。
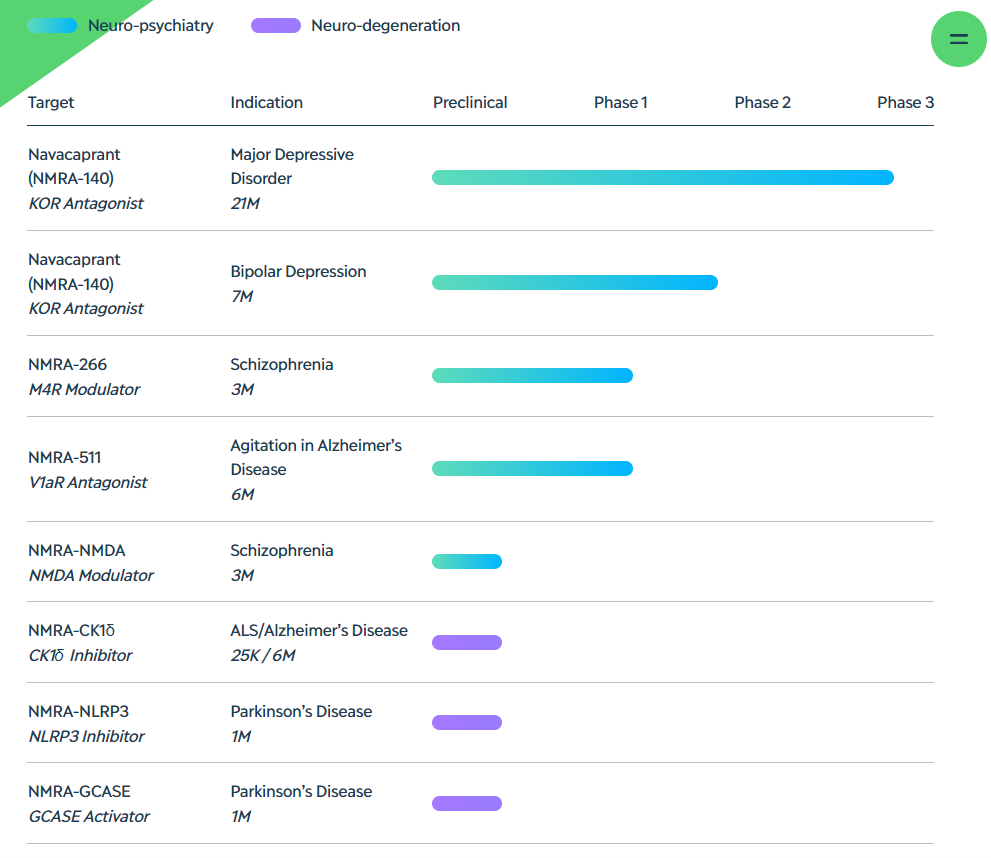
首席执行官Gosebruch在一份声明中说:"我们预计将迎来几个重要的里程碑,包括重度抑郁症的III期研究数据,以及启动navacaprant治疗双相抑郁症的II期研究,"他还补充说,Neumora公司还将启动其在研血管加压素1a受体拮抗剂NMRA-511的阿尔茨海默病Ib期研究。
在本周一的临床试验之前一周,百时美施贵宝公司的抗精神病药物KarXT在精神分裂症晚期研究中取得了重大胜利,在EMERGENT-4的III期研究中,超过75%的患者在52周的随访中症状得到了至少30%的改善。KarXT 最初由 Karuna Therapeutics 开发,BMS于2023年12月以140亿美元的价格收购了 Karuna Therapeutics。
勃林格殷格翰公司也瞄准了这一市场,该公司上个月与 Sosei Heptares 公司达成了一项高达 7.32 亿美元的交易,获得了后者治疗精神分裂症所有症状的一流 GRP52 激动剂的许可权。
<END>
要解锁更多企业药品研发信息吗?查询药融云数据库(vip.pharnexcloud.com/?zmt-mhwz)掌握药品各国上市情况、药品批文信息、销售情况与各维度分析、市场竞争格局、一致性评价情况、集采中标情况、药企申报审批信息、最新动态与前景等,以及帮助企业抉择可否投入时提供数据参考!注册立享15天免费试用!

















































 浙公网安备33011002015279
浙公网安备33011002015279 本网站未发布麻醉药品、精神药品、医疗用毒性药品、放射性药品、戒毒药品和医疗机构制剂的产品信息
本网站未发布麻醉药品、精神药品、医疗用毒性药品、放射性药品、戒毒药品和医疗机构制剂的产品信息
收藏
登录后参与评论
暂无评论