
2024年4月3日,美国食品药品监督管理局(FDA)宣布批准Basilea Pharmaceutica公司自研新分子实体药物Zevtera(有效成分:Ceftobiprole Medocaril Sodium)上市。Zevtera用于治疗金黄色葡萄球菌血流感染(菌血症)(SAB)成人患者(包括右侧感染性心内膜炎患者),急性细菌性皮炎和皮肤结构感染(ABSSSI)成人患者,以及社区获得性细菌性肺炎(CABP)成人和儿童患者(3个月至18岁以下)。
Zevtera用于菌血症(SAB)的治疗
金黄色葡萄球菌血流感染(菌血症)(SAB)是指细菌出现在血流中。可能经由泌尿道或静脉插管自发发生,也可能继发于口腔、消化道、泌尿道或创伤的护理或者其他操作。菌血症可能导致迁徙性感染,包括心内膜炎,尤其是存在心脏瓣膜病变者。隐性菌血症通常没有症状,但可导致发热。其他症状出现常常提示更加严重的感染,例如脓毒症或脓毒性休克。
一项随机、双盲、多中心的III期临床研究(NCT03138733),评估了Zevtera与Daptomycin(达托霉素)相比在治疗金黄色葡萄球菌菌血症(包括感染性心内膜炎)中的有效性和安全性。本次临床试验于2018年8月26日由Basilea开展,在2022年3月11日完成,共入组390名金黄色葡萄球菌菌血症患者。在试验中,研究人员随机分配了192名受试者接受Zevtera治疗,198名受试者接受Daptomycin(达托霉素)作为对照治疗。Zevtera治疗组在开始后前8天每6小时静脉注射一次,之后每8小时静注一次,Daptomycin(达托霉素)对照治疗组每24小时静脉注射一次。主要疗效指标是随机分组后70天的总体治疗成功率,包括存活率、症状减轻、金黄色葡萄球菌血流清除率、无新的金黄色葡萄球菌菌血症相关并发症以及未使用其他潜在有效抗生素。
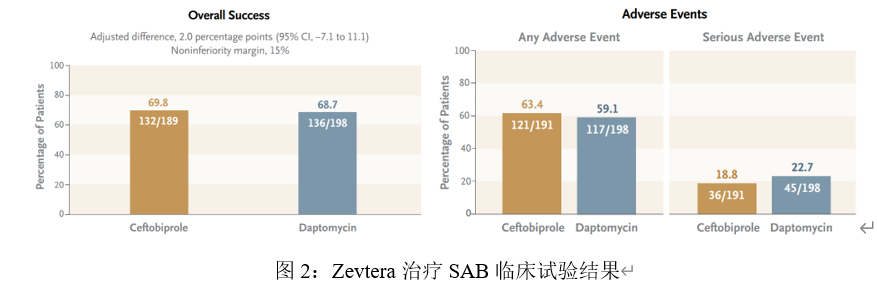
临床结果显示,在有效性方面,在接受Zevtera治疗的受试者中,69.8%的受试者取得了总体成功,而在接受对照药治疗的受试者中,68.7% 的受试者取得了总体成功;在安全性方面,两组患者发生不良反应或严重不良反应的比例相似。Zevtera组的受试者胃肠道不良反应发生率略高于Daptomycin(达托霉素)组。这些数据表明Zevtera的治疗效果并不比Daptomycin(达托霉素)差。
Zevtera用于ABSSSI的治疗
急性细菌性皮炎和皮肤结构感染(ABSSSI)是一种复杂且完全的皮肤细菌感染,目前ABSSSI的主要症状包括蜂窝织炎、丹毒、淋巴管炎等,在过去的20年里,世界范围内被诊断出的ABSSSI患者数量逐步增加,ABSSSI常见并发症包括继发性关节感染、血液感染(BSI)和截肢,其中BSI被认为是最为严重的并发症之一,细菌会随着血液循环累及身体各个器官,严重的患者可以引起多脏器功能衰竭或引起感染脓毒症休克,危及生命。
一项随机、双盲、多中心的III期临床研究(NCT03137173)比较了Zevtera与Vancomycin(万古霉素)对于ABSSSI治疗的有效性和安全性,该项临床试验于2018年2月19日开展,于2019年4月22日完成,共入组679名ABSSSI患者,其中335名受试者接受Zevtera治疗,另外344名受试者接受Vancomycin(万古霉素)联合氨曲南治疗。本次试验的主要疗效终点是意向治疗(ITT)人群开始治疗 48-72 小时后的早期临床反应。早期临床反应要求原发皮损缩小至少 20%,存活至少 72 小时,并且没有额外的抗菌治疗或意外手术。
结果显示,Zevtera治疗组的早期临床成功率为 91.3%,而对照组的早期临床成功率为 88.1%,非劣效性得到证实(调整后差异:3.3%;95% CI:-1.2, 7.8)。两组在治愈试验(TOC)检查时由研究者评估的临床成功率相似,在ITT(90.1% vs 89.0%)和临床可评估人群(97.9% vs 95.2%)中均显示出非劣效性。两组治疗的成功率和安全性相似。这些结果表明Zevtera的治疗效果并不比万古霉素/氨曲南差。

图3:Zevtera治疗ABSSSI临床试验结果
Zevtera用于CABP的治疗
社区获得性细菌性肺炎(CABP)是一种普遍而严重的感染。每五名CABP患者中就有一名感染严重,需要住院治疗,这些患者的死亡率为 8%。在确诊CABP后,应在数小时内开始使用涵盖可能病原体的抗生素进行治疗。延迟抗生素治疗或使用无效抗生素治疗会增加患者发病率和死亡率。
一项随机、双盲、多中心的III期临床研究(NCT00326287)评估了Zevtera与安慰剂组相比对于社区获得性细菌性肺炎(CABP)的治疗效果,该项临床试验开始于2006年6月,于2007年7月结束,共入组638名受试者。这其中的314名受试者接受Zevtera治疗,其余324名受试者接受Ceftriaxone(头孢曲松)治疗。疗效的主要衡量指标是治疗结束后7-14天进行的临床治愈率检测。
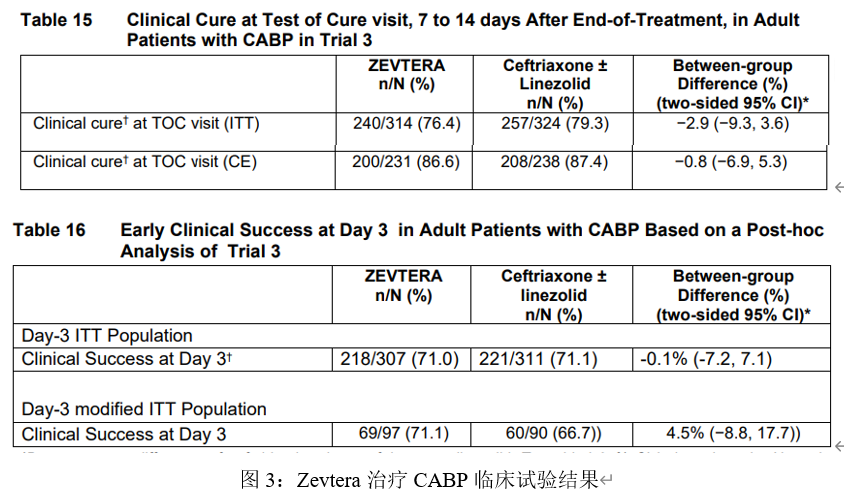
结果显示,在接受Zevtera治疗的受试者中,76.4%的人达到了临床治愈,而在接受对照药治疗的受试者中,79.3%的人达到了临床治愈。另一项分析考虑了更早的第3天临床治愈时间点,接受Zevtera治疗的患者中71%获得了临床治愈,而接受对照药治疗的患者中71.1%获得了临床治愈。
这些结果表明,对于在社区环境中感染肺炎并需要住院治疗的患者而言,静脉注射Zevtera的疗效并不亚于Ceftriaxone(头孢曲松)联合或不联合linezolid(利奈唑胺)。
Zevtera临床历程
本次FDA的批准是基于Zevtera在3项关键的III期临床研究中表现出的积极结果,分别是NCT03138733、NCT03137173和NCT00326287,这3项临床研究分别评估了Zevtera用于SAB、ABSSSI和CABP患者治疗的安全性和有效性,此外在世界范围内Zevtera开展几十项临床研究,充分评估了其药效学、药代动力学、安全性、有效性、耐受性等,以下归纳了部分Zevtera重要的临床研究。

总结
Zevtera是一款静脉注射的新一代头孢抗生素,可快速杀死多种革兰氏阳性细菌(如金黄色葡萄球菌,包括耐甲氧西林菌株)和革兰氏阴性菌。FDA药物评价与研究中心抗感染药物部主任Peter Kim说:"FDA致力于促进被证明安全有效的新抗生素的供应,Zevtera将为一些严重的细菌感染提供额外的治疗选择。"更多药物信息请登录药融云数据库查看。
参考资料:
[1]FDA官网:https://www.fda.gov/
[2]Basilea 官网:https://www.basilea.com/
[3]Holland TL, Cosgrove SE, Doernberg SB, et al. Ceftobiprole for Treatment of Complicated Staphylococcus aureus Bacteremia. N Engl J Med. 2023;389(15):1390-1401.
[4]Overcash JS, Kim C, Keech R, et al. Ceftobiprole Compared With Vancomycin Plus Aztreonam in the Treatment of Acute Bacterial Skin and Skin Structure Infections: Results of a Phase 3, Randomized, Double-blind Trial (TARGET). Clin Infect Dis. 2021;73(7):e1507-e1517.
<END>
要解锁更多企业药品研发信息吗?查询药融云数据库(vip.pharnexcloud.com/?zmt-mhwz)掌握药品各国上市情况、药品批文信息、销售情况与各维度分析、市场竞争格局、一致性评价情况、集采中标情况、药企申报审批信息、最新动态与前景等,以及帮助企业抉择可否投入时提供数据参考!注册立享15天免费试用!






























![医药高地:核药!恒瑞医药镥[177Lu]氧奥曲肽注射液获批临床](https://yaorongyun-public.oss-cn-shanghai.aliyuncs.com/images/covers/202302/09/e3938ad9f1d23e2fd043611c4a98c02a.png)












 浙公网安备33011002015279
浙公网安备33011002015279 本网站未发布麻醉药品、精神药品、医疗用毒性药品、放射性药品、戒毒药品和医疗机构制剂的产品信息
本网站未发布麻醉药品、精神药品、医疗用毒性药品、放射性药品、戒毒药品和医疗机构制剂的产品信息
收藏
登录后参与评论