
近日,传奇生物(NASDAQ:LEGN)在美国新泽西州萨默塞特发布了2023年第四季度和全年的未经审计财务业绩以及公司主要亮点。
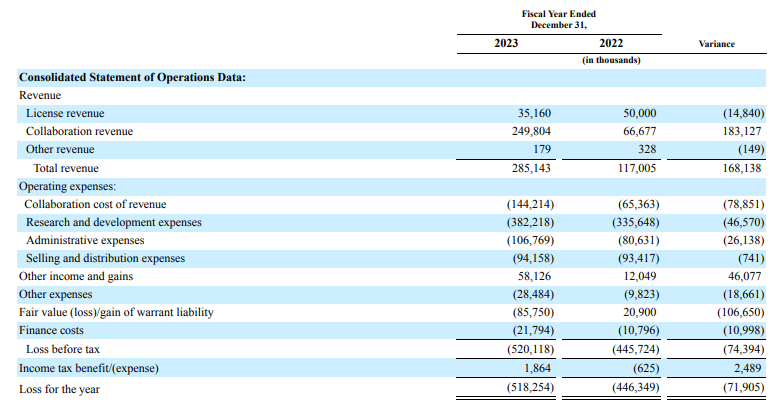
财报显示,2023年传奇生物总营收2.85亿美元,同比增长143.7%;合作收入2.5亿美元,同比增长275%,主要由与杨森协议相关的CARVYKTI®销售额增加驱动的;研发费用3.82亿美元,同比增长13.9%,主要是cilta-cel的持续研发活动,包括3期临床试验患者入组率增加以及其他管线产品研发活动增多导致的。
其中2023 Q4总营收7946.4万美元,同比增长187.6%。
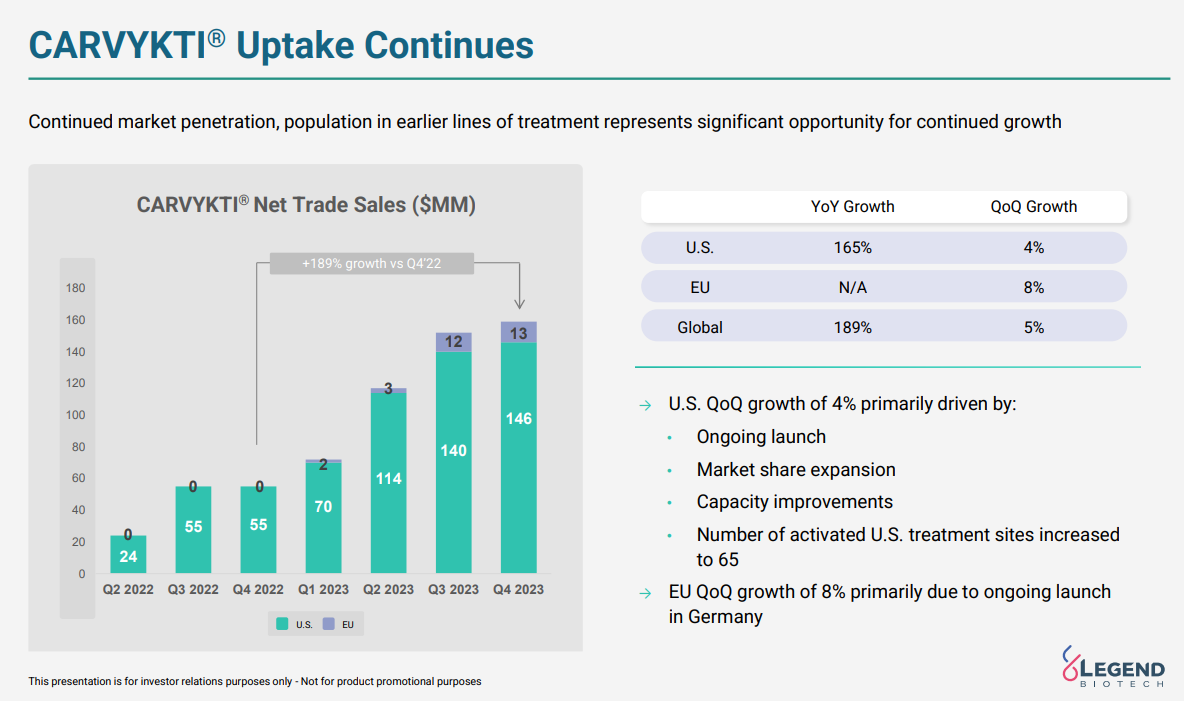
早在1月份,强生发布2023年全年业绩时就有披露CARVYKTI®(西达基奥仑赛,cilta-cel)2023 Q4销售额约1.59亿美元,较2022年大增194%;2023全年总销售额为5亿美元,同比增长276%,明年有望突破10亿美元。
2017年12月,传奇生物与强生制药就Carvykti以3.5亿美元首付款签订合作协议,共同负责全球范围的药物开发、临床试验、生产及商业化;中国分成:传奇生物70%、强生30%;其他地区分成:各按50%。

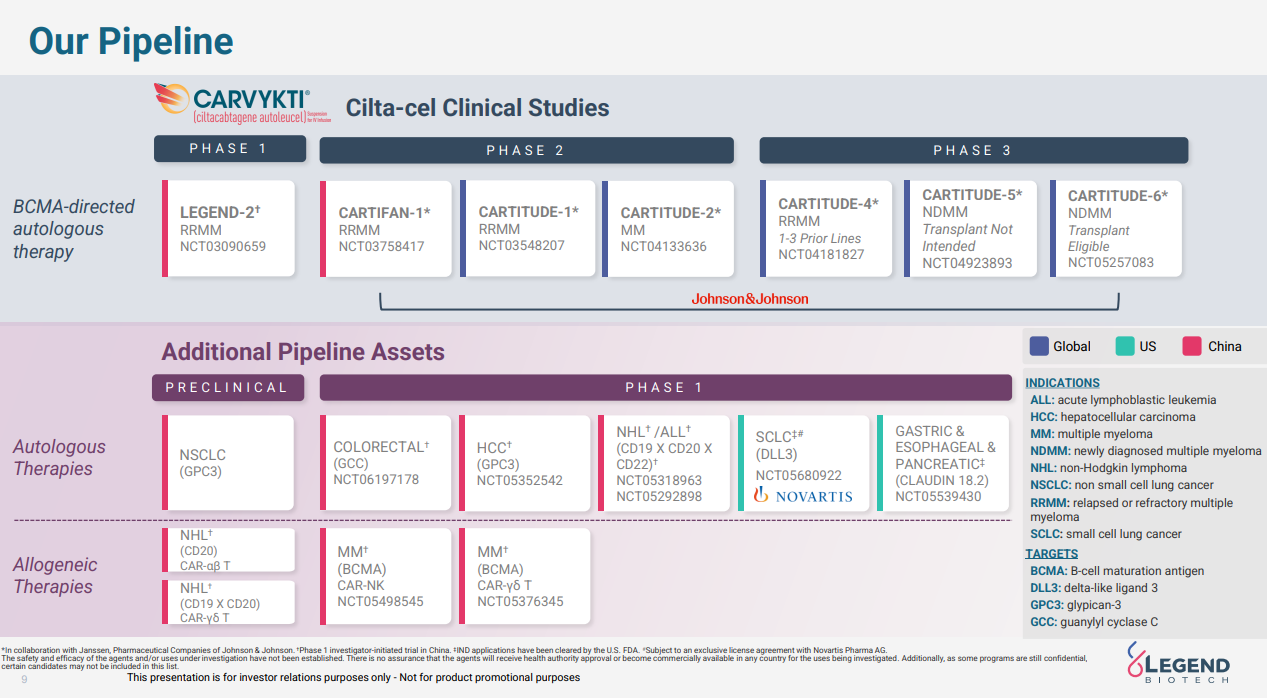
Carvykti是全球第2款BCMA CAR-T疗法,2022年2月28日,CARVYKTI获得美国FDA批准上市,用于治疗复发或难治性多发性骨髓瘤(R/R MM)患者。2022年12月30日,传奇生物在国内递交的「西达基奥仑赛注射液」上市申请获受理(受理号:CXSS2200094)。2023年1月12日,西达基奥仑赛上市申请拟纳入优先审评。2023年6月6日,传奇生物向FDA递交补充生物制品许可申请(sBLA),扩大CARVYKTI适应症范围,纳入既往至少接受过一种治疗(包括一种蛋白酶体抑制剂和一种免疫调节剂)的复发且来那度胺耐药的多发性骨髓瘤成人患者。
此外,强生/传奇生物已经向欧盟EMA和FDA提交了扩大Carvykti适应症的申请,FDA将PDUFA目标审评日期定为2024年4月5日。
传奇生物还更新了其主要业务进展:
▪ 2024年1月3日,根据与诺华制药股份公司达成的开发、生产和商业化LB2102以及特定靶向DLL3的其他潜在嵌合抗原受体T细胞(CAR-T)疗法的全球许可协议,传奇生物获得1亿美元的预付款。
▪ CARVYKTI®现已在德国和奥地利上市,在全球80多家授权治疗中心治疗了2,500多例患者,商业需求持续增加。
▪ 自2023年初以来,产能扩张了100%,包括在根特的Obelisc新工厂开始临床生产。
▪ 计划到2025年底实现年产能10,000剂的目标。
▪2023年美国血液学学会年会上公布的3期CARTITUDE-4研究患者报告结局数据表明,与标准疗法相比,CARVYKTI®经治患者的健康相关生活质量获得有临床意义的改善,多发性骨髓瘤也有所减轻。
传奇生物目前每股价格62.82美元,市值114.5亿美元,较去年同期增长27%。
总结
BCMA CAR-T疗法的赛道越来越火热。BCMA CAR-T疗法的开拓者Abecma在2023年全球收入为4.72亿美元,同比增长22%。
中国在该赛道中突破不断。去年6月,驯鹿生物和信达生物开发的伊基奥仑赛注射液(商品名:福可苏)获批上市,适应症同为复发或难治性多发性骨髓瘤成人患者,为国内首款款全人源靶向BCMA CAR-T细胞治疗药物。今年3月1日,科济药业的BCMA CAR-T产品赛恺泽®(泽沃基奥仑赛注射液)获NMPA批准上市,用于治疗复发或难治性多发性骨髓瘤成人患者。
除此之外,还有包括恒润达生的HR003、亘喜生物的GC012F、西比曼生物的C-CAR088以及精准生物的C-4-29等多款BCMA CAR-T/双靶点BCMA CAR-T产品处于临床阶段。
放眼全球,Cartesian公司开发的BCMA CAR-T疗法Descartes-08,用于治疗全身性重症肌无力(gMG)2期临床即将于2024上半年启动。Arcellx公司开发的BCMA CAR-T疗法Anito-cel用于治疗复发性或难治性多发性骨髓瘤患者的1期结果显示缓解率100%,相信在未来BCMA CAR-T疗法有望在更多适应症中发挥价值,为患者提供治愈希望。
<END>
要解锁更多企业药品研发信息吗?查询药融云数据库(vip.pharnexcloud.com/?zmt-mhwz)掌握药品各国上市情况、药品批文信息、销售情况与各维度分析、市场竞争格局、一致性评价情况、集采中标情况、药企申报审批信息、最新动态与前景等,以及帮助企业抉择可否投入时提供数据参考!注册立享15天免费试用!






















































 川公网安备51019002008863号
川公网安备51019002008863号 本网站未发布麻醉药品、精神药品、医疗用毒性药品、放射性药品、戒毒药品和医疗机构制剂的产品信息
本网站未发布麻醉药品、精神药品、医疗用毒性药品、放射性药品、戒毒药品和医疗机构制剂的产品信息
收藏
登录后参与评论
暂无评论