
2023年7月,Recordati制药集团宣布与GSK(葛兰素史克)达成协议,在21个国家(主要是欧洲)将Avodart(度他雄胺)和Combodart/Duodart(度他雄胺+ tamsulosin)商业化,但不包括那些已经签订分销协议的国家。Avodart和Combodart/Duodart可以用于治疗良性前列腺增生(BPH)的中度至重度症状,并降低中度至重度BPH症状患者的急性尿潴留(AUR)和手术风险。

Recordati首席执行官Rob Koremans表示:该协议为Recordati提供了两个领先的原创品牌,加强了公司在泌尿科领域的业务,与公司目前的产品组合具有协同作用,满足了不用的患者需求并具有不同的定位。
1.公司简介
据药融云数据库显示:Recordati制药集团成立于1926年,总部位于米兰,是意大利历史最悠久的制药公司之一。自成立以来,该集团不断发展壮大,成为一家领先的国际制药集团,并于1984年在意大利证券交易所上市。目前集团员工超过4600多人,主要致力于心血管和泌尿生殖系统治疗领域中新药实体的研发,以及罕见疾病的治疗方法。Recordati集团的增长得益于其产品和服务的质量,以及基于业务发展和收购的重点战略实施国际化和多元化政策。
除了在西欧和中东欧的子公司外,Recordati还在美国、加拿大、墨西哥、南美的几个国家、中东、日本、澳大利亚和新西兰、中国、韩国、蒂尔基耶和北非直接开展业务。目前集团拥有七家制药工厂和一家专门生产罕见病药物的包装和分销工厂,以及两个生产多种活性物质和中间体的化学制药工厂。
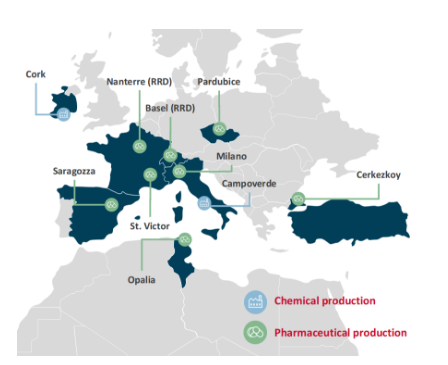
Recordati通过Recordati Rare Diseases在全球开展罕见病业务,覆盖全球100多个国家,Recordati Rare Diseases是完全致力于研究,开发和销售用于治疗罕见疾病的药物的业务部门。其产品组合最初致力于罕见的遗传代谢疾病,通过从诺华公司获得Isturisa(osilodrostat)、Signifor(门冬氨酸帕瑞肽)和长效药物Signifor LAR(pasireotide pamoate)这3款内分泌药物,从而巩固了其产品组合。
2022年,通过收购专注于治疗罕见肿瘤疾病的全球生物制药公司EUSA Pharma,Recordati在其治疗罕见和稀有肿瘤疾病的产品组合中增加了四种具有高增长潜力的产品。近年来,该集团开发治疗罕见疾病的药物的活动已扩展到北美和南美的各个国家,以及中东,日本,澳大利亚,新西兰,中国和韩国。目前公司市值约102.7亿美元(截止2023年11月15日)。

收购EUSA Pharma相关报道

目前公司市值在全球医药企业排行61位
2.产业布局
Recordati集团生产和推广一系列创新药物,制药活动延伸到该过程的所有阶段,包括研发、生产、包装、储存和商业化。
主要产品
Recordati的产品涵盖化学药品、SPC(专业和初级保健)以及罕见病领域。其中化学制药业务主要是为Recordati制药产品和国际制药行业生产中间体和活性物质;SPC涵盖从2b期临床阶段到上市的创新产品,包括心脏代谢、泌尿科/泌尿肿瘤科、胃肠、咳嗽和感冒;罕见病领域重点关注内分泌学、肿瘤学和代谢等。
知名的产品包括用于治疗心血管疾病的药物Zanidip(乐卡地平)和Zanipress/Zanextra(乐卡地平+依那普利)。其中,Zanidip是一种二氢吡啶类钙通道阻滞剂,可单独使用或与血管紧张素转换酶抑制剂联合使用,用于治疗高血压、慢性稳定型心绞痛和Prinzmetal变异型心绞痛。
Zanipress/Zanextra为血管紧张素转换酶抑制剂(ACEI),用于治疗单用乐卡地平或依那普利无法控制的原发性高血压;同时,还提供Seloken(琥珀酸美托洛尔),主要用于治疗高血压、心绞痛、心肌梗死等疾病,2017年Recordati从阿斯拉康购买了该产品在欧洲的销售权;泌尿科领域的代表产品包括Eligard(醋酸亮丙瑞林),用于晚期前列腺癌的姑息治疗;在代谢领域,Recordati销售Alipza(匹伐他汀),主要用于控制高胆固醇血症的他汀类药物;在胃肠病学领域,提供清洁肠道和治疗便秘的综合产品;中枢神经系统区域,提供治疗精神分裂症的抗精神病药物Reagila(cariprazine)。
以下是公司的部分产品清单:
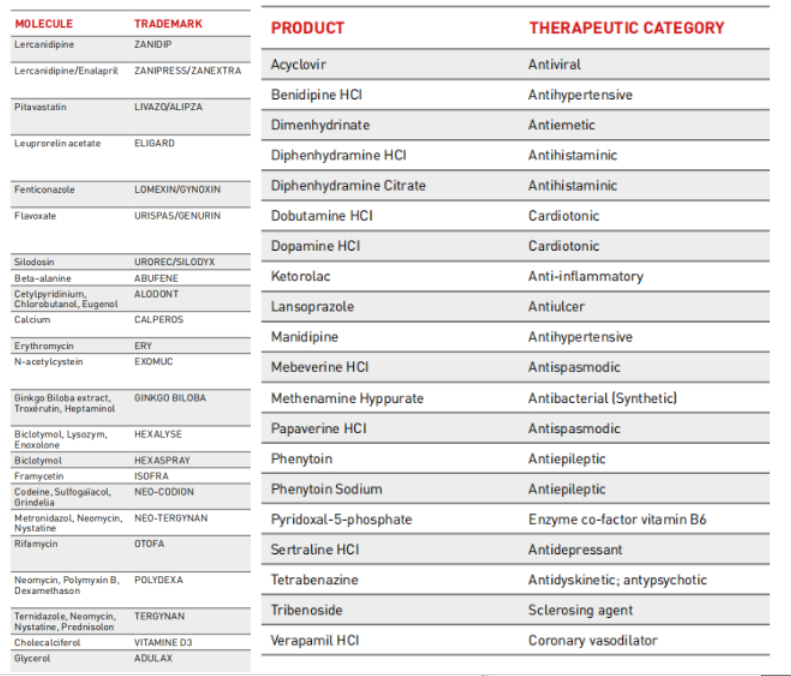
研发管线
Recordati的研发部门由一支高度专业化的研究人员和技术人员组成,不断开发源自内部或通过其他制药公司和研究机构的开发协议获得新管线,研发管线包括已有药物的新适应症开发和新药物的研究。
已有药物的研发管线

Eligard(醋酸亮丙瑞林)是一种用于治疗晚期前列腺癌的注射用处方药,从Tolmar获得,目前正在开发用于激素依赖性前列腺癌,新方法批准后将会继续进行研究。
Isturisa(osilodrostat)已在美国、欧洲、瑞士、澳大利亚、以色列和日本获批用于治疗内源性库欣综合征/库欣病,目前正在其他国家备案。Isturisa是FDA批准的第一个通过阻断11β-羟化酶和阻止皮质醇生物合成直接解决皮质醇过量产生的药物。Signifor(门冬氨酸帕瑞肽)已获批用于治疗垂体依赖性库欣病,目前在研究通过皮下注射来治疗肥胖后低血糖患者,正在进行临床试验2期研究。2019年7月,诺华将Isturisa、Signifor(门冬氨酸帕瑞肽)和长效药物Signifor LAR(pasireotide pamoate)这3款内分泌药物以3.9亿美元出售给了Recordati。

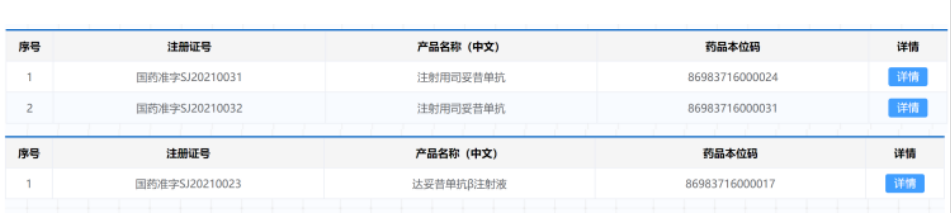
截图来源:药融云全球药物研发数据库
Cystadrops(cysteamine hydrochloride)已在美国和欧盟获批用于胱氨酸病患者的角膜胱氨酸结晶沉积,当前正在美国和欧盟进行新制剂的开发。
Qarziba(达妥昔单抗β)已在欧盟、英国、澳大利亚、巴西、以色列、俄罗斯、中国香港和中国台湾获批用于治疗用于治疗高危及复发难治性神经母细胞瘤患者。目前正在包括美国和瑞士地区进行注册。Sylvant(司妥昔单抗)已在在包括欧盟、美国和中国在内的40多个国家获批用于中心型Castleman病(又称特发性MCD,iMCD)。目前正在进行潜在适应症扩展评估。Qarziba和Sylvant均通过收购EUSA Pharma获得。2020年初,EUSA Pharma与百济神州就Sylvant(司妥昔单抗)及Qarziba(达妥昔单抗β)在大中华地区达成独家开发和商业化协议,且两种药物已获得中国国家药品监督管理局批准。
新药研发
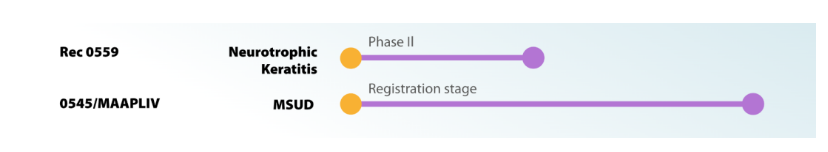
REC 0559是一种p75NTR激动剂候选药物,由MimeTech SRL (MIME技术有限公司)公司最早进行研发,目前由Recordati在全球范围内开发,正在研究用于神经营养性角膜炎,当前进行到临床试验2期,国内未研发。FDA已授予REC 0559孤儿药资格。REC 0545一种5-HT1A receptor拮抗剂药物,目前正准备开发用于枫糖浆尿病,预计在今年提交,国内未研发。
3.财务状况
以下是Recordati近五年来的营收趋势,在2022年表现出了强劲的收入势头。

据药融云数据库显示:2022年合并净收入为18.533亿欧元,与上年同期相比增加17.3%,其中包括其与EUSA Pharma收购的罕见病和肿瘤产品组合带来的1.36亿欧元收入。在专业和初级保健部门,除了Eligard的贡献增加外,集团季节性流感和胃肠道疾病的医疗专业销售额持续强劲增长。
在罕见疾病领域,新肿瘤产品的贡献,以及内分泌学特许经营权的持续进步(收入为1.719亿欧元,2021年为1.266亿欧元)以及Panhemathin和Cystadrops在罕见代谢产品组合中的强劲表现支撑了增长。EBITDA为6.728亿欧元,与上年同期相比增长11.7%;净利润为3.123亿欧元,与上年同期相比下降19.1%。

2023年上半年合并净收入为10.443亿欧元,与2022年上半年相比增加17.0%,这得益于所有业务的强劲势头和EUSA Pharma的成功整合。专业和初级保健产品组合在2023年上半年贡献了6.689亿欧元的收入,罕见病业务的收入为3.444亿欧元。反映了与EUSA Pharma收购的罕见肿瘤产品的整合,该产品贡献了9560万欧元的收入。
EBITDA为4.062亿欧元,与2022年同期相比增长21.3%,收入利润率为38.9%(2022年上半年为37.5%),反映了运营杠杆效益和之前宣布的效率举措,以及调整后毛利率的显著弹性,与上一年基本持平。净利润为2.276亿欧元,比2022年同期增长50.3%,占收入的21.8%,这也反映了非经常性支出的显着降低。期内自由现金流为2.617亿欧元,远高于上年同期(增长4300万欧元),吸收了营收增加和现金利息支出增加带来的营运资本增长。
参考:
NMPA/CDE
药融云数据库
相关公司公开披露(除标注外,正文图片均来自企业官网);
https://Recordati.com/media/;等等。
<END>
要解锁更多企业药品研发信息吗?查询药融云数据库(vip.pharnexcloud.com/?zmt-mhwz)掌握药品各国上市情况、药品批文信息、销售情况与各维度分析、市场竞争格局、一致性评价情况、集采中标情况、药企申报审批信息、最新动态与前景等,以及帮助企业抉择可否投入时提供数据参考!注册立享15天免费试用!


















































 浙公网安备33011002015279
浙公网安备33011002015279 本网站未发布麻醉药品、精神药品、医疗用毒性药品、放射性药品、戒毒药品和医疗机构制剂的产品信息
本网站未发布麻醉药品、精神药品、医疗用毒性药品、放射性药品、戒毒药品和医疗机构制剂的产品信息
收藏
登录后参与评论
暂无评论