
2023年11月9日(美国时间11月8日)和黄医药宣布,其与合作伙伴武田共同开发的药物Fruzaqla(呋喹替尼/fruquintinib)在美国获批进入当地医药市场,用于治疗晚期结直肠癌。这是美国首个且唯一获批用于治疗经治转移性结直肠癌的,针对全部三种抗血管内皮生长因子(VEGF)受体的高选择性抑制剂。值得一提的是,这也是第6款在美国FDA上市的国产创新药。
首款在美获批的国产新药:百济神州BTK抑制剂泽布替尼
2019年11月14日,泽布替尼在美国取得全球首次批准,实现中国抗癌新药出海“零的突破”,随后其陆续在中国、加拿大、澳大利亚、俄罗斯、欧盟等多个国家和地区获批上市,目前其商业化足迹已遍布全球40多个市场。此外,其在全球范围内仍有多项药政申报正在审评中。

2021年6月11日举行的26届欧洲血液学协会年会(EHA 2021)网络大会的主席研讨会上,百济神州发布的一项全球头对头3期临床研究最新数据表明:该公司自主研发的抗癌新药泽布替尼(商品名“百悦泽”),以更好的疗效和安全性,在数据上优胜强生公司研发的抗癌药伊布替尼。这是中国创新药首次在头对头中打败欧美跨国公司药物。2022年12月14日,百济神州公布,公司自主研发的BTK抑制剂泽布替尼(商品名:百悦泽®)在全球3期头对头研究ALPINE试验中无进展生存期(PFS)的终期分析结果。
经独立评审委员会(IRC)和研究者评估,泽布替尼对比伊布替尼,用于治疗复发/难治性(R/R)慢性淋巴细胞白血病(CLL)/小淋巴细胞淋巴瘤(SLL)患者,取得PFS的优效性(HR:0.65[95% CI,0.49 ~ 0.86],p = 0.0024)。24个月时,IRC评估的泽布替尼PFS率为79.5%,而伊布替尼则为67.3%。基于ALPINE研究,泽布替尼成为目前全球首个且唯一一款对比伊布替尼,取得PFS与总缓解率(ORR)双重优效性的BTK抑制剂。

百济神州 2023 H1财报显示,百济神州核心自研产品百悦泽®(泽布替尼)持续放量,上半年全球销售额达 36.12 亿元,上年同期为 15.14 亿元。在美国,泽布替尼销售额总计 25.19 亿元,相较上年同期 10.15 亿元,增长超过一倍。在中国,百济神州继续巩固泽布替尼在国内 BTK 市场的领导地位,上半年中国市场销售额总计 6.69 亿元,上年同期为 4.55 亿元。
传奇生物:BCMA CAR-T产品西达基奥仑赛
西达基奥仑赛(Cilta-cel,CARVYKTI)是传奇生物开发的一种CAR-T疗法,在美国和欧洲之前被称为JNJ4528,而在中国则被称为LCAR-B38M细胞疗法。2017年12月传奇生物与强生子公司杨森达成了全球化合作和许可协议,共同对西达基奥仑赛进行开发、生产和商业化。传奇生物向强生授予在全球范围内共同开发和商业化西达基奥仑赛的许可,由传奇生物负责大中华区的价格批准和预订销售,由强生负责世界各地的价格批准和预订销售。根据协议,传奇生物将从杨森获得3.5亿美元的预付款,并有权在开发、生产、监管和销售方面达到里程碑进展时获得额外付款。
该协议规定,在除大中华区以外的全球市场中,传奇生物和杨森公司的成本和利润分摊比例为50%/50%,在大中华区该分摊比例为70%/30%(传奇/杨森)。自此,西达基奥仑赛开启全球性研发、临床、生产的商业化征程。

西达基奥仑赛于2022年2月28日获得FDA批准上市,用于治疗复发或难治性多发性骨髓瘤成人患者,这是首款中国自主原创并在美国上市的CAR-T细胞治疗产品。此次获批是主要基于关键性临床Ib/II期CARTITUDE-1 (NCT03548207) 研究结果。
最新数据显示,西达基奥仑赛在既往接受过四线或者以上治疗(包括蛋白酶体抑制剂、免疫调节剂和抗CD38单克隆抗体)的复发或难治性多发性骨髓瘤患者中显示出高达98%的总缓解率。在关键的CARTITUDE-1 (NCT03548207) 研究中,97例R/R MM患者出现了早期、深度持久的缓解,总缓解率(ORR)高达98%(95%CI:92.7-99.7),78%的患者获得了严格的完全缓解(sCR,95%CI:68.8-86.1)。在18个月的中位随访时间中,中位缓解持续时间(DOR)为21.8个月(95% CI,21.8-无法预估)。

天济医药:全新机理外敷银屑病药物本维莫德
2022年5月24日,Dermavant Sciences宣布FDA已批准VTAMA(本维莫德,1%)乳膏上市,用于成人斑块型银屑病的局部治疗。本维莫德由国内企业天济医药研发、是具有自主知识产权的“first-in-class”首创新药。2012年,天济医药将本维莫德境外开发权授予GSK,合同首付款约2亿美元;2018年7月,GSK又以3.3亿美元的价格将本维莫德在中国境外的开发权出售给Dermavant公司。
早在2019年5月,本维莫德以“1类新药”在国内获批上市,用于适合局部治疗的成人轻至中度稳定性寻常型银屑病。这也是目前首款我国先批准上市之后才获美国FDA批准的创新药。

在两项关键性III期临床试验(PSOARING 1和PSOARING 2)中,与对照组相比,第12周时VTAMA乳膏在医师总体评估(PGA)评分“皮肤症状完全清除”(PGA=0)或“几乎完全清除”(PGA=1)方面表现出高度统计学显著改善,并且评分至少提高两级的患者比例显著高于对照组,达到试验的主要终点。同时,VTAMA乳膏也达到了所有关键次要终点,包括PASI75(银屑病面积与严重性指数评分改善75%)。
百奥泰:托珠单抗生物类似药
2023年9月29日,百奥泰/渤健宣布托珠单抗生物类似药(tocilizumab-bavi/BAT1806,商品名:Tofidence)获FDA批准上市,用于治疗中度至重度活动性类风湿关节炎、多关节幼年特发性关节炎和全身性幼年特发性关节炎。该产品为FDA批准的首款托珠单抗生物类似药。
TOFIDENCE是一款靶向白介素-6受体(IL-6R)的重组人源化单克隆抗体,可与可溶性及膜结合型IL-6 受体(sIL-6R 和 mIL-6R)特异性结合,并抑制由 sIL-6R 和 mIL-6R 介导的信号传导。
渤健对Tofidence的结构、物理化学和生物学特性进行了广泛的分析表征,并证明了其与原研托珠单抗(Actemra,罗氏)的生物相似性。此外,一项随机、双盲、单剂量、三臂、平行I期研究评估了Tofidence与托珠单抗在健康志愿者中的药代动力学、安全性和免疫原性;一项随机、双盲、多剂量、三臂、平行III期研究评估了Tofidence与托珠单抗在甲氨蝶呤控制不足的类风湿性关节炎患者中的疗效和药代动力学、安全性和免疫原性。这些数据皆表明Tofidence是托珠单抗的生物类似药。

根据罗氏2022年财报,托珠单抗的年销售额为27.01亿瑞士法郎(约28.30亿美元)。Tofidence成功在美上市,有望瓜分这一巨大市场。
君实生物:首款在美获批的国产PD-1产品特瑞普利单抗
2023年10月28日,Coherus BioSciences与君实生物宣布,美国FDA批准其单抗Loqtorzi(toripalimab,特瑞普利单抗)联合吉西他滨/顺铂作为晚期复发或转移性鼻咽癌(NPC)患者的一线治疗。其单药也获批用于复发或转移性鼻咽癌含铂治疗后的二线及以上治疗。特瑞普利单抗是首个FDA批准用以治疗鼻咽癌的PD-1单抗。

特瑞普利单抗(中文商品名:拓益)是一款以PD-1为靶点的单抗药物,其上市申请是基于JUPITER-02(一项随机、双盲、安慰剂对照、国际多中心3期临床研究)及POLARIS-02(一项多中心、开放标签、2期关键注册临床研究)的研究结果。在JUPITER-02临床3期研究中,与单独化疗相比,特瑞普利单抗联合化疗显著改善患者的无进展生存期(PFS),将疾病进展或死亡风险降低了48%。
该药物还显示总生存期(OS)出现具有统计学显著性和临床意义的改善,与单独化疗相比,特瑞普利单抗导致死亡风险降低37%。JUPITER-02研究结果于2021年6月在美国临床肿瘤学会(ASCO)年会的全体大会(#LBA2)上首次发表,随后作为《自然-医学》(Nature Medicine)2021年9月刊的封面文章发表。
POLARIS-02研究共纳入190例复发或转移性鼻咽癌患者接受特瑞普利单抗单药治疗,结果显示,在ITT人群中(N=190),客观缓解率(ORR)为20.5%,中位缓解持续时间(DOR)为12.8个月,中位总生存期(OS)为17.4个月;在92例既往接受过至少2线系统化疗失败的患者中,ORR为23.9%,中位缓解持续时间(mDOR)达到14.9个月,疾病控制率(DCR)为41.3%,中位总生存时间(mOS)达到15.1个月。2021年1月POLARIS-02研究在国际著名期刊《临床肿瘤学杂志》(Journal of Clinical Oncology,IF: 32.956)发表。

君实生物合作伙伴Coherus对特瑞普利单抗的销售表示乐观,认为鼻咽癌适应症在两年后能够达到销售额峰值2亿美元。抗PD-1单抗药物特瑞普利单抗治疗鼻咽癌获得了FDA的孤儿药(用于预防、治疗、诊断罕见病的药品)资格和突破性疗法认定,美国明年鼻咽癌新发病例约为2000例。
和黄医药:口服VEGFR1/2/3抑制剂呋喹替尼
2023年11月9日(美国时间11月8日)和黄医药宣布,其与合作伙伴武田共同开发的药物Fruzaqla(呋喹替尼/fruquintinib)在美国获批进入当地医药市场,用于治疗晚期结直肠癌。这是美国首个且唯一获批用于治疗经治转移性结直肠癌的,针对全部三种抗血管内皮生长因子(VEGF)受体的高选择性抑制剂。

FRUZAQLA(呋喹替尼)是一种选择性的口服VEGFR-1、-2及-3抑制剂。VEGFR抑制剂在抑制肿瘤的血管生成中起到至关重要的作用。FRUZAQLA被设计为拥有更高的激酶选择性,旨在降低脱靶激酶活性,从而实现更高的药物暴露、对靶点的持续覆盖以及当潜在作为联合疗法时拥有更高的灵活度。迄今为止,FRUZAQLA展示出可控的安全性特征,其与其他抗肿瘤疗法联合使用的研究正在进行中。
2007年,呋喹替尼在位于上海浦东张江的实验室首次合成最初的一个小分子结构,2018年在中国获批上市。今天,终于实现了在美国的成功上市!该药物于2020年1月纳入国家医保目录,目前市场已覆盖全国328个城市,超过3000家肿瘤医院。根据药融云全国医院销售数据,截至2023年上半年,该药物在院内累计销售超过10亿元人民币。资料显示,呋喹替尼在三线结直肠癌患者中的市场占有率达47%,惠及逾8万名结直肠癌患者。
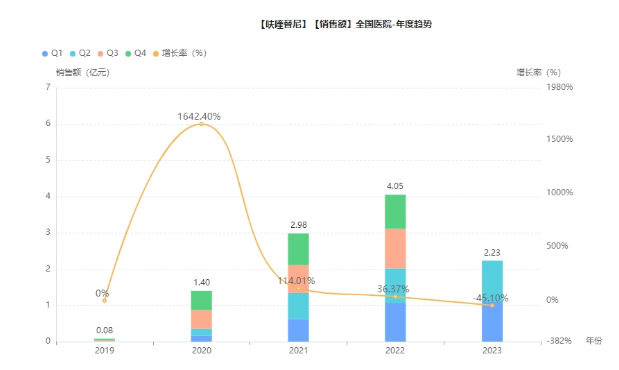
来源:药融云全国医院销售数据
FRUZAQLA的获批是基于两项大型III期临床试验的数据,包括:国际多中心临床试验FRESCO-2研究,其数据亦已于《柳叶刀 (The Lancet) 》上发表;以及于中国开展的FRESCO研究,其数据亦已于《美国医学会杂志 (JAMA) 》上发表。上述研究探索了FRUZAQLA联合最佳支持治疗对比安慰剂联合最佳支持治疗用于治疗经治转移性结直肠癌患者。FRESCO及FRESCO‑2研究均达到了其主要终点及关键次要终点,并在总共734名接受FRUZAQLA治疗的患者中展现出了一致的获益。各项研究的安全性特征亦保持一致。
FRESCO及FRESCO-2研究的数据亦支持了向欧洲药品管理局("EMA")提交的呋喹替尼上市许可申请,该申请已于2023年6月获确认及受理。此外,一项向日本医药品和医疗器械局("PMDA")的申请亦于2023年9月提交。期待呋喹替尼在欧洲和日本早日获批。
总结
美国市场是所有中国创新药企向往的“神圣之地”,究其原因在于中美医疗支出和创新药定价的差距,在美国等发达国家市场上市是创新药放量的关键。
2021年美国医疗费用支出达4.3万亿美元,中国医疗费用支出达1.1万亿美元,中美医疗费用支出的差距达3.9倍。而中美人均医疗支出差距更是明显,2021年美国人均医疗费用支出达1.3万美元,中国人均医疗费用支出达784美元,中美医疗支出差距达16.6倍。
<END>
要解锁更多企业药品研发信息吗?查询药融云数据库(vip.pharnexcloud.com/?zmt-mhwz)掌握药品各国上市情况、药品批文信息、销售情况与各维度分析、市场竞争格局、一致性评价情况、集采中标情况、药企申报审批信息、最新动态与前景等,以及帮助企业抉择可否投入时提供数据参考!注册立享15天免费试用!


















































 浙公网安备33011002015279
浙公网安备33011002015279 本网站未发布麻醉药品、精神药品、医疗用毒性药品、放射性药品、戒毒药品和医疗机构制剂的产品信息
本网站未发布麻醉药品、精神药品、医疗用毒性药品、放射性药品、戒毒药品和医疗机构制剂的产品信息
收藏
登录后参与评论
暂无评论