
医药工业和医疗装备产业是卫生健康事业的重要基础,事关人民群众生命健康和高质量发展全局。创新药研发创新难度大、周期长、投入高,这是新药研发的三大痛点,可谓来之不易。据药融云《全球在研新药与靶点月报》整理,9月全球在研创新药动态中,多家药企取得新进展,涉及迪哲、康方生物、泽璟制药、远大医药等众多药企。
1.《肿瘤学年鉴》发表!迪哲医药公布JAK1抑制剂研究成果
9月初,迪哲医药宣布,其自主研发的T细胞淋巴瘤领域高选择性JAK1抑制剂戈利昔替尼1期临床试验(JACKPOT8的A部分)研究成果发表于国际期刊《肿瘤学年鉴》(AnnalsofOncology)。
T细胞淋巴瘤(PTCL)是一种异质性强、侵袭性高的非霍奇金淋巴瘤(NHL),约占全球NHL的7%~10%。PTCL具有亚型多、易复发和预后差等特点,初治失败后的r/rPTCL预后极差,3年总体生存率仅为21%~28%,目前临床尚缺乏有效治疗方法。JAK/STAT信号通路在包括T细胞淋巴瘤在内的多种血液系统恶性肿瘤的发生发展中具有重要作用。
戈利昔替尼作为新一代、强效且高选择性JAK1抑制剂,通过靶向JAK/STAT通路能有效抑制肿瘤细胞生长与增殖。此外,该产品对JAK家族其它成员有200~400倍的选择性,有效地降低了由于脱靶导致的药物安全性风险。分析显示,戈利昔替尼单药显示出强效持久的抗肿瘤活性,客观缓解率(ORR)达44.3%,且其中一半以上肿瘤缓解的受试者达到了完全缓解(CR),CR率达23.9%。
据药融云数据库显示,戈利昔替尼新适应症:既往至少接受过一次标准治疗的复发或难治的外周T细胞淋巴瘤(r/rPTCL)成人患者,上市申请已受理,正在审评审评中(受理号:CXHS2300082)。
审评时间轴
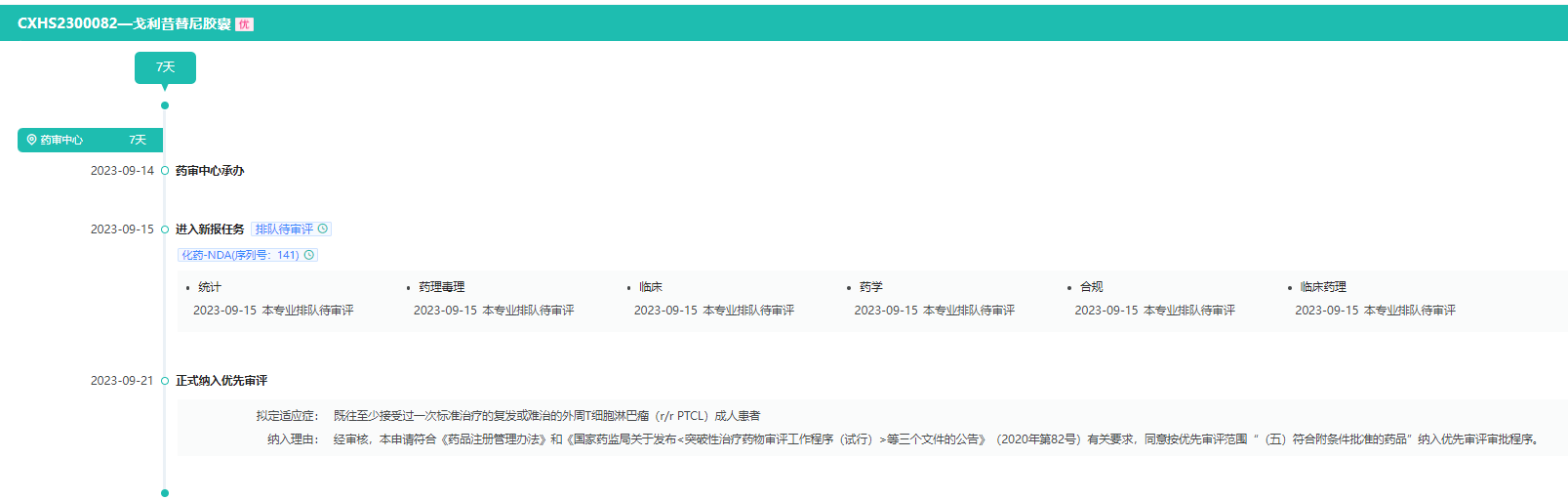
截图来源:药融云中国药品审评数据库
2.康方生物公布IL-4Rα单抗1期临床结果
9月中旬,康方生物宣布,其自主研发的新型人源化白介素-4受体α单克隆抗体AK120(IL-4Rα单抗)治疗中重度特应性皮炎(AD)的1期临床研究成果发表于《皮肤病学与治疗》(DematologyandTherapy)。
特应性皮炎(AD)是一种慢性、复发性和炎症性皮肤病,AD患者常合并过敏性皮炎、哮喘等其它特应性疾病,伴有剧烈瘙痒,严重影响生活质量,给患者及其家庭带来巨大且持久的经济和精神负担。
研究表明,Th2型炎症是特应性皮炎的基本特征,IL-4和IL-13是介导AD发病的重要细胞因子,主要由Th2细胞、嗜碱性粒细胞和2型固有淋巴样细胞等产生,在AD的发生发展中起着关键作用。
而IL-4Rα是促炎性细胞因子IL4、IL-13受体的共同亚基。AK120正是一款人源化IL-4Rα单克隆抗体,通过与IL-4Rα特异性结合以阻断IL-4与IL-13介导的信号通路,抑制相关免疫炎症反应的发生与发展。AK120有望选择性抑制Th2通路,从而预防或逆转AD的发展。分析显示,AK120可有效抑制IL-4/IL-13信号通路。
给药后生物标志物血清胸腺和活化调节趋化因子配体17(TARC/CCL17)和免疫球蛋白E(IgE)均较基线明显下降;健康受试者单次皮下给药和AD患者多次皮下给药后,AK120暴露量均呈近似剂量依赖性。剂量递增至最高600mg,各队列受试者均展现出良好的安全性和耐受性。
据药融云数据库显示,目前治疗特应性皮炎适应症,已上市的药品共有61种,葛兰素史克、辉瑞、赛诺菲、拜耳、诺华等药企均有布局。
治疗特应性皮炎药品数量TOP10公司
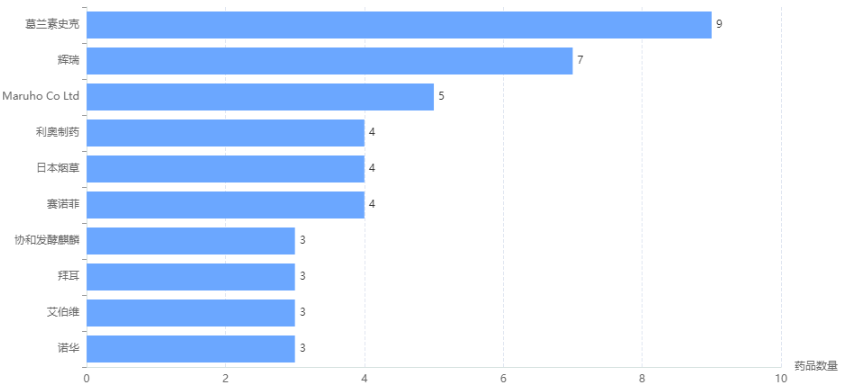
截图来源:药融云全球药物研发数据库
3.有望上市!泽璟制药「重组人促甲状腺激素」3期临床达主要终点
9月末,泽璟制药宣布其研发的注射用重组人促甲状腺激素(rhTSH)用于分化型甲状腺癌患者术后辅助诊断的3期临床试验ZGTSH004达到了方案预设的主要终点。
人促甲状腺激素基本信息
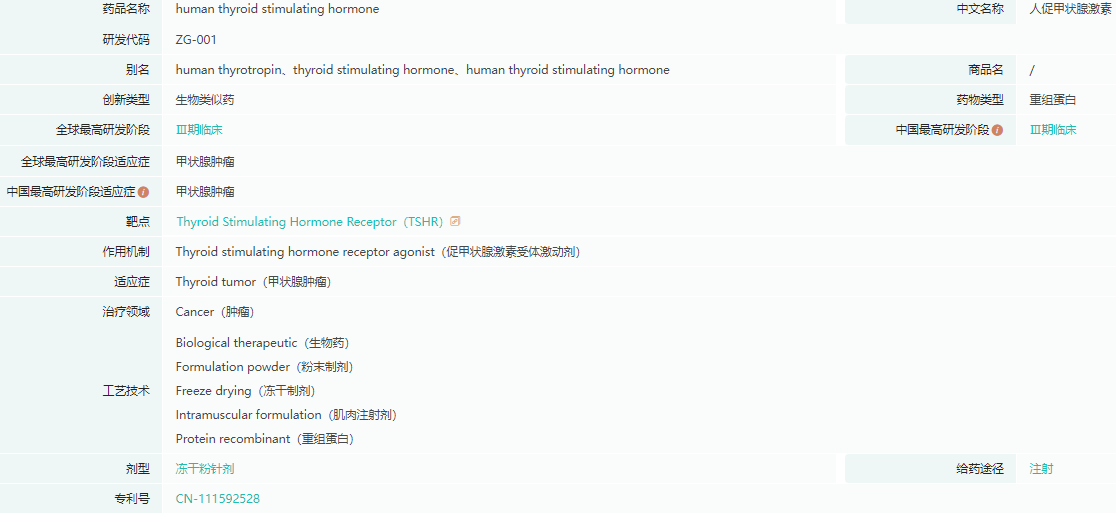
截图来源:药融云全球药物研发数据库
分化型甲状腺癌是甲状腺癌的主要亚型,约占甲状腺癌新发病例数约90%。近年来,由于早期诊断手段的进步和筛查加强,分化型甲状腺癌新发病例数快速增加。由于中国分化型甲状腺癌新发病例数的增长所带来的复查监测与辅助治疗的需求增加,未来分化型甲状腺癌术后辅助诊断及术后辅助治疗的需求将不断扩大。
注射用重组人促甲状腺激素(rhTSH)是泽璟制药研发的生物大分子药物,属于治疗用生物制品。人体内源性的促甲状腺激素是糖蛋白激素家族成员,主要在人垂体表达、分泌入血并和表达于甲状腺细胞和高分化的甲状腺癌细胞表面的促甲状腺素受体重组蛋白(hTSHR)蛋白结合,可刺激碘摄取和有机化,以及甲状腺球蛋白(Tg)、三碘甲状腺原氨酸(T3)和甲状腺素(T4)的合成和释放。此次达到主要终点的ZGTSH004试验是一项开放、单臂、自身对照、多中心的3期临床研究,在中国医学科学院北京协和医院、河南省肿瘤医院等研究中心开展。
试验主要目的为:评价分化型甲状腺癌术后辅助诊断131I全身显像(WBS)中,使用重组人促甲状腺激素处理的显像效果不劣于甲状腺激素撤除疗法(THW)。临床研究结果表明,试验的有效性和安全性结果符合预期,试验达到方案预设的主要终点。
4.针对过敏性鼻炎!远大医药创新鼻喷剂3期临床达主要终点
9月中旬,远大医药宣布,其创新产品Ryaltris复方鼻喷剂(GSP301NS)在中国开展的用于治疗12岁及以上患者的季节性过敏性鼻炎(SAR)的3期临床研究(GSP301-308)已完成并成功达到主要终点。
过敏性鼻炎(SAR)是一种常见的呼吸道疾病。中国是世界上过敏性鼻炎发病率较高的国家之一。根据中国相关流行病学调查结果,中国成人过敏性鼻炎患病率约17.6%,患病群体已近2.5亿人口,其中中重度持续性过敏性鼻炎患者约1.3亿,患者群体庞大。
据药融云药店零售数据库显示,2022年呼吸系统药物的销售额高达2744亿元,其中过敏性鼻炎治疗药物,近三年在零售药店的销售规模呈现量价齐升的良性增长态势。仅2022年第二季度过敏性鼻炎治疗药物的销售额就达到近40亿元,同比增长13.6%。
呼吸系统用药全国零售药店年度销售趋势
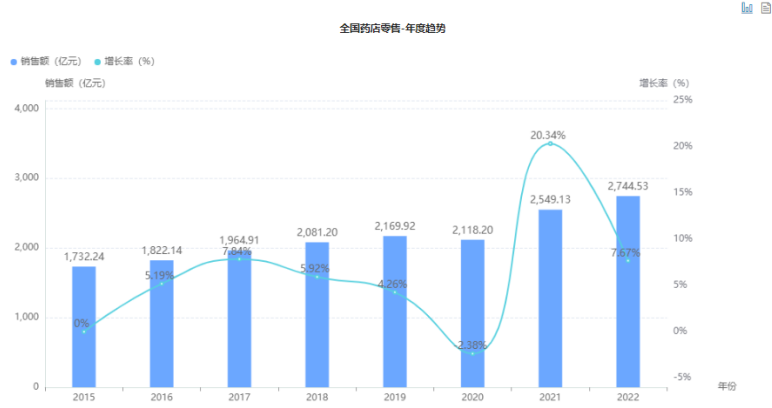
截图来源:药融云全国药店零售数据库
GSP301NS是一种新型的抗组胺药和皮质类固醇的复方鼻喷剂,用于治疗成人和青少年季节性过敏性鼻炎。作为复方制剂,GSP301NS能够给季节性过敏性鼻炎患者带来更为便捷的治疗方式,提高患者的依从性,为患者带来新的治疗手段。分析显示,GSP301NS组、盐酸奥洛他定鼻喷剂组和糠酸莫米松鼻喷剂组治疗14天期间受试者自评的上午和下午12小时rTNSS平均值较基线变化的最小二乘均值分别为-3.84、-2.58和-3.35。
由统计数据可见,GSP301NS组rTNSS下降幅度大于对照药治疗组,且组间差异有临床意义和统计学意义,证明GSP301NS的疗效评分均优于单方原研制剂。同时,该产品的安全性、耐受性及药代动力学特征也都达到了预设的临床终点。
<END>
以上仅是部分内容,想要获取9月《全球在研新药与靶点月报》全部内容,请关注“药融云”公众号,后台回复“报告”关键词进行领取;或者前往“药融云”数据库进行查询。

















































 浙公网安备33011002015279
浙公网安备33011002015279 本网站未发布麻醉药品、精神药品、医疗用毒性药品、放射性药品、戒毒药品和医疗机构制剂的产品信息
本网站未发布麻醉药品、精神药品、医疗用毒性药品、放射性药品、戒毒药品和医疗机构制剂的产品信息
收藏
登录后参与评论
暂无评论