
近日,华东医药股份有限公司全资子公司杭州中美华东制药有限公司(简称“中美华东”)收到国家药品监督管理局(NMPA)核准签发的《药物临床试验批准通知书》(通知书编号:2023LP01815、2023LP01816、2023LP01817),由中美华东申报的HDM1002片临床试验申请获得批准,适应症为超重或肥胖人群的体重管理。

HDM1002片是由杭州中美华东制药有限公司自主研发并拥有全球知识产权的1类化药新药,是具有口服活性、强效、高选择性的GLP-1受体小分子完全激动剂。临床前研究显示,HDM1002可强效激活GLP-1受体,诱导环磷酸腺苷(cAMP)产生,具有强效的改善糖耐受、降糖和减重作用并且显示出良好的安全性。
2023年5月,HDM1002片用于治疗成人2型糖尿病的临床试验申请,先后获得NMPA和美国FDA批准。2023年6月,中美华东完成向CDE递交HDM1002片的临床试验申请,并于近日获得NMPA批准,同意本品在成人超重/肥胖患者中开展临床试验。
在肥胖或体重超重患者治疗领域领域,华东医药现有产品奥利司他胶囊为处方药(卡优平)和OTC(健姿)双跨产品,通过近年来国内市场销售和推广,已积累一定的学术推广基础和市场资源。2023年6月30日,由中美华东申报的利拉鲁肽注射液肥胖或超重适应症的上市许可申请获得批准,为中国大陆第一款获批的GLP-1类减肥药物,将满足更多肥胖和超重患者的用药选择。
关于华东医药
华东医药股份有限公司(证券代码:000963)于1999年上市,公司业务覆盖医药全产业链,以医药工业为主导,同时拓展医药商业、医美产业和工业微生物业务,已发展成为集医药研发、生产、经销为一体的大型综合性医药上市公司。
研发管线(部分)
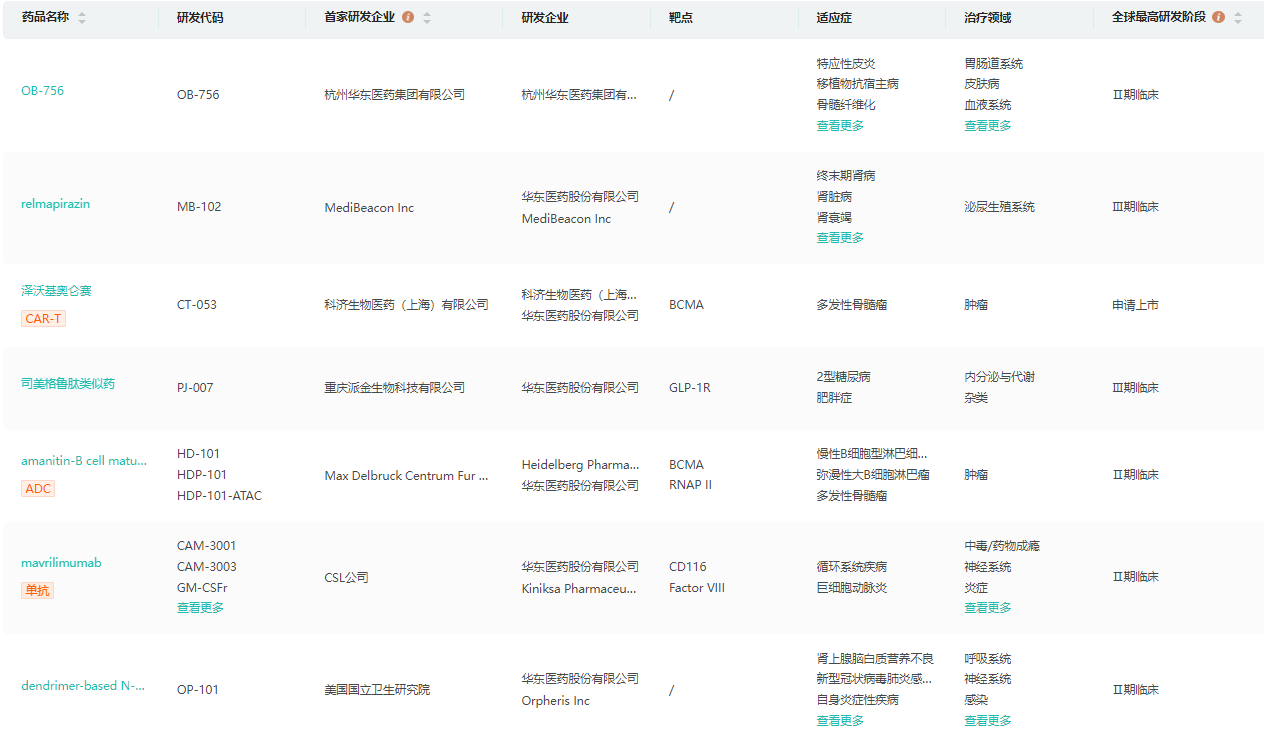
截图来源:药融云全球药物研发数据库
参考资料:
1.公司官网
2.药融云数据库
<END>
要解锁更多企业药品研发信息吗?查询药融云数据库(vip.pharnexcloud.com/?zmt-mhwz)掌握药品各国上市情况、药品批文信息、销售情况与各维度分析、市场竞争格局、一致性评价情况、集采中标情况、药企申报审批信息、最新动态与前景等,以及帮助企业抉择可否投入时提供数据参考!注册立享15天免费试用!



































![医药高地:核药!恒瑞医药镥[177Lu]氧奥曲肽注射液获批临床](https://oss-personal-public.bcpmdata.com/images/covers/202302/09/e3938ad9f1d23e2fd043611c4a98c02a.png)



















 川公网安备51019002008863号
川公网安备51019002008863号 本网站未发布麻醉药品、精神药品、医疗用毒性药品、放射性药品、戒毒药品和医疗机构制剂的产品信息
本网站未发布麻醉药品、精神药品、医疗用毒性药品、放射性药品、戒毒药品和医疗机构制剂的产品信息
收藏
登录后参与评论
暂无评论