
据药融云《全球在研新药与靶点月报》数据统计,2023年8月共有119个化药1类新药受理号获CDE承办(含补充申请30个),其中国产78个,进口11个;从申请类型来看,包括临床申请83个,上市申请6个,涉及58个品种,63家企业。
8月共有82个1类治疗用生物制品受理号获CDE承办(含补充申请24个),其中国产50个,进口8个,从申请类型来看,包括临床申请51个,上市申请7个,涉及72个品种,75家企业。与此同时,还有3个1类中药受理号获CDE承办,从申请类型来看,全部为临床申请,涉及2个品种,2家企业。
8月,共有99款新药获批临床(共计168个受理号),其中包括47款化药,49款生物制品,3款中药;其中获批临床的3款1类中药,分别是成都马甲子生物的马甲子胶囊、康缘药业的乌鳖还闺颗粒、中国中医科学院西苑医院的麻荆宣肺颗粒。
2023年8月国内获批临床新药一览表(部分)
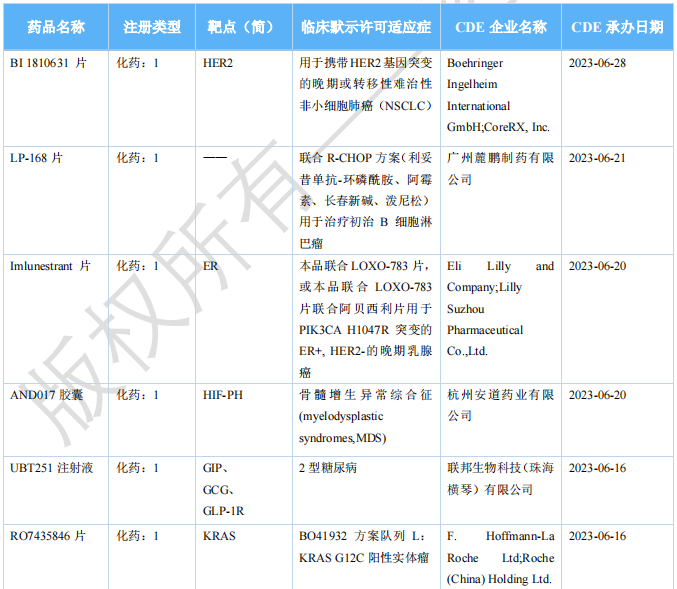
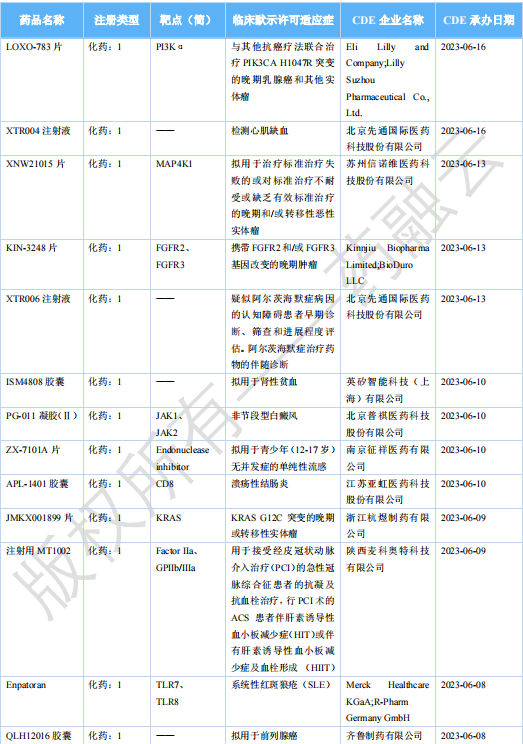
图片来源:药融云《全球在研新药与靶点月报》
同时,本月有4款新药获批上市,包括烨辉医药的甲磺酸贝舒地尔片(商品名:乐舒克)、信达生物的托莱西单抗注射液(商品名:信必乐)、迪哲医药的舒沃替尼片(商品名:舒沃哲)、诺华的英克司兰钠注射液(商品名:乐可为)。
1. 甲磺酸贝舒地尔片——全球首款ROCK2抑制剂
烨辉医药的甲磺酸贝舒地尔片在国内获批上市,用于治疗对糖皮质激素或其他系统治疗应答不充分的12岁及以上慢性移植物抗宿主病(cGVHD)患者。
甲磺酸贝舒地尔片(Belumosudil)是由Kadmon Holdings公司开发的一款ROCK2激酶抑制剂,ROCK2介导的信号通路在调节炎症和纤维化反应中具有重要作用。Belumosudil能通过减轻STAT3的磷酸化,加强STAT5的磷酸化,从而下调过度活化的T辅助细胞(Th17),并增强调节性T细胞(Treg)功能,进而重建免疫平衡。
甲磺酸贝舒地尔片获批进口-耗时616天
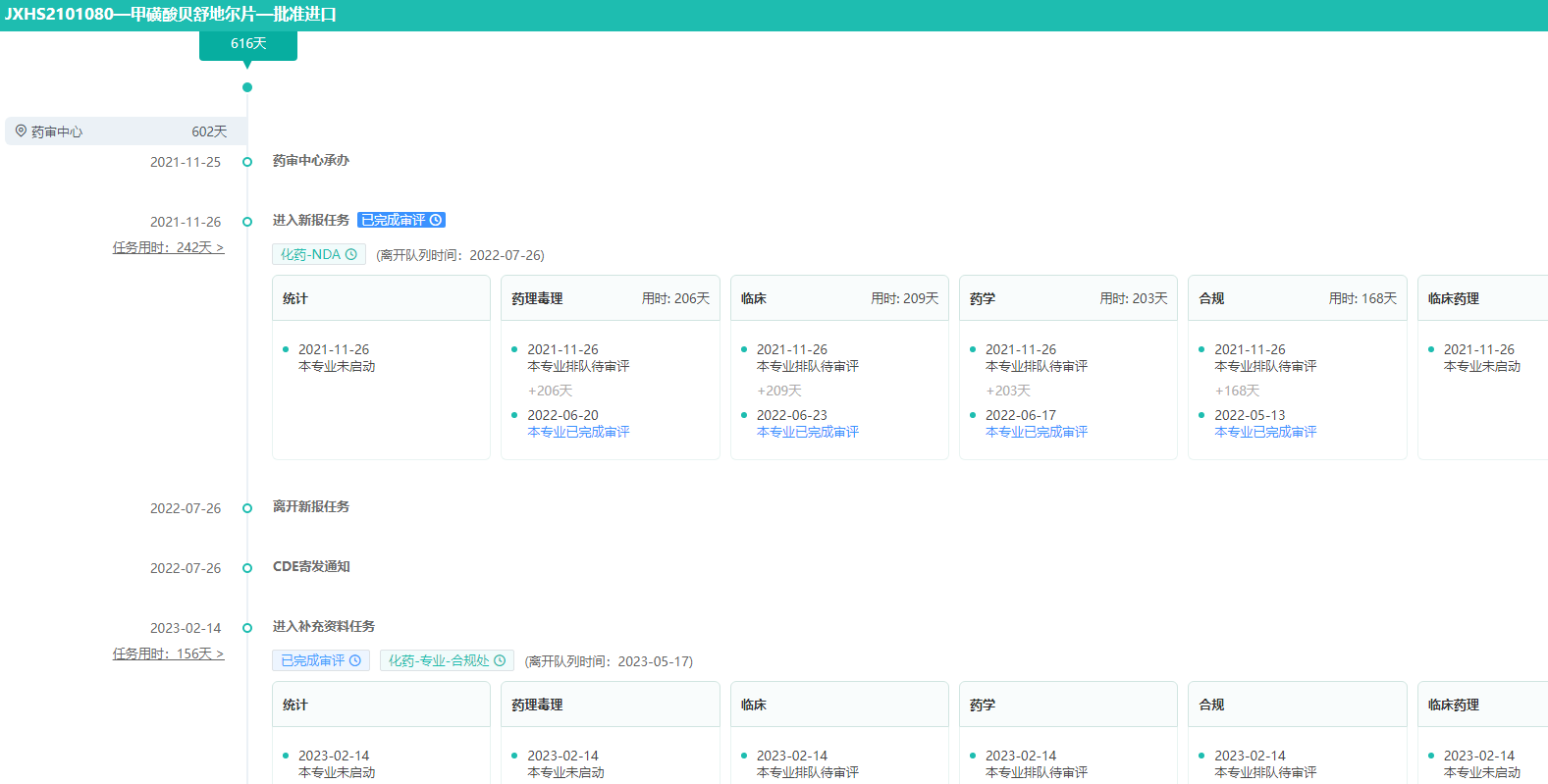
图片来源:药融云中国药品审评数据库
2019年,烨辉医药与Kadmon Holdings达成战略合作,成立合资公司BK Pharmaceuticals在中国开发和商业化belumosudil用于治疗GVHD。
药融云全球药物研发数据库显示,贝舒地尔(Belumosudil)由于治疗效果显著,2017年10月,被FDA授予孤儿药资格;2019年10月,又纳入突破性治疗品种;2020年8月,FDA将其纳入实时肿瘤学审评(RTOR)项目;同年11月,FDA 受理了 Belumosudil 的新药上市申请(NDA)并授予其优先审评资格,并于2021年7月正式批准Belumosudil上市,用于治疗12岁以上的cGVHD患者,是首款获FDA批准的ROCK2抑制剂。2021年9月,赛诺菲以约19亿美元收购了Kadmon。
目前,国内其他ROCK相关在研药物还包括华润医药的NIP292(I期临床)、中国生物制药的TDI01(II期临床)、正大天晴药业的TQ-05105(II期临床)等,相信这些ROCK抑制剂类药物未来为我国cGVHD、SSc、IPF以及其他难治性疾病患者带来更多的临床获益。
TDI01全球研发详情查询
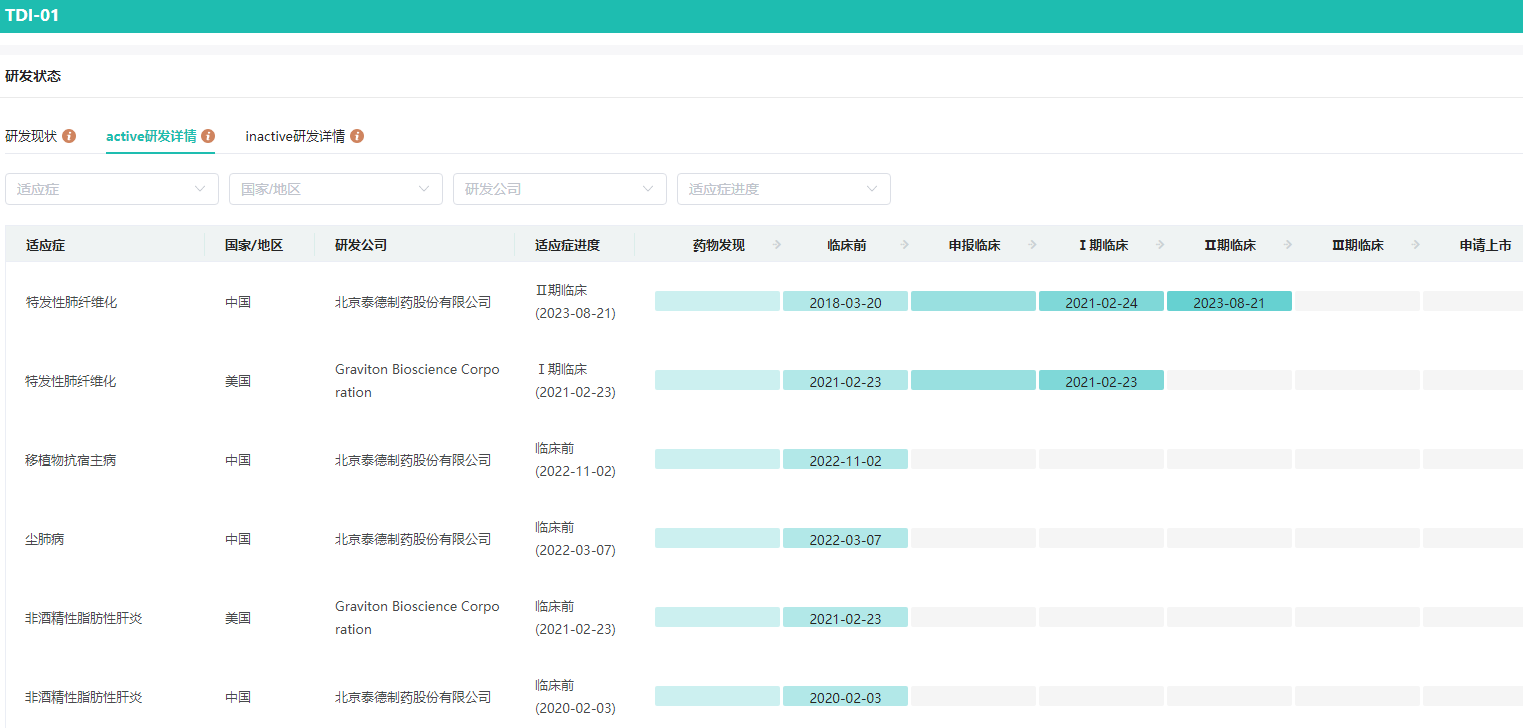
图片来源:药融云全球药物研发数据库
2. 托莱西单抗注射液——首个国产PCSK-9降脂新药
信达生物的托莱西单抗注射液获批上市,是首个国产PCSK-9抑制剂,获批适应症为:在控制饮食的基础上,与他汀类药物、或者与他汀类药物及其他降脂疗法联合用药,用于在接受中等剂量或中等剂量以上他汀类药物治疗,仍无法达到低密度脂蛋白胆固醇(LDL-C)目标的原发性高胆固醇血症(包括杂合子型家族性和非家族性高胆固醇血症)和混合型血脂异常的成人患者。
托莱西单抗注射液是信达生物自主研发的一款前蛋白转化酶枯草溶菌素9(PCSK9)抑制剂,通过抑制PCSK9,阻断血浆PCSK9与低密度脂蛋白受体(LDLR)的结合,进而阻止LDLR的内吞和降解,增加细胞表面LDLR表达水平和数量,增加LDLR对低密度脂蛋白胆固醇(LDL-C)的重摄取,降低循环LDL-C水平,最终达到降低血脂的目的。
药融云数据库显示,信达生物目前已有9个产品在国内获批上市,包括托莱西单抗(商品名:信必乐)、信迪利单抗注射液(商品名:达伯舒)、贝伐珠单抗生物类似药(商品名:达攸同)、阿达木单抗生物类似药(商品名:苏立信)、利妥昔单抗生物类似药(商品名:达伯华)、佩米替尼片(商品名:达伯坦)、塞普替尼(商品名:睿妥)、奥雷巴替尼(商品名:耐立克)、雷莫西尤单抗(商品名:希冉择)。
信达生物研发管线——研发阶段分布
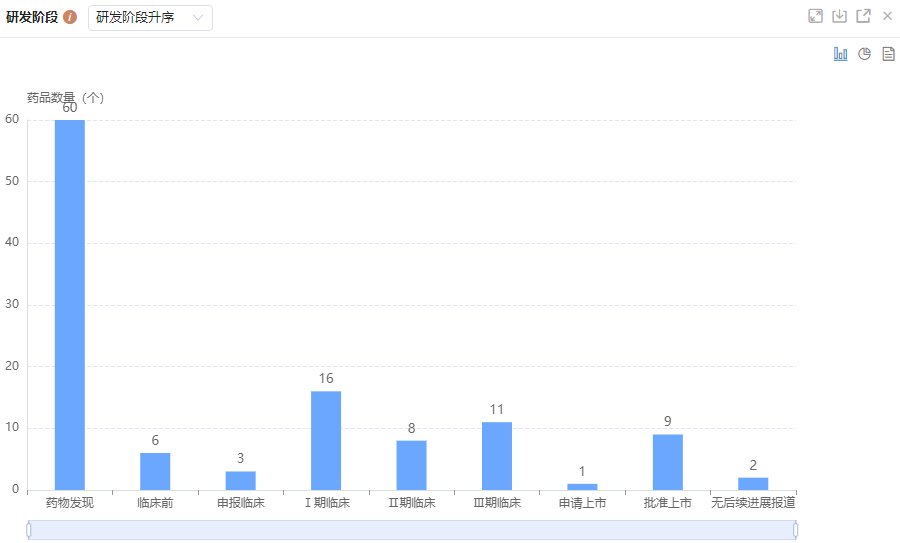
图片来源:药融云全球药物研发数据库
截至目前,国内有4款PCSK9靶向药物获批上市,分别是安进的单抗Repatha(Evolocumab,依洛尤单抗)、赛诺菲/再生元的单抗Praluent(Alirocumab,阿利西尤单抗)以及诺华的siRNA药物Leqvio(inclisiran),以及信达生物/礼来的托莱西单抗(tafolecimab,IBI-306)。信达的国产PCSK9单抗获批上市,将有助于打破进口垄断,同时惠及中国高胆固醇血症患者。
君实生物的昂戈瑞西单抗是第二款申报上市的国产PCSK-9抑制剂,2023年4月,昂戈瑞西单抗用于治疗原发性高胆固醇血症(包括杂合子型家族性和非家族性)和混合型血脂异常,以及用于成人或12岁以上青少年的纯合子型家族性高胆固醇血症的两项适应症上市申请获CDE受理。
除此之外,我国还有多家药企布局PCSK9靶点,如君实生物的昂戈瑞西单抗,是第二款申报上市的国产PCSK-9抑制剂;以及恒瑞医药的SHR-1209也已进入申请上市阶段;还有天广实生物、天士力生物、信立泰、瑞博生物也纷纷布局,其中信立泰已有两款PCSK9靶向药进入临床。
3. 舒沃替尼片——国创首款!潜在同类最佳肺癌靶向药
NMPA附条件批准迪哲医药的1类创新药舒沃替尼片(商品名:舒沃哲)上市,用于既往经含铂化疗治疗时或治疗后出现疾病进展,或不耐受含铂化疗,并且经检测确认存在表皮生长因子受体(EGFR)20号外显子插入突变的局部晚期或转移性非小细胞肺癌(NSCLC)的成人患者。
药融云数据库显示,此前舒沃替尼片已被中国纳入优先审评审批并获得突破性疗法。舒沃替尼是迄今为止肺癌领域首个且唯一获中美双“突破性疗法认定”的国创新药,也是首个获上市受理的、针对EGFR exon20ins突变型晚期NSCLC 的中国原研创新药。
舒沃替尼片批文信息
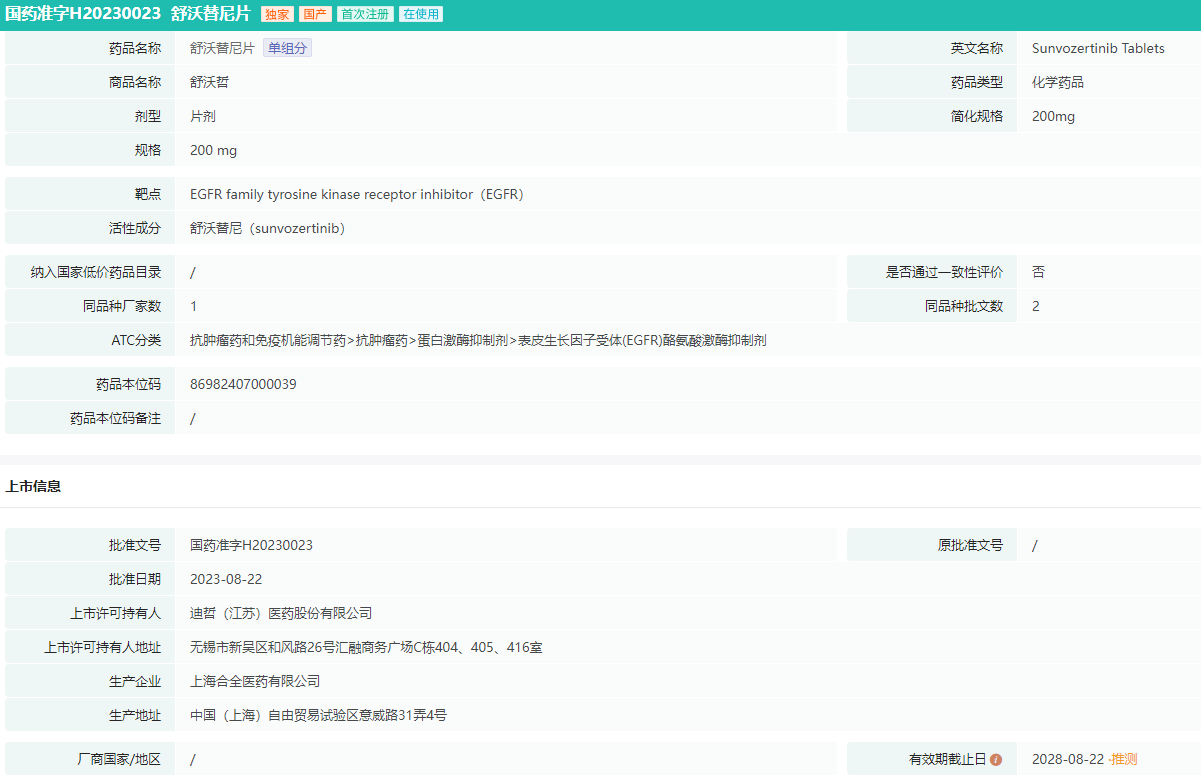
图片来源:药融云中国药品批文数据库
舒沃替尼是一款口服、不可逆、针对多种EGFR突变亚型的高选择性EGFR酪氨酸激酶抑制剂(TKI),临床研究证实,这款药物对约 30 种 EGFR 外显子 20 插入亚型,无论突变位置如何,都具有抗肿瘤活性!希望这款国创新药早日造福更多国内的肺癌患者。
4. 英克司兰钠注射液——全球首创siRNA降胆固醇药物
诺华的小干扰RNA降胆固醇药物英克司兰钠注射液(Inclisiran注射液)在国内获批上市,作为饮食的辅助疗法,用于成人原发性高胆固醇血症(杂合子型家族性和非家族性)或混合性血脂异常患者的治疗。
inclisiran是一款靶向PCSK9的小干扰核酸(siRNA)疗法,inclisiran可直接与编码PCSK9蛋白的mRNA结合,通过RNA干扰作用降低mRNA的水平,从而防止肝脏生成PCSK9蛋白,每年进行两次Inclisiran注射即可降低低密度脂蛋白胆固醇(LDL-C),是一款长效降脂siRNA疗法。
2021年12月,Inclisiran注射液在美国获FDA批准上市,用于治疗接受最高耐受剂量他汀疗法后,仍存在高水平低密度脂蛋白胆固醇(LDL-C)的成人患者。Inclisiran注射液是FDA批准的首款也是唯一一款用于降低LDL-C的siRNA药物。
<END>
想要获取药融云8月《全球在研新药与靶点月报》的全部内容,可以关注“药融云”公众号,后台回复“报告”关键词进行领取。























































 川公网安备51019002008863号
川公网安备51019002008863号 本网站未发布麻醉药品、精神药品、医疗用毒性药品、放射性药品、戒毒药品和医疗机构制剂的产品信息
本网站未发布麻醉药品、精神药品、医疗用毒性药品、放射性药品、戒毒药品和医疗机构制剂的产品信息
收藏
登录后参与评论
暂无评论