
据药融云数据库,近日先声药业与瑞士Idorsia公司合作的新型抗失眠药物盐酸Daridorexant片启动临床,为评估Daridorexant在健康受试者中单次和多次口服给药的药代动力学特征、安全性和耐受性的单中心、随机、双盲、安慰剂对照的Ⅰ期临床研究。

截图来源:药融云中国临床试验数据库
此外,先声药业还有还有SIM0801(治疗阿尔兹海默症)、SIM0800(治疗脑卒中伴发脑水肿)、SIM0802(治疗缺血性脑卒中等)等药物正在研发中,其在神经系统领域的优势进一步凸显。
Daridorexant:可长期用药
Daridorexant是一种双重食欲素受体拮抗剂(DORA),可阻断促进觉醒的食欲素神经肽(食欲素A和食欲素B)与其受体结合,与与传统失眠药物(如苯二氮䓬类药物)通过镇静大脑来促进睡眠不同,Daridorexant仅阻断食欲素神经肽对食欲素受体的激活。因此,Daridorexant减少唤醒驱动,诱导睡眠发生,而不改变睡眠结构,且没有次日残留效应。
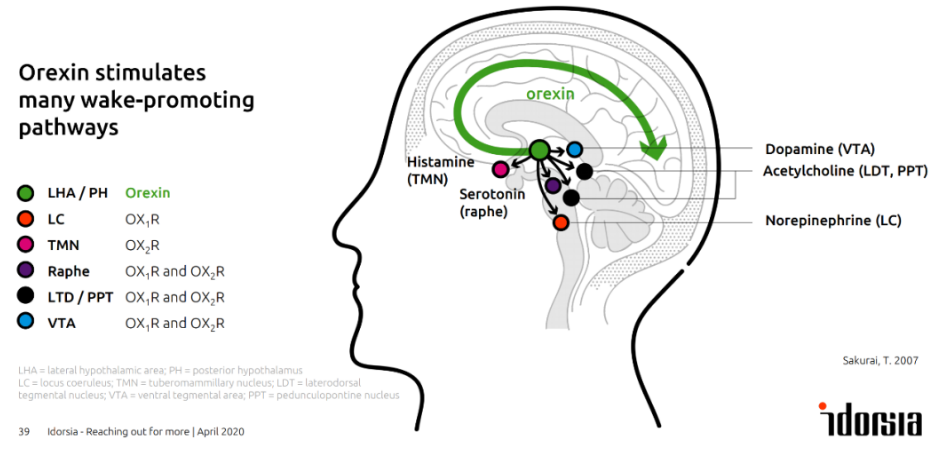
图片来源:Idorsia官网
Daridorexant的III期临床数据已于《柳叶刀神经病学》发表:主要研究表明,在治疗的第1个月及第3个月,Daridorexant较安慰剂显著改善了入睡、睡眠维持,及自我报告的总睡眠时间,并且不改变睡眠结构。此外,研究还表明Daridorexant安全耐受性良好,未发现依赖性、反跳性失眠、戒断症状和药物滥用证据,显著区分于苯二氮䓬受体激动剂所报告的结果。Daridorexant已获得长达12个月持续治疗的临床数据,结果支持Daridorexant可以长期用药。
Daridorexant除可改善慢性失眠障碍成年人群的夜间睡眠外,还可改善患者的日间功能,是唯一一款获得欧洲药品监督管理局(EMA)批准的改善日间功能的DORA类失眠药物。目前,Daridorexant已于美国、英国、意大利、德国、瑞士、加拿大获批上市。
2022年11月15日,先声药业与Idorsia订立独家授权协议,获得授Daridorexant在大中华地区的开发及商业化的独家权利。Idorsia公司将获得3000万美元的首付款,并有资格在中国注册获批后获得2000万美元额外里程碑付款等。2023年7月,该药在国内获批临床,拟用于治疗症状持续存在至少3个月且对日间功能产生影响的成人失眠患者。
国内暂无同类药物上市
苏沃雷生是全球首个上市的食欲素受体拮抗剂,通过增加患者睡意促进患者入眠,增加患者的睡眠质量。今年4月,根据《麻醉药品和精神药品管理条例》有关规定,国家药品监督管理局、公安部、国家卫生健康委员会决定将6类药品列入麻醉药品和精神药品目录,其中便包括了苏沃雷生,被列入第二类精神药品目录。
苏沃雷生暂时仅有原研药上市,全球范围内只在美国和日本两个国家进行上市销售。查询国内苏沃雷生相关情况了解到,默沙东在国内申请了苏沃雷生相关的药物专利,预计于2027年过期;申请了苏沃雷生制剂专利,预计2033年过期。
在国内原研药物专利仍处于有效期的情况下,天津天药药业提交了苏沃雷生中间体专利申请和仿制药上市申请(获批临床默示许可)。目前天药药业的专利申请处于实审中,出于商业原因,苏沃雷生的BE试验已主动暂停。
先声药业:超60项管线推进,神经系统领域优势凸显
在神经系统领域,先声药业的依达拉奉右莰醇注射用浓溶液(商品名:先必新)作为脑卒中治疗领域的重磅创新药,2022年院内销售额大涨117.6%,突破20亿元大关;2023上半年已经惠及患者约56万人,同比增长33%,覆盖超4200家医疗机构,占据超过22%的卒中注射液市场份额。
目前,先必新填补脑出血(ICH)治疗空白的新适应症开发已完成Ⅱ期临床首例患者入组(登记号:CTR20231571),先必新舌下片新药上市申请(NDA)获受理(受理号:CXHS2300058),先必新系列产品将有望应用于卒中全程治疗,覆盖从入院前急救、缺血性/出血性卒中治疗及卒中后认知障碍改善整个过程。此外,还有SIM0801(治疗阿尔兹海默症)、SIM0800(治疗脑卒中伴发脑水肿)、SIM0802(治疗缺血性脑卒中等)等药物正在研发中。
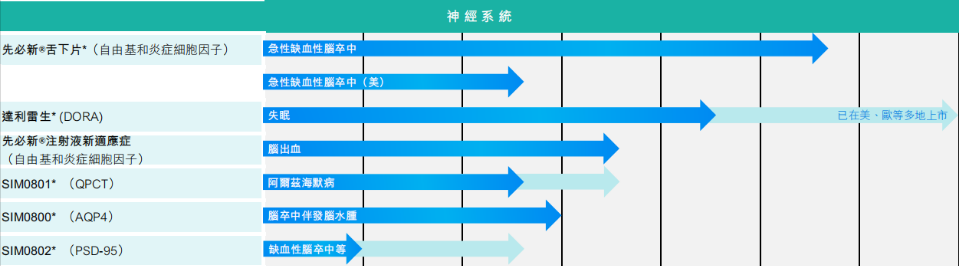
截图来源:企业财报
据先声药业2023年度中期业绩公告,目前先声药业已拥有创新药研发管线超60项,通过对研发和BD的有效投入,晚期管线不断充实。公告期内,先声共新增新药上市申请(NDA)3项,3项新分子新药临床试验申请(IND)获受理,临床项目入组受试者超640例,管线进展持续提速。
在公告披露的处于NDA/关键临床阶段的候选药物中,先必新舌下片、CMAB009(有望成为首个国内上市的用于mCRC治疗的国产抗EGFR单克隆抗体药物)、苏维西塔单抗(新一代重组人源化抗血管内皮生长因子单克隆抗体)、最佳机制失眠药达利雷生(Daridorexant)等众多高潜创新药,均将有助于先声药业的创新药收入再创新高。
先声药业其他领域在研药品

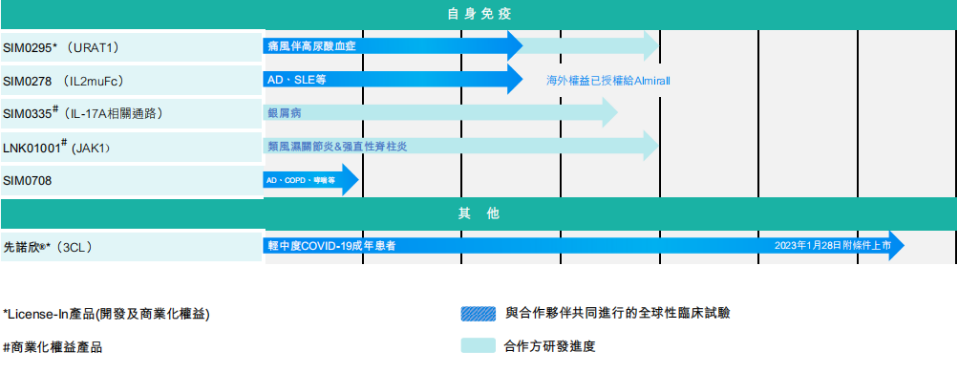
截图来源:企业财报
<END>
要解锁更多企业药品研发信息吗?查询药融云数据库(vip.pharnexcloud.com/?zmt-mhwz)掌握药品各国上市情况、药品批文信息、销售情况与各维度分析、市场竞争格局、一致性评价情况、集采中标情况、药企申报审批信息、最新动态与前景等,以及帮助企业抉择可否投入时提供数据参考!注册立享15天免费试用!



































![医药高地:核药!恒瑞医药镥[177Lu]氧奥曲肽注射液获批临床](https://oss-personal-public.bcpmdata.com/images/covers/202302/09/e3938ad9f1d23e2fd043611c4a98c02a.png)


















 川公网安备51019002008863号
川公网安备51019002008863号 本网站未发布麻醉药品、精神药品、医疗用毒性药品、放射性药品、戒毒药品和医疗机构制剂的产品信息
本网站未发布麻醉药品、精神药品、医疗用毒性药品、放射性药品、戒毒药品和医疗机构制剂的产品信息
收藏
登录后参与评论
暂无评论