
8月16日,华东医药发布2023年半年度报告,上半年公司实现营业收入203.85亿元,同比增长12.02%;实现归属于上市公司股东的扣除非经常性损益的净利润 14.27 亿元,同比增长 12.24 %。
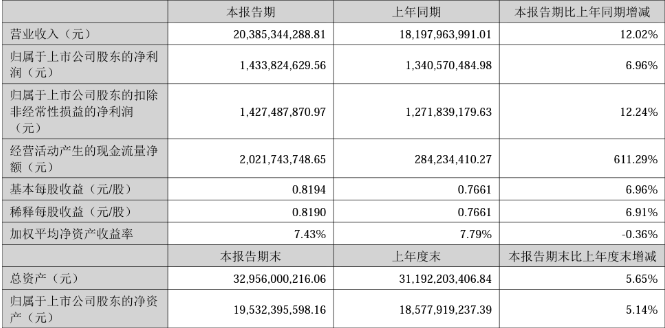
核心子公司中美华东报告期内整体经营继续保持积极增长趋势,实现营业收入(含CSO 业务)60.54 亿元,同比增长 10.04%,实现合并扣非归母净利润 12.26亿元,同比增长15.11%,净资产收益率12.38%。
管线及研发投入方面,报告期内,华东医药在研项目合计82个,其中创新产品及生物类似药项目51个。报告期内公司医药工业研发投入10.57亿元;其中直接研发支出6.68亿元,同比增长15.91%。
其中:
华东医药自主研发的口服小分子GLP-1受体激动剂HDM1002糖尿病适应症已于2023年5月首获中美双IND批准,并于2023年6月初实现首次人体试验(FIH)首例受试者用药。肥胖适应症的中国IND申请已于2023年6月递交。
HDM1002研发进度查询
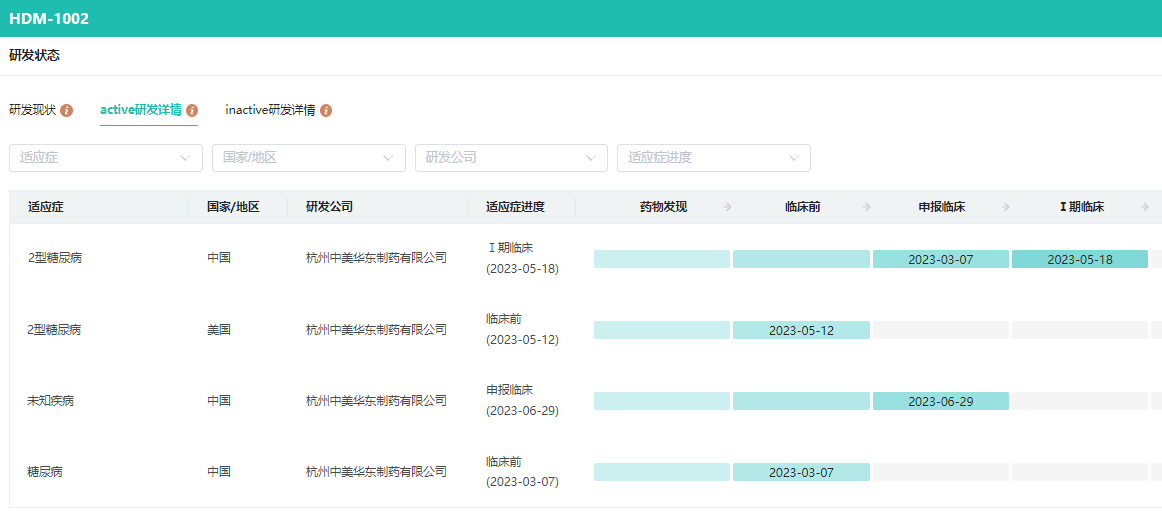
截图来源:药融云全球药物研发数据库
公司自主研发的 GLP-1R/GIPR 双靶点长效多肽类激动剂 HDM1005 已进入 IND 研究 阶段,目前项目推进顺利,预计2024年初递交IND申请。
控股子公司道尔生物在研的 GLP-1R/GCGR/FGF21R 靶点的多重激动剂 DR10624 于 2023 年 7月在新西兰完成了治疗肥胖症的I期多次递增剂量给药(MAD)临床试验的首例 受试者给药。DR10624用于超重或肥胖人群的体重管理的中国 IND申请已于 2023年 7月 获批,糖尿病适应症的中国 IND申请已于 2023年 6月递交,重度高甘油三酯血症适应症 的中国IND已于2023年8月递交。
利拉鲁肽注射液糖尿病适应症已于2023年 3月获得 NMPA批准上市,肥胖或超重适应症已于2023年6月获得NMPA批准上市。
司美格鲁肽注射液目前已完成 I期临床并达到等效性研究终点,Ⅲ期临床研究工作已启动。
德谷胰岛素注射液目前已完成 I期临床并达到等效性研究终点,Ⅲ期临床研究工作已启动。
<END>
要解锁更多企业药品研发信息吗?查询药融云数据库(vip.pharnexcloud.com/?zmt-mhwz)掌握药品各国上市情况、药品批文信息、销售情况与各维度分析、市场竞争格局、一致性评价情况、集采中标情况、药企申报审批信息、最新动态与前景等,以及帮助企业抉择可否投入时提供数据参考!注册立享15天免费试用!























































 川公网安备51019002008863号
川公网安备51019002008863号 本网站未发布麻醉药品、精神药品、医疗用毒性药品、放射性药品、戒毒药品和医疗机构制剂的产品信息
本网站未发布麻醉药品、精神药品、医疗用毒性药品、放射性药品、戒毒药品和医疗机构制剂的产品信息
收藏
登录后参与评论
暂无评论