 近日,武田在2023第一季度财报中表示,其已经在美国、欧洲和中国上市的治疗肺癌产品Exkivity的一项一线治疗晚期非小细胞肺癌的III期临床试验(EXCLAIM-2)因为无疗效获益而终止。公司正在与监管机构就这些数据进行讨论,并将决定下一步的行动。
近日,武田在2023第一季度财报中表示,其已经在美国、欧洲和中国上市的治疗肺癌产品Exkivity的一项一线治疗晚期非小细胞肺癌的III期临床试验(EXCLAIM-2)因为无疗效获益而终止。公司正在与监管机构就这些数据进行讨论,并将决定下一步的行动。

Exkivity是武田研发的一种新型、高选择性靶向于EGFR和人表皮生长因子受体2(HER2)20号外显子插入突变的小分子酪氨酸激酶抑制剂(TKI)。

EXCLAIM-2(NCT04129502)是一项国际多中心、开放标签、随机对照III期临床试验,主要研究终点BRIC评估的PFS。计划入组318例患者。EXCLAIM-2临床研究的阴性结果将让EXKIVITY失去获得一线治疗EGFR Exon 20in突变阳性NSCLC患者适应症的机会。
NCT04129502试验结果详情

截图来源:药融云全球临床试验数据库
武田2023Q1总收入为1.059万亿日元(约为75亿美元,按最新汇率1 日元 ≈ 0.0071 美元计算),同比增长8.9%。这主要归功于日元疲软以及除肿瘤学以外的关键业务领域的增长。
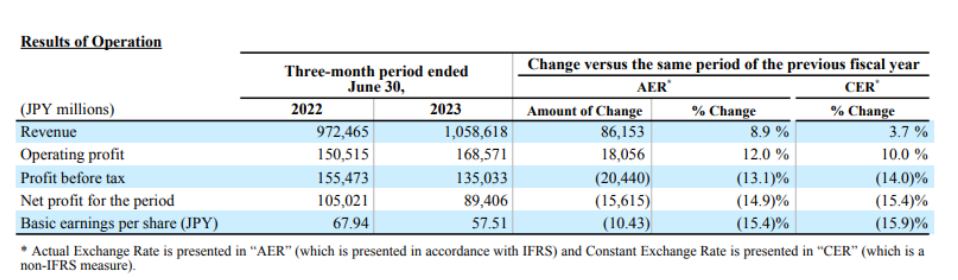
根据财报,武田预计Exkivity的最高销售额将达到3亿至6亿美元。在截至今年3月的12个月里,这款EGFR抑制剂的销售额为2,600万美元(1.86亿人民币,按最新汇率1.00 美元 =7.17 人民币)。武田曾表示,Exkivity和强生的Rybrevant平分了二线市场。
此前,强生宣布其Rybrevant已经成功地延缓了一线NSCLC患者的癌症进展。两种药物均利用单组试验的肿瘤缩小数据,于2021年获得FDA加速批准,用于有EGFR外显子20插入突变的NSCLC的二线治疗。
武田设计的Exclaim-2与Rybrevant的PAPILLON试验不同。武田将Exkivity作为单一药物在一线进行测试,而强生则将Rybrevant与化疗联合使用。
参考资料:
1.武田官网
2.药融云数据库
要解锁更多企业药品研发信息吗?查询药融云数据库(vip.pharnexcloud.com/?zmt-mhwz)掌握药品各国上市情况、药品批文信息、销售情况与各维度分析、市场竞争格局、一致性评价情况、集采中标情况、药企申报审批信息、最新动态与前景等,以及帮助企业抉择可否投入时提供数据参考!注册立享15天免费试用!























































 川公网安备51019002008863号
川公网安备51019002008863号 本网站未发布麻醉药品、精神药品、医疗用毒性药品、放射性药品、戒毒药品和医疗机构制剂的产品信息
本网站未发布麻醉药品、精神药品、医疗用毒性药品、放射性药品、戒毒药品和医疗机构制剂的产品信息
收藏
登录后参与评论
暂无评论