2023年6月23日-26日,美国糖尿病协会第83届年会科学会议(ADA2023)召开,本次会议上多家国内外企业公布了其GLP-1类药物的最新减重相关临床数据。其中,先为达公布了GLP-1受体激动剂Ecnoglutide(XW003)的最新临床数据、礼来公布了小分子GLP-1R激动剂Orforglipron的最新临床数据、勃林格殷格翰公布了GLP-1R/GCGR双靶点激动剂Survodutide的最新临床数据。目前国内在研减肥药进展较快的企业有华东医药、仁会生物、诺和诺德、礼来等。
图:国内部分在研减重药物
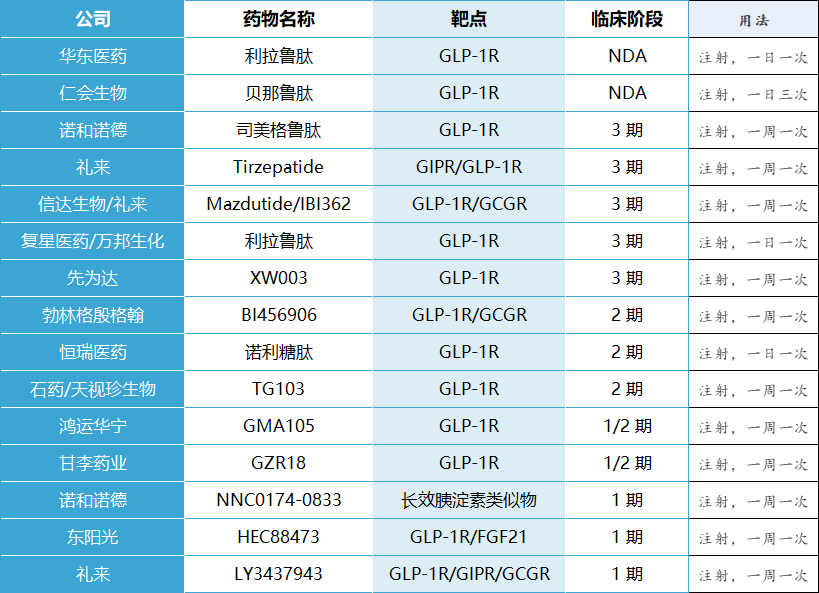
资料来源:安信证券、药融云数据库
恒瑞医药在糖尿病领域布局多年,已有创新药恒格列净获批上市。降糖药开发成减肥药,GLP-1减肥药大战正酣。恒瑞管线中GLP-1类产品颇为丰富,公司在2022年报中也有展示。恒瑞还在继续开发新品,据药融云数据库,2023年5月5日,恒瑞医药1类新药HRS9531注射液已获批临床,用于减重。
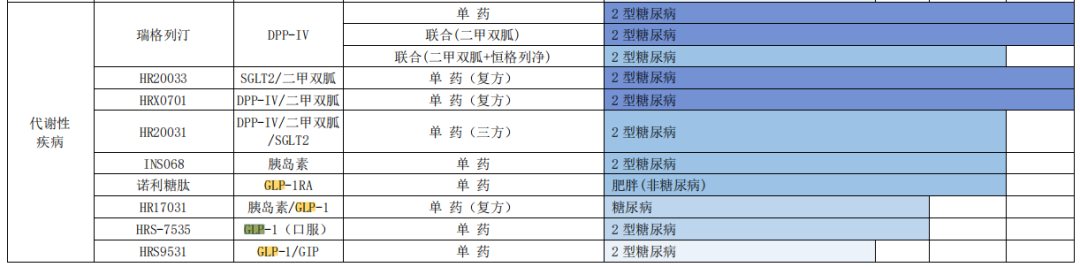

图片来源:恒瑞医药2022年财报
此次ADA大会,恒瑞医药的两款在研创新药——新型口服小分子GLP-1RA(HRS-7535)和GLP-1/GIP双受体激动剂(HRS9531)最新研究成果精彩亮相。
这两项研究均为随机、双盲、安慰剂对照、单次递增剂量(SAD)和多次递增剂量(MAD)的I期研究,在健康受试者中观察两种药物的安全性、耐受性、药代动力学(PK)和药效学(PD),整体表现令人鼓舞。以下是两款创新药的最新研究结果。
新型口服小分子GLP-1RA(HRS-7535):SAD和MAD均具有可接受的安全性和良好PK/PD,且受试者体重明显下降。
背景:HRS-7535是一种新型口服小分子GLP-1RA。临床前研究发现,在无严格限食的情况下,HRS-7535可明显改善葡萄糖耐量,促进胰岛素分泌,减少摄食量。本研究旨在健康受试者中评估SAD和MAD的HRS-7535的安全性、耐受性、PK和PD(NCT05347758)。
方法:研究纳入年龄18~55岁、体重指数(BMI)19.0~28.0kg/m2,糖化血红蛋白(HbA1c)<6.2%的明显健康成人。在SAD中,健康受试者随机(6:2)接受HRS-7535(15mg、60mg和120mg)或安慰剂治疗。在MAD中,健康受试者随机(18:6)接受每日HRS-7535[120mg(30/60/90/120mg滴定方案)]或匹配的安慰剂治疗4周。
结果:
参与SAD和MAD的受试者各有24例。两组中治疗期间出现的不良事件(TEAE)均为轻度。PK大致成比例。在SAD中,HRS-7535给药范围内的中位达峰时间(Tmax)为5.98~5.99h,末端清除半衰期(t1/2)为5.28~9.08h。在MAD中,第28天时HRS-7535给药范围内的中位Tmax为5.98~10.98h,几何平均t1/2为6.48~8.42h。在MAD中,使用HRS-7535的受试者第29天时的体重自基线平均下降4.38kg。
结论:无论SAD还是MAD,HRS-7535均具有可接受的安全性和良好的PK/PD;此外,在健康受试者中还可观察到体重明显下降。这些发现支持HRS-7535在代谢综合征患者中的进一步临床探索。
GLP-1/GIP双受体激动剂(HRS9531):耐受性良好,明显降低血糖和体重
背景:越来越多的证据表明,GLP-1/GIP双受体激动剂能够显著控制血糖并减轻体重。本研究旨在健康受试者中观察GLP-1/GIP双受体激动剂(HRS9531)的安全性、耐受性、PK和PD(NCT05152277)。
方法:在SAD中,健康受试者随机(4:1)接受皮下注射HRS9531(0.1mg、0.3mg、0.9mg、2.7mg、5.4mg和8.1mg)或安慰剂治疗。在MAD中,健康受试者随机(4:1)接受HRS9531[0.9mg、2.7mg和5.4mg(2.7/2.7/4.0/5.4mg滴定)]或安慰剂治疗,每周1次,持续4周。两组的主要终点均为安全性和耐受性。
结果:
分别有60例和30例受试者被纳入SAD和MAD。不良事件均为轻度到中度(大多数为轻度),未发生严重低血糖或其他严重事件。
在0.9~8.1mg剂量范围内,HRS9531的药物暴露与剂量成比例。SAD的中位Tmax和平均t1/2分别为48~72h和156~182h,MAD在第4次给药后的中位Tmax和平均t1/2分别为48~72h和169~192h。
在单次和多次给药后,空腹血糖(FPG)水平均呈剂量依赖性下降。在MAD中,与安慰剂相比,第23天时口服葡萄糖耐量试验(OGTT)0~2h葡萄糖曲线下面积(AUC)呈剂量依赖性下降。
在SAD中,体重下降呈剂量依赖性,8.1mg组第8天时平均最大减重幅度为3.8kg(4.9%)。在MAD中,0.9~5.4mg组第29天时(治疗4周后)的平均减重幅度范围为4.3~7.7kg(6.7%~9.3%),5.4mg组第36天时的减重幅度最大(8.0kg,10.0%)。
结论:HRS9531耐受性良好,能明显降低血糖和体重。这些数据支持HRS9531治疗代谢相关疾病(如T2DM和肥胖)的进一步临床开发。
本次HRS-7535、HRS9531在ADA年会上展示的最新研究结果令人鼓舞,期待二者未来有更多数据发布,为GLP-1RA、GLP-1/GIP双受体激动剂在代谢相关疾病防治中的应用积累更多中国人群数据。
恒瑞医药最近好消息不断,近期,CDE承办了恒瑞医药1类新药注射用瑞卡西单抗的上市申请,拟定适应症(或功能主治)为用于治疗高胆固醇血症患者。注射用瑞卡西单抗是公司自主研发的抗PCSK9的单克隆抗体。目前全球已有两款同类药物获批上市,包括安进公司研发的依洛尤单抗和赛诺菲公司研发的阿利西尤单抗。经查询EvaluatePharma数据库,2022年依洛尤单抗和阿利西尤单抗全球销售额合计约18.75亿美元。截至目前,注射用瑞卡西单抗相关项目累计已投入研发费用约2.5亿元。
资料来源:
安信证券
<END>






















































 川公网安备51019002008863号
川公网安备51019002008863号 本网站未发布麻醉药品、精神药品、医疗用毒性药品、放射性药品、戒毒药品和医疗机构制剂的产品信息
本网站未发布麻醉药品、精神药品、医疗用毒性药品、放射性药品、戒毒药品和医疗机构制剂的产品信息
收藏
登录后参与评论
暂无评论