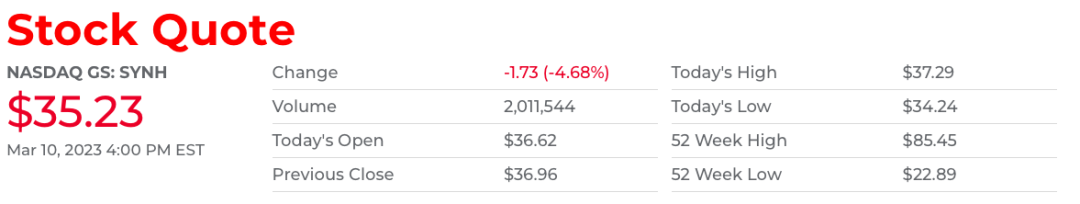
近日,Creative Medical Technology Holdings(NASDAQ:CELZ)宣布,与Syneos Health(Nasdaq: SYNH)达成合作,对其细胞疗法进行1/2期随机试验,用于潜在的1型糖尿病治疗。双方合作的财务细节没有披露。
2月8日,Creative Medical的治疗1型糖尿病候选药物CELZ-201获得了FDA的批准,进入安全性和有效性的1/2期试验,预计将于本月底开始。
截图来源:药融云全球临床试验数据库
Creative首席执行官Timothy Warbington表示:“这项首次在国内开展的临床试验对公司来说是一个里程碑事件,反映了我们致力于开发具有潜力的新型疗法,以解决高未满足的医疗需求。”
Creative Medical Technology Holdings是一家生物技术公司,致力于在免疫治疗、内分泌学、泌尿学、神经学和骨科领域识别和翻译新型生物疗法。
Creative研发管线

Syneos Health是一家全集成生物制药解决方案机构,旨在加速客户的成功。公司将独特的临床、医疗事务和商业见解转化为结果,以应对市场情况。
2月16日,Syneos发布2023财报,去年全年收入53.931亿美元,按固定货币计算较上年增长5.8%。临床解决方案收入40.706亿美元增长3.8%。收购为临床解决方案报告的收入增长贡献了约66个基点。商业解决方案收入13.225亿美元,按固定货币基准增长12.6%。
2月28日,Syneos推出了一个去中心化的临床试验中心网络,旨在推动“数字医疗技术解决方案”。该网络将覆盖各种各样的治疗领域,包括内科和全科医学、家庭医学、神经病学、内分泌学、儿科和精神病学等。
参考资料:
[1] 各公司官网
[2] 药融云数据库vip.pharnexcloud.com/?zmt-mhwz
<END>






















































 川公网安备51019002008863号
川公网安备51019002008863号 本网站未发布麻醉药品、精神药品、医疗用毒性药品、放射性药品、戒毒药品和医疗机构制剂的产品信息
本网站未发布麻醉药品、精神药品、医疗用毒性药品、放射性药品、戒毒药品和医疗机构制剂的产品信息
收藏
登录后参与评论
暂无评论