2月28日,ADC Therapeutics公布2022年财报:全年营收2.1亿美元,同比增长519%,净利润亏损1.56亿美元;去年研发费用投入达1.88亿美元,同比增长18.9%。自2011年成立以来,该公司一直处于净亏损状态,且逐年扩大。
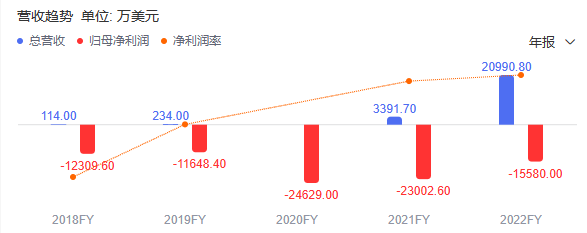
公司的核心产品Zynlonta于2021年4月上市,是FDA批准的首款靶向CD19 的ADC药物。Zynlonta在2022年全年销售额为7490万美元,同比增长120.9%,去年第四季度净销售额为1980万美元,同比增长仅16.5%。虽然营收大增5倍,但是核心产品销售,低于市场预期。近一年ADC Therapeutics市值目前仅剩下2.6亿美元,蒸发超过80%。
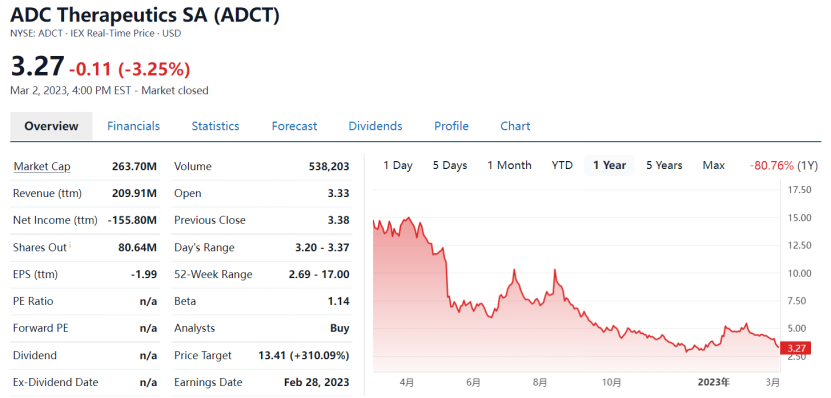
但是在第四季度业绩电话会议上,ADC Therapeutic领导团队确对公司未来发展充满希望,公司首席执行官Ameet Mallik表示“或许新领导人将带来释放公司全部价值的能力,公司将迎来下一阶段的增长。在未来三到五年内,我们预计将继续增长Zynlonta的销售额,推进管线,扩大我们的新合作伙伴关系范围,并实现盈利。”
未来公司将专注的三大核心增长支柱有三个:最大化Zynlonta的商业价值,推进基于pbd的管线和扩展ADC平台。
值得一提的是,ADC Therapeutics2022年许可证收入1.35亿美元,包括来自Sobi的5000万美元的欧洲监管批准里程碑,以及Sobi和田边三菱制药公司的8500万美元的预付款项。在欧洲, 公司与Sobi已经于2022年7月,达成合作协议,引进Loncastuximab Tesirine在欧洲等地权益, 预计2023年第二季度, Sobi将在欧洲推动ZYNLONTA上市。
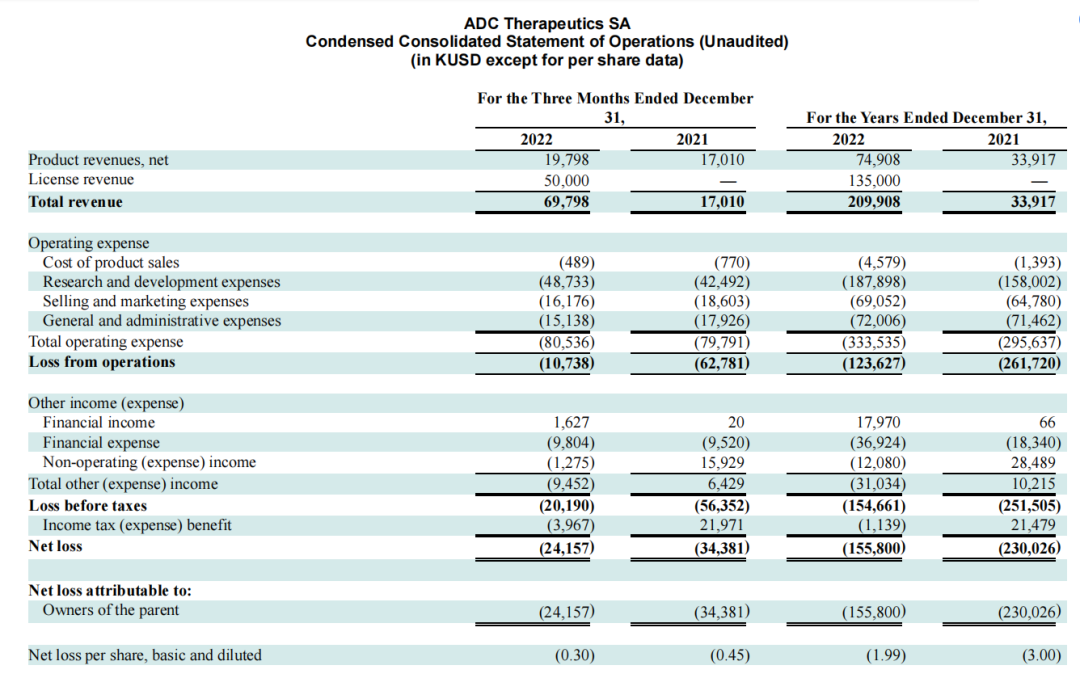
在日本,2021年1月,ADC Therapeutics与田边三菱制药(MTPC)签订了独家许可协议,后者将在日本开发和商业化Zynlonta用于所有血液和实体瘤适应症。预计总支付金额2.35亿美元。
ADC Therapeutics与田边三菱制药就Zynlonta签订的交易信息
截图来源:药融云全球医药交易数据库
ADC therapeutic 目前仅有ZYNLONTA进入商业化阶段。在Cami之后, ADCT-601、ADCT-602和ADCT-901也在2022年进入1期临床。国内瓴路药业(Overland Pharmaceuticals)和ADC Therapeutics的合资公司Overland ADCT BioPharma负责在大中华区和新加坡开发和商业化ADC Therapeutics的四款ADC药物, 包括:ZYNLONTA,ADCT-602,ADCT-601和ADCT-901。
关于ZYNLONTA

- 获批情况
ZYNLONTA(loncastuximab tesirine)首次在2021年4月获得FDA批准上市,用于治疗成人复发或难治性弥漫大B细胞淋巴瘤(DLBCL),同年底获得欧盟和英国批准上市。据药融云数据库显示,截止目前,ZYNLONTA针对弥漫大B细胞淋巴瘤、B淋巴细胞瘤、高级别B细胞淋巴瘤的适应症均已获批上市。
ZYNLONTA适应症研发现状
截图来源:药融云全球药物研发数据库
- 临床试验
目前正在进行几项LOTIS系列试验,评估针对DLBCL和B-NHL的疗效和安全性以及联合用药相关情况。

2022年7月11日,瓴路爱迪思宣布,在LOTIS-5验证性第三阶段全球临床试验中,首例患者在中国接受了ZYNLONTA(朗妥昔单抗)联合利妥昔单抗的治疗,该试验主要用于二线或更晚的、不符合移植条件的弥漫性大B细胞淋巴瘤(DLBCL)患者。

截图来源:药融云全球药物研发数据库
关于ADC Therapeutics

ADC Therapeutics公司(纽约证交所:ADCT)是一家处于商业阶段的生物技术公司,以其新一代靶向抗体药物结合物(ADCs)改善癌症患者的生活。公司正在推进其基于PBD的ADC专利技术,以改变血液系统恶性肿瘤和实体瘤患者的治疗模式。ADC Therapeutics公司的CD19导向型ADC ZYNLONTA(loncastuximab tesirine-lpyl)已被美国食品和药物管理局批准用于治疗经过两线或多线系统治疗后的复发或难治性弥漫性大B细胞淋巴瘤。ZYNLONTA也在与其他药物联合开发中。除ZYNLONTA外,ADC Therapeutics公司还有多种ADC正在进行临床和临床前开发。

参考资料:
[1] 药融云数据库
[2] ADC Therapeutic 2022年报
[3] https://ir.ADCtherapeutics.com/press-releases/press-release-details
想要解锁更多药企信息吗?查询药融云数据库(vip.pharnexcloud.com/?zmt-mhwz)掌握药企公司基本信息、投融资情况、产品管线分布、药物销售情况与各维度分析、药物研发情况、年度报告、最新进展动态、临床试验信息、市场规模与前景等,以及帮助企业抉择可否投入时提供数据参考!注册立享15天免费试用!

<END>























































 川公网安备51019002008863号
川公网安备51019002008863号 本网站未发布麻醉药品、精神药品、医疗用毒性药品、放射性药品、戒毒药品和医疗机构制剂的产品信息
本网站未发布麻醉药品、精神药品、医疗用毒性药品、放射性药品、戒毒药品和医疗机构制剂的产品信息
收藏
登录后参与评论
暂无评论