
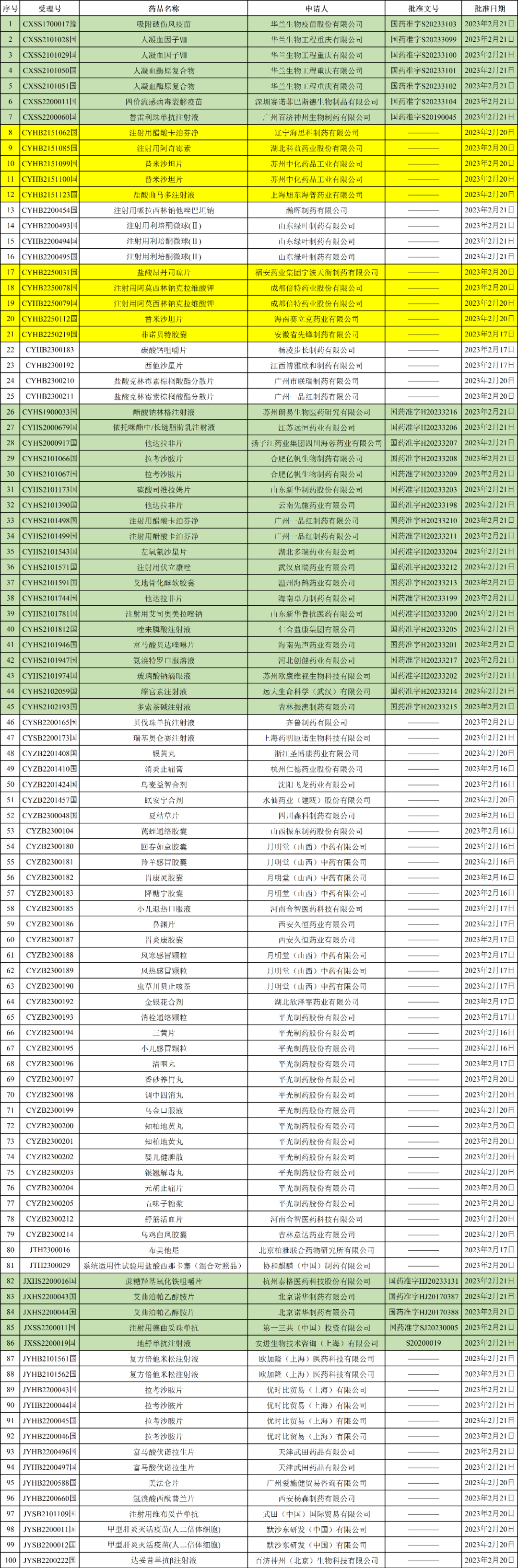
2023年02月24日,NMPA发布最新药品批准证明文件送达信息,本批次共有100个受理号获批,其中10个为一致性评价受理号,包括:
- 辽宁海思科制药有限公司,注射用醋酸卡泊芬净
- 湖北科益药业股份有限公司,注射用阿奇霉素
- 成都倍特药业股份有限公司,2品规注射用阿莫西林钠克拉维酸钾
- 等
另有32个上市申请受理号获批,涉及25个品种,多个品种视同通过一致性评价。
- 山东新华制药股份有限公司,碳酸司维拉姆片
- 海南先声药业有限公司,富马酸贝达喹啉片
- 北京诺华制药有限公司,2品规艾曲泊帕乙醇胺片
- 等
此外,百济神州抗PD-1抗体替雷利珠单抗(商品名:百泽安)的第10项适应症获批,用于一线治疗肿瘤表达PD-L1的晚期或转移性胃或胃食管结合部(G/GEJ)腺癌患者。
据药融云数据库查询,替雷利珠单抗于2019年12月26日首次获批在中国上市,用于治疗霍奇金淋巴瘤。在上市后,百济神州还在不断进行针对其他适应症的研发,截止目前已新增上市了转移性非小细肺癌、转移性食管鳞状细胞癌、肝细胞癌、晚期实体瘤等多个适应症。2022年,替雷利珠单抗在我国院内的销售额同比增长110%,达到了10.80亿人民币。
截图来源:药融云全国医院销售数据库
阿斯利康和第一三共联合开发的注射用德曲妥珠单抗正式在中国获批上市。适应症为:单药适用于治疗既往接受过一种或一种以上抗HER2药物治疗的不可切除或转移性HER2阳性成人乳腺癌患者。德曲妥珠单抗是一款靶向HER2的抗体偶联药物,最早于2019年12月在美国上市,用于治疗转移性乳腺癌。2022年在全球售卖了3亿美元。
德曲妥珠单抗研发现状
截图来源:药融云全球药物研发数据库
第一三共在中国向CDE递交的德曲妥珠单抗新药进口上市申请,于2022年3月21日获CDE承办。2022年4月,CDE将德曲妥珠单抗的该适应症上市申请纳入优先审评,可加快审评速度,加快新药上市速度。
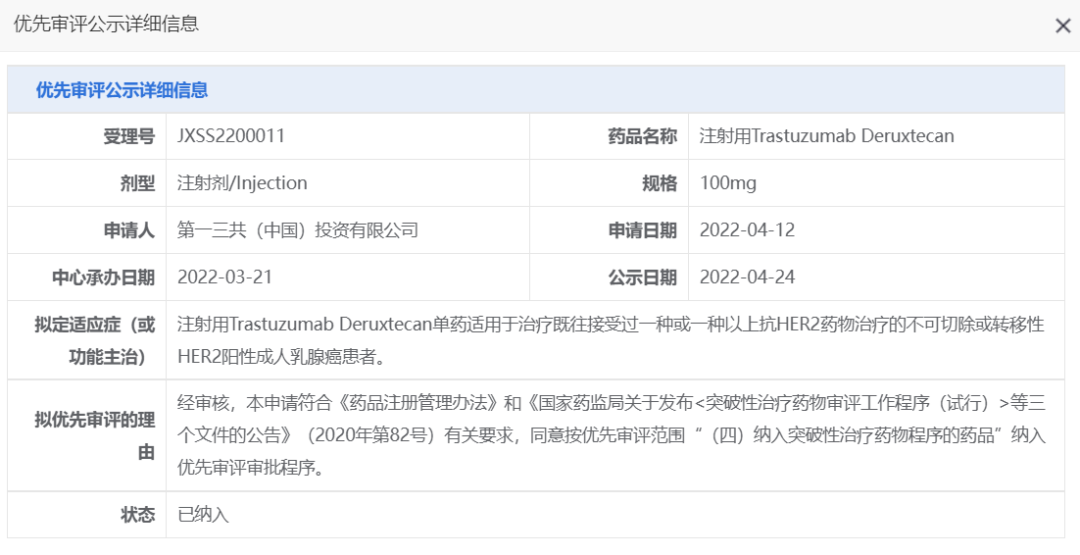
截图来源:CDE官网
2023年02月24日药品批准证明文件送达信息
想要解锁更多药品信息吗?查询药融云数据库(vip.pharnexcloud.com/?zmt-mhwz)掌握药品各国上市情况、药品批文信息、销售情况与各维度分析、市场竞争格局、药企申报审批信息、最新动态与前景等,以及帮助企业抉择可否投入时提供数据参考!注册立享15天免费试用!

<END>


































![医药高地:核药!恒瑞医药镥[177Lu]氧奥曲肽注射液获批临床](https://oss-personal-public.bcpmdata.com/images/covers/202302/09/e3938ad9f1d23e2fd043611c4a98c02a.png)



















 川公网安备51019002008863号
川公网安备51019002008863号 本网站未发布麻醉药品、精神药品、医疗用毒性药品、放射性药品、戒毒药品和医疗机构制剂的产品信息
本网站未发布麻醉药品、精神药品、医疗用毒性药品、放射性药品、戒毒药品和医疗机构制剂的产品信息
收藏
登录后参与评论
暂无评论