
近年来,受一致性评价、集采常态化等利好政策支持与资本加码,国内创新药开发持续升温,研发难度加大,部分靶点同质化严重,各大药企不断内卷。此时,高技术、高壁垒的高端制剂不失为一条创新的“捷径”。
高端制剂技术是改良型新药发展的核心技术,与仿制药相比,其技术门槛更高,更具成长性;与原研相比,其在临床时间、研发难度、研发成本等方面又更具备优势。因此高端制剂是企业差异化发展的高性价比方向,其产品创造的收入不亚于新分子实体。
高端制剂的特殊剂型包括脂质体、微球、口溶膜、胶束、纳米粒、PEG(聚乙二醇)化等众多缓控释和靶向剂型,其中脂质体是制剂领域中难度较大、研发门槛较高的高端制剂,并已成为药物开发的主流趋势之一。脂质体作为药物输送载体可以增加包封药物的溶解度;提高药物的治疗效果,减少用药量;减轻药物的不良反应;延长药物的体内循环时间;克服肿瘤细胞的耐药性;提高药物输送的靶向性;具有良好的生物相容性。
目前我国仅有3个纳米脂质体药物获得生产批文,分别为注射用紫杉醇脂质体、盐酸多柔比星脂质体、注射用两性霉素B脂质体。目前国内市场,已上市的脂质体制剂企业有绿叶制药、石药集团、上药新亚、常州金远和复旦张江。
2月20日,浙江智达药业的盐酸多柔比星脂质体注射液获批上市,视同通过一致性评价,高端制剂脂质体市场新添一玩家。盐酸多柔比星属广谱抗肿瘤药,常用于多发性骨髓瘤、淋巴瘤、卵巢癌、乳腺癌的化疗。而盐酸多柔比星脂质体注射液则可实现药物的增效减毒,定向聚集和精准治疗。

截图来源:NMPA官网
据药融云一致性评价数据库显示,此前,该50亿高端制剂已有石药集团欧意药业(首家)、常州金远药业过评,加上此次的浙江智达药业,终于迎来了一致性评价满3家,此后在药品集中采购等方面不再选用未通过仿制药一致性评价的品种。
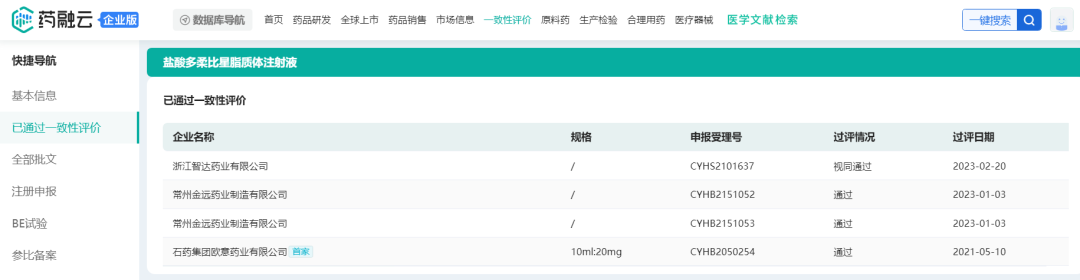
截图来源:药融云一致性评价数据库
据药融云统计,盐酸多柔比星脂质体注射液在我国院内的销售情况表现为水涨船高,每年都保持着较平稳增长。2021年同比2022年增长了20.57%,突破五十亿大关。此前,国内仅有3家药企拥有该高端制剂仿制药的药品批文,获批生产销售,除了过评的企业外,还有一家上海复旦张江。其中,石药集团欧意药业占据其销售市场的绝对领导地位,2021年的份额为59.97%,其次是常州金远药业(27.2%)、上海复旦张江(12.83%)。
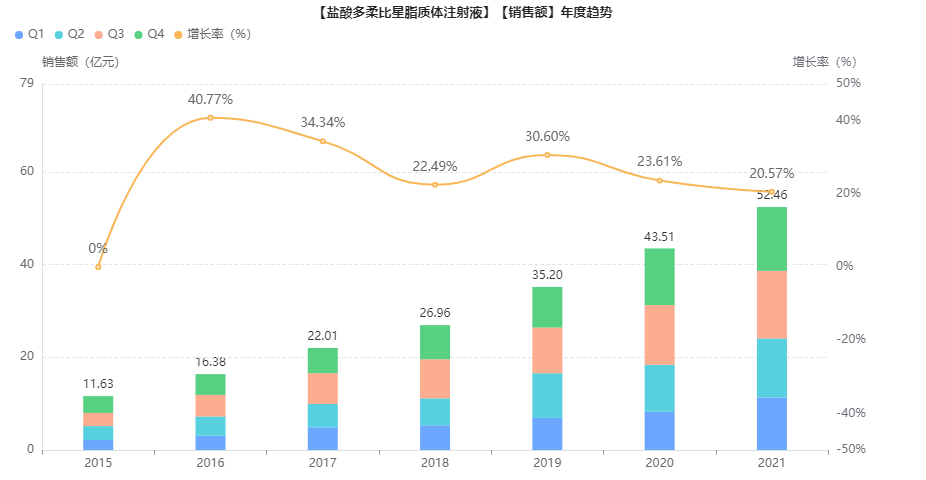
截图来源:药融云全国医院(全终端)销售数据库
近年来,我国大力推进医药体系改革,鼓励医药体系的自主创新。一致性评价和国家集中带量采购推动提升仿制药质量,鼓励发展高端制剂。CDE曾于2020年10月发布盐酸多柔比星脂质体注射液仿制药研究技术指导原则(试行),提出仿制药开发过程中药学研究、非临床研究和生物等效性研究的技术要求,旨在为该仿制药的研发提供技术指导。
根据药物临床试验登记与信息公示平台显示,浙江智达药业已完成盐酸多柔比星脂质体注射液生物等效性试验。
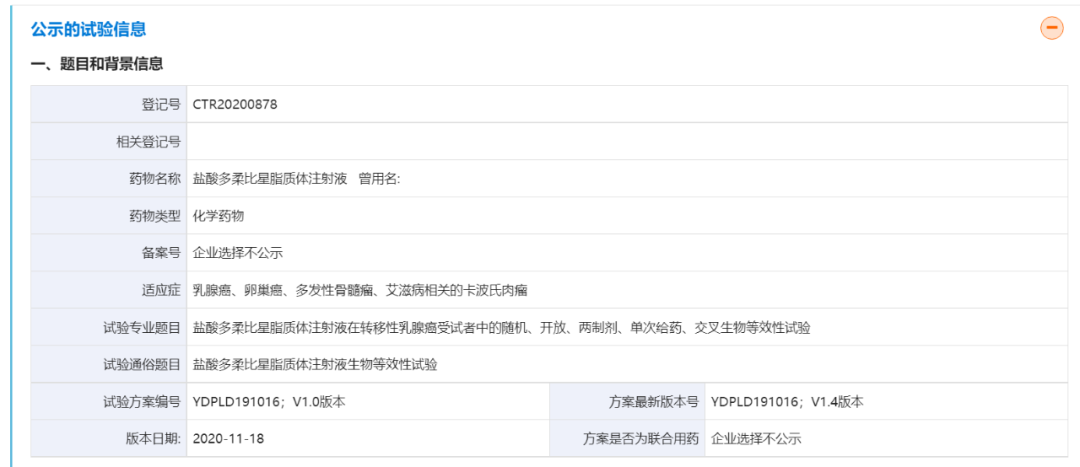
试验目的:
主要目的:评价浙江智达药业有限公司生产的盐酸多柔比星脂质体注射液(10ml:20mg)与参比制剂盐酸多柔比星脂质体注射液(10ml:20mg)(商品名:CAELYX®)的人体生物等效性。次要目的:评价中国转移性乳腺癌患者单次空腹静脉注射受试制剂盐酸多柔比星脂质体注射液(10ml:20mg)和参比制剂盐酸多柔比星脂质体注射液(10ml:20mg)(商品名:CAELYX®)后的安全性。
此外,据CDE显示,浙江海正药业、无锡紫杉药业、齐鲁制药均提交了盐酸多柔比星脂质体注射液的仿制药上市申请,目前均处于审评审批中。
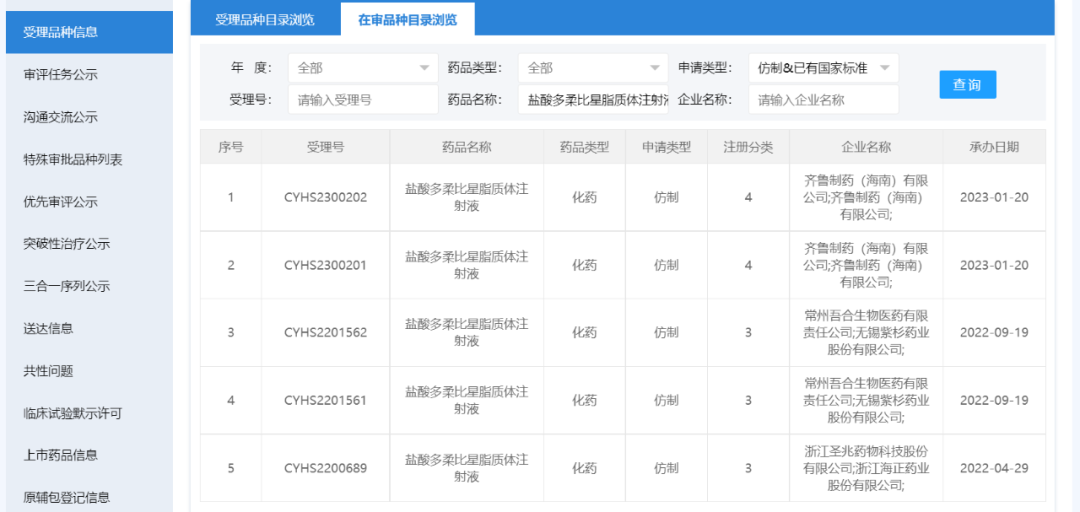
截图来源:CDE官网
参考来源:
[1] CDE官网
[2] NMPA官网
[3] 药融云数据库
想要解锁更多药品信息吗?查询药融云数据库(vip.pharnexcloud.com/?zmt-mhwz)掌握药品各国上市情况、药品批文信息、销售情况与各维度分析、市场竞争格局、药企申报审批信息、最新动态与前景等,以及帮助企业抉择可否投入时提供数据参考!注册立享15天免费试用!

<END>






















































 川公网安备51019002008863号
川公网安备51019002008863号 本网站未发布麻醉药品、精神药品、医疗用毒性药品、放射性药品、戒毒药品和医疗机构制剂的产品信息
本网站未发布麻醉药品、精神药品、医疗用毒性药品、放射性药品、戒毒药品和医疗机构制剂的产品信息
收藏
登录后参与评论
暂无评论