
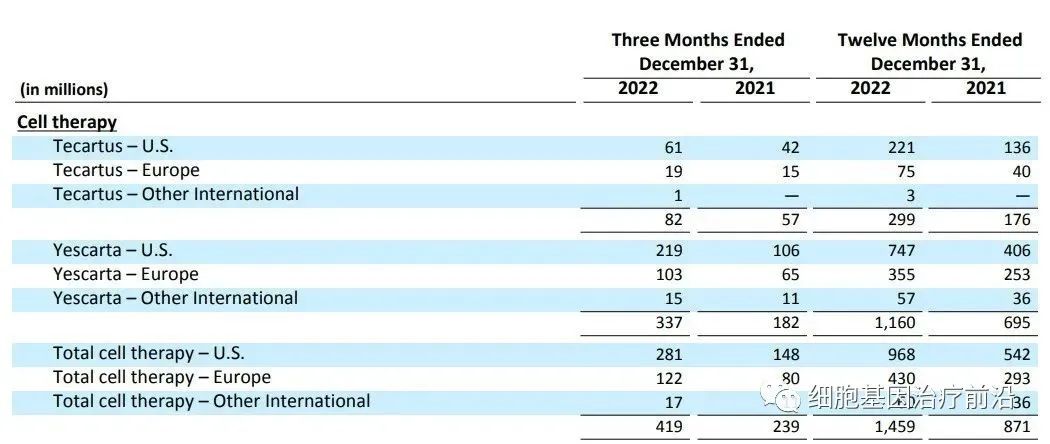
2月2日,吉利德公布了2022财报:全年总收入269.82亿美元,其中CAR-T疗法Tecartus全年营收2.99亿美元,另外一款疗法Yescarta营收11.6亿美元。两款CAR-T疗法总营收达到了14.59亿美元,同比增长67.5% 。
2月9日,吉利德科学公司旗下公司Kite公布了CAR-T疗法Tecartus(brexucabtagene autoleucel)的关键临床研究( ZUMA-3)三年随访结果。
研究显示,Tecartus治疗成人复发/难治性B细胞前体急性淋巴细胞白血病(ALL)的中位OS(mOS)为 26 个月,缓解率(CR+CRI)达71%。
在2期治疗患者队列(n=55)中位随访时间为38.8个月(范围32.7-44.6)。36.0个月时的OS率为47.1% (95% CI,32.7-60.2),所有接受治疗的2期患者(n=55)的中位OS为26.0个月,完全缓解(CR)或CR伴血液学不完全恢复(CRi)(n = 39)。总体CR率(CR + CRi)、CR和随后的异基因造血干细胞移植(allo-SCT)移植率分别下调为71%、56%和20%后保持不变。
对于在1期和2期均接受关键剂量治疗的患者(n=78),数据截止时的中位随访时间为41.6个月(范围32.7-70.3)。在数据截止时,36%的患者(n=28)仍然存活,所有接受治疗的患者(n=78)中位OS为25.6个月(95% CI, 16.2-47.0)。
brexucabtagene autoleucel临床试验全球开展情况
截图来源:药融云全球临床试验数据库
经药融云数据库查询,2021年10月,美国FDA宣布,批准吉利德CAR-T疗法Tecartus(Brexucabtagene Autoleucel)一项新适应症,用于治疗复发或难治性B细胞急性淋巴细胞白血病(B-ALL)成年患者(18岁及以上)。至此,Tecartus成为首个获批治疗成人ALL的CAR-T疗法。
2022年9月,吉利德子公司Kite宣布,欧盟委员会(EC)已批准其CAR-T疗法Tecartus(brexucabtagene autoleucel)新适应症上市,用于治疗26岁及以上成人复发或难治性B细胞前体急性淋巴细胞白血病(ALL)。
Tecartus部分适应症研发现状(active)
截图来源:药融云全球药物研发数据库
最后,ZUMA-3研究员、Bijal Shah博士表示:“对于患有ALL的成年患者,需要提供长期的治疗方案,CAR-T疗法Tecartus这些新数据表明,持久的反应率和生存期可显著改善ALL的成年患者的治疗。”
一、关于Tecartus
Tecartus是一种CD19导向的自体CAR-T疗法,其原理是将患者自身的T细胞进行基因修饰使其表达靶向抗原CD19的嵌合抗原受体(CAR),CD19是一种表达于多种血液肿瘤细胞表面的抗原蛋白,包括B细胞淋巴瘤和白血病细胞。经改造后的T细胞回输至患者体内,从而识别并攻击表达CD19的肿瘤细胞及其他B细胞。
二、关于ZUMA-3研究
ZUMA-3是一项正在进行的国际多中心(美国、加拿大、欧洲)、单臂、开放标签、注册注册性I/II期研究,用于接受过标准系统治疗或造血干细胞移植后难治性或复发的ALL成年(≥18岁)患者。旨在评估Tecartus针对接受过标准系统治疗或造血干细胞移植后难治性或复发的ALL成年患者的疗效和安全性。主要终点是总体完全缓解(OCR)率或外周血细胞未完全恢复的完全缓解(CRi)率。次要终点包括缓解持续时间(DOR)、无复发生存期(RFS)、总生存期(OS)、微小残留病(MRD)阴性率和异基因造血干细胞移植率(alloc-SCT rate)。
三、关于ALL
复发或难治性B细胞前体急性淋巴细胞白血病(ALL)是一种侵袭性罕见的血癌,也可累及淋巴结、脾脏、肝脏、中枢神经系统和其他器官。全球每年约有6.4万人被诊断为ALL,虽然80%的ALL发生在儿童身上,但它在成人中是一种毁灭性的疾病。在成人中,最常见的一种形式是前体B细胞ALL,占病例的75%。患有ALL的成年人中有50%会复发,且生存率非常低,目前标准治疗的中位总生存期(OS)大约只有8个月。
参考资料:
[1] Gilead官网
[2] 药融云数据库
想要解锁更多药物研发信息吗?查询药融云数据库(vip.pharnexcloud.com/?zmt-mhwz)掌握药物基本信息、市场竞争格局、销售情况与各维度分析、药企研发进展、申报审批情况、最新市场动态、市场规模与前景等,以及帮助企业抉择可否投入时提供数据参考!注册立享15天免费试用!

<END>





















































 川公网安备51019002008863号
川公网安备51019002008863号 本网站未发布麻醉药品、精神药品、医疗用毒性药品、放射性药品、戒毒药品和医疗机构制剂的产品信息
本网站未发布麻醉药品、精神药品、医疗用毒性药品、放射性药品、戒毒药品和医疗机构制剂的产品信息
收藏
登录后参与评论
暂无评论