
10月14日,NMPA发布最新一批药品批准证明文件待领取信息,其中,石药欧意的玛巴洛沙韦片获批上市,斩获该抗流感单剂量口服药物的国内首仿药。据悉,我国部分省份已经开始进入流感流行季节,并且高于新冠肺炎疫情发生以来的同期水平。抗流感药物的获批有利于短期和长期的流感疫情防控。


截图来源:NMPA官网
玛巴洛沙韦是一款创新的帽状结构依赖性核酸内切酶抑制剂(Cap-dependent endonuclease inhibitor),其作用机制与目前已有抗病毒疗法不同,它可阻截病毒细胞内的核酸内切酶,令病毒失去自我复制能力。玛巴洛沙韦是目前获批的首个、也是唯一一个抗流感的单剂量口服药物。该药最早由日本盐野义开发,后授权给罗氏负责Xofluza美国、中国等市场的开发及销售。
2021年4月,罗氏的单剂量口服创新药物速福达®(英文商品名:Xofluza®,中文通用名:玛巴洛沙韦,英文名:Baloxavir marboxil)获得中国国家药品监督管理局正式批准,用于治疗12周岁及以上急性无并发症的流感患者,包括存在流感并发症高风险的患者。
玛巴洛沙韦片中国批文信息
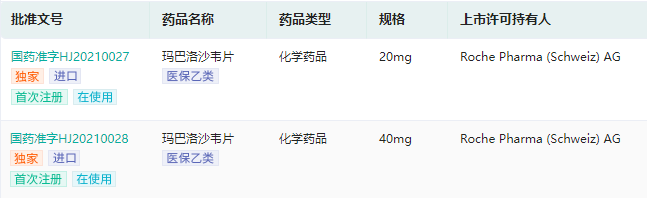
截图来源:药融云中国药品批文数据库
据药融云数据库查询,此前在2021年7月1日,CDE就受理公示了石药欧意递交的4类仿制药玛巴洛沙韦片的上市申请,是国内首家布局该药的企业,目前也是唯一一家。此次获批上市,石药欧意顺理成章地成为该抗流感单剂量口服药物的国内首仿药企业。
另外,在抗流感新药方面,国内企业也在积极开发,目前相关产品有:众生睿创的ZSP1273(最高III期临床阶段)、珍宝岛药业/广州市恒诺康医药的注射用HNC042(I期临床阶段)、青峰医药/银杏树的GP681(最高III期临床阶段)、太景医药研发(北京)有限公司核酸內切酶抑制剂TG-1000(II期临床阶段)、征祥医药的抗流感新药ZX-7101A(最高III期临床阶段)、安帝康生物的ADC189(I期临床阶段)以及中国药科大学抗病毒1类新药黄芩素(天然药物衍生)等。
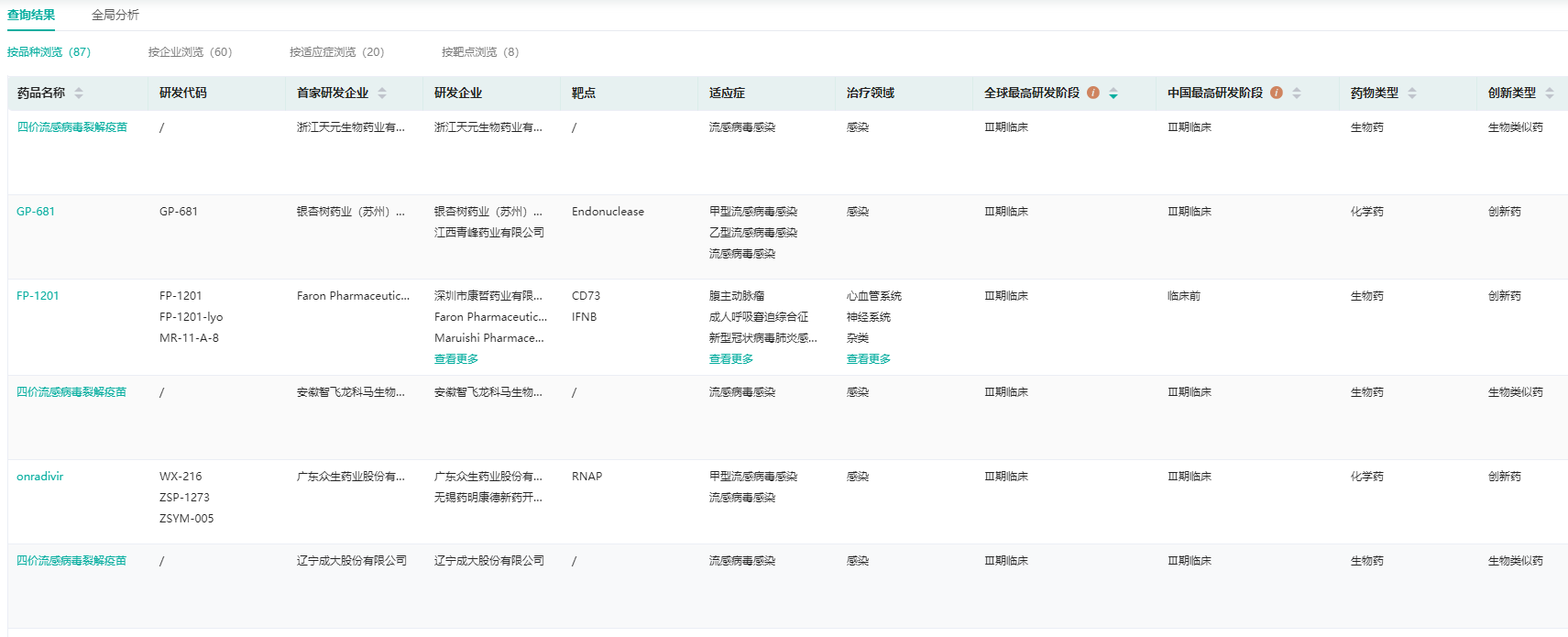
截图来源:药融云全球药物研发数据库
参考来源:
[1]NMPA官网
[2] 药融云数据库
想要解锁更多仿制药信息吗?查询药融云数据库(vip.pharnexcloud.com/?zmt-mhwz)掌握仿制药国内市场格局、上市情况、一致性评价、销售情况与各维度分析、企业申报情况、国家审批最新进展、集采情况、价格信息、市场规模与前景等,以及帮助企业抉择可否投入仿制时提供数据参考!注册立享15天免费试用!

—END—









































 浙公网安备33011002015279
浙公网安备33011002015279 本网站未发布麻醉药品、精神药品、医疗用毒性药品、放射性药品、戒毒药品和医疗机构制剂的产品信息
本网站未发布麻醉药品、精神药品、医疗用毒性药品、放射性药品、戒毒药品和医疗机构制剂的产品信息
收藏
登录后参与评论
暂无评论