
8月11日,齐鲁制药的2.4类新药硫酸阿托品滴眼液获得临床默示许可,用于延缓儿童近视发展。这是齐鲁制药2022年第9款获批临床的新药。

截图来源:CDE官网
低浓度硫酸阿托品滴眼液可以说是一个超级明星品种。近视一旦发生,不可逆转,只能延缓其进一步进展。低浓度硫酸阿托品滴眼液对近视控制的效果已被国际和国内的众多临床研究证实。据悉,在国际上使用阿托品滴眼液控制近视已近20年,并证实0.01%硫酸阿托品对于近视控制的有效率可达到30%-50%。如果联合角膜塑形镜使用,近视防控效果将会更好。
目前,国内尚没有低浓度阿托品滴眼液产品正式获批,仅有兴齐眼科医院、河南省立眼科医院等部分医疗机构有“院内制剂”。所谓院内制剂,又称医疗机构制剂,是医疗机构根据本单位临床需要经批准而配制、自用的固定处方制剂,是市场上没有供应的品种。
据药融云统计显示,硫酸阿托品滴眼液已有10余家药企申报临床,涉及24个受理号。其中艾尔健康眼药、乐普药业、齐鲁制药、博瑞制药、杭州赫尔斯、沈阳兴齐、兆科眼科按2.4类申报,欧康维视、日本参天等按2.2类申报,日本参天还有2个受理号按2.2/2.4申报,台湾五福按5.2类申报。经中国临床试验数据库查询,兆科眼科、沈阳兴齐和欧康维视的硫酸阿托品滴眼液已到临床III期阶段,进展最快。
硫酸阿托品滴眼液临床申报情况(部分,查看更多点击此处)
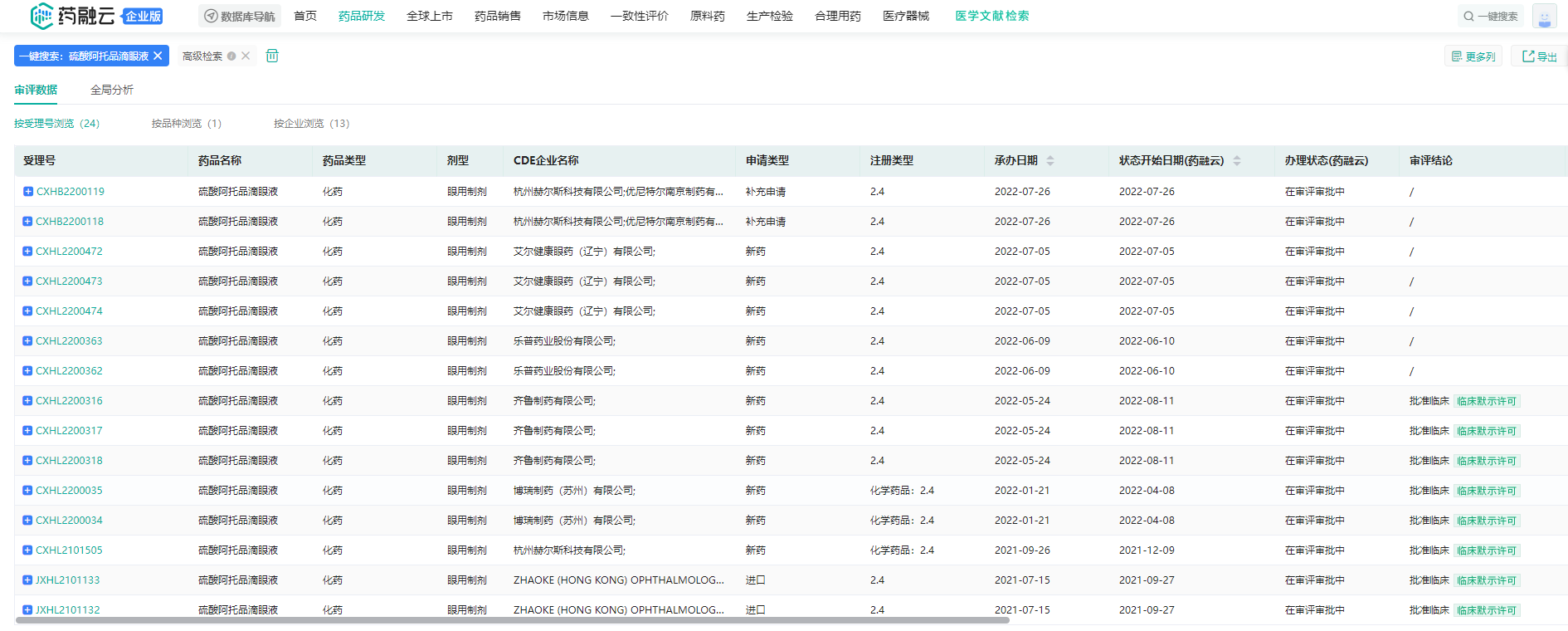
截图来源:药融云中国药品审评数据库
2022年以来,齐鲁制药已有9款新药获批临床(17个受理号)。其中6款为1类新药,分别为QL1706注射液、QLH11906片、注射用QLS31904、注射用QLS21908、QL1604注射液、注射用QLS31906。另有硫酸阿托品滴眼液、利培酮口溶膜和甲磺酸仑伐替尼胶囊等3款2类新药。
齐鲁制药2022年新药获批临床情况(截止8月10日)

数据来源、整理:药融云
1类新药中,除注射用QLS21908用于自身免疫性疾病外,其余均用于肿瘤治疗领域。
注射用QLS21908是齐鲁制药自主开发的创新型生物大分子药物,拟开展治疗 FcγRⅡA 靶点相关的自身免疫性疾病研究。目前国内尚无处于临床试验阶段的同靶点相关产品,QLS21908有望为自身免疫性疾病患者提供新的治疗选择。目前,齐鲁制药正在开展此药的I期临床试验(登记号CTR20221304)。
注射用QLS31906是齐鲁制药的一款双特异性抗体药物,拟用于治疗恶性肿瘤。2021年12月7日,CDE受理该品种的临床试验申请,于今年2月初获得默示许可。
注射用QLS31904是齐鲁制药自主研发的一款靶向DLL3/CD3的双特异性抗体,前期研究已表明,QLS31904能识别肿瘤细胞表面的特异性抗原,同时激活机体自身的免疫细胞,特异性杀伤肿瘤抗原阳性的细胞,以达到治疗的目的。今年7月,齐鲁制药开展并公示了此药的I期临床试验(登记号CTR20221779)。
QL1706注射液项目是齐鲁制药基于MabPair组合抗体生物技术研发的,主要靶向PD-1和CTLA-4D的新型治疗用抗肿瘤组合抗体。今年陆续获得多项临床默示许可,针对非小细胞肺癌、直肠癌、肾细胞癌和宫颈癌等癌种。目前,QL1706注射液最高已到临床II期临床试验阶段。
QLH11906是齐鲁制药开发的一款pan-RAF抑制剂,今年获得的两项临床试验默示许可,拟开发用于治疗MAPK信号通路异常的晚期实体瘤。据公开资料,齐鲁制药QLH11906有望成为BRAF和KRAS突变肿瘤患者的治疗药物。今年6月底,齐鲁制药开展并公示了此药的I期临床试验(登记号CTR20221464)。
利培酮口溶膜是齐鲁制药2022年的第一个改良型新药申请,也是齐鲁制药申报的第6个口溶膜制剂。此外,齐鲁制药还先后申报了阿立哌唑口溶膜、奥氮平口溶膜、草酸艾司西酞普兰口溶膜、盐酸美金刚口溶膜、孟鲁司特钠口溶膜、他达拉非口溶膜等多个口溶膜产品。
甲磺酸仑伐替尼胶囊是一种酪氨酸激酶抑制剂。目前国内已有正大天晴、石药欧意、先声药业等多家药企获批生产销售,齐鲁制药的甲磺酸仑伐替尼胶囊也于2021年9月获批上市,用于既往未接受过全身系统治疗的不可切除的肝细胞癌患者。今年2月,齐鲁制药又递交2.4类临床申请,后于4月获得临床默示许可,拓展适应症,联合QL1706注射液用于一线治疗晚期肾细胞癌的成人患者、既往接受过一线治疗失败的晚期肾细胞癌的成人患者。
参考来源:
[1] CDE官网
[2] 药融云数据库
想要解锁更多药企创新药信息吗?查询药融云数据库(https://www.pharnexcloud.com/?zmt-mhwz)掌握药企创新药产品布局、基本信息、研发阶段、最新进展、申报获批情况、临床试验信息、市场规模与前景,可否投入研发!注册立享15天免费试用和虎年首份医药数据大礼包!

—END—
















































 浙公网安备33011002015279
浙公网安备33011002015279 本网站未发布麻醉药品、精神药品、医疗用毒性药品、放射性药品、戒毒药品和医疗机构制剂的产品信息
本网站未发布麻醉药品、精神药品、医疗用毒性药品、放射性药品、戒毒药品和医疗机构制剂的产品信息
收藏
登录后参与评论
暂无评论