
近日,Escend Pharmaceuticals,Inc. 公司宣布,美国食品和药物管理局(FDA)已批准其主要候选药物ES-3000的在研新药申请,用于复发或难治性(R / R)急性髓系白血病(AML)的Ⅰ期临床试验。
Ⅰ期研究的主要目的是确定ES-3000在复发或难治性急性髓系白血病受试者中的安全性和耐受性。FDA孤儿产品开发办公室(OOPD)此前已授予ES-3000孤儿药称号,用于治疗急性髓系白血病和慢性髓系白血病。FDA孤儿药指定提供7年的营销排他性和某些激励措施,包括联邦拨款、税收抵免和新药上市申请(NDA)费用豁免。
“ES-3000成功申请IND加强了我们对其开发的坚定信念。ES-3000可以通过靶向白血病干细胞为持久缓解和减少复发提供新的治疗选择,白血病干细胞在抗治疗中起核心作用。”MBA联合创始人兼首席执行官Saira Bates说。“ES-3000是一种新型小分子,具有有前途的临床前数据,支持靶向白血病干细胞。“联合创始人兼董事长Dennis Brown博士表示。
关于ES-3000
ES-3000是一种口服生物可利用的小分子药物,通过一种新的作用机制减少β-catenin的表达来消融白血病干细胞。Wnt/β-catenin途径对癌症干细胞的存活至关重要。除急性髓系白血病外,ES-3000还在不断拓展适应症的开发中,用于治疗慢性髓系白血病(CML)、骨髓增生异常综合征(MDS)和三阴性乳腺癌(TNBC)。曾于2016年6月获得美国FDA获准的孤儿药称号,用于治疗慢性髓系白血病;同年12月,美国FDA再次获准其孤儿药称号,用于治疗急性髓系白血病。
ES-3000药物基本信息
截图来源:药融云全球药物研发数据库
关于急性髓系白血病
急性髓系白血病(AML)是成人中最常见的急性白血病,存活率最低。急性髓系白血病约占全球所有成人白血病的25%,其中美国、欧洲和澳大利亚的发病率最高。在美国,每年约有20000人被诊断患有急性髓系白血病。急性髓系白血病是一种血液和骨髓的侵袭性癌症,可阻止白细胞成熟,导致“原始细胞”积聚,从而无法为正常血细胞留出空间。但急性髓系白血病是一种具有多种基因突变的异质性疾病。这种异质性延伸到白血病干细胞(LSC),会导致个体患者中有多个LSC库,其表型和分子上可能不同。LSC对当前的化疗方案具有相对的抵抗力,可能是导致急性髓系白血病疾病进展的原因。与慢性髓系白血病 LSC一样,急性髓系白血病 LSC也依赖于β-catenin的过度表达,这使得ES-3000成为急性髓系白血病的治疗候选药物。我们的目标是开发ES-3000,用于治疗急性髓系白血病的现行标准护理疗法,以提供更持久的缓解并减少复发。
关于Escend Pharmaceuticals,Inc.
Escend Pharmaceuticals的使命是通过消融癌症干细胞为肿瘤孤儿适应症开发治疗方法。其业务战略是选择具有既定临床安全性,但尚未获得美国上市批准的小分子候选药物,并将其与适当的肿瘤学适应症相匹配,其中它们对特定细胞途径的影响可以用于开发新的治疗方法。该公司主要研究管线见图所示。
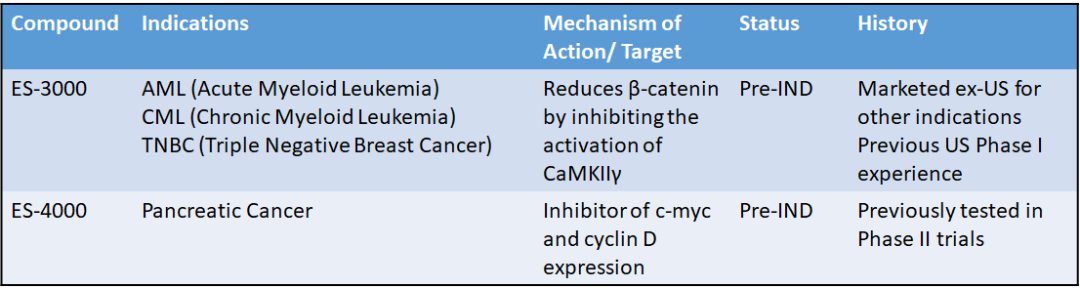
信息来源:
[1]http://www.escendpharma.com/
[2]药融云数据库
想要解锁更多药企创新药信息吗?查询药融云数据库(https://www.pharnexcloud.com/?zmt-mhwz)掌握药企创新药产品布局、基本信息、研发阶段、最新进展、申报获批情况、临床试验信息、市场规模与前景,可否投入研发!注册立享15天免费试用和虎年首份医药数据大礼包!

<END>






















































 川公网安备51019002008863号
川公网安备51019002008863号 本网站未发布麻醉药品、精神药品、医疗用毒性药品、放射性药品、戒毒药品和医疗机构制剂的产品信息
本网站未发布麻醉药品、精神药品、医疗用毒性药品、放射性药品、戒毒药品和医疗机构制剂的产品信息
收藏
登录后参与评论
暂无评论