
引言

2022年7月11日,以色列生物技术公司Can-Fite BioPharma Ltd.宣布其它计划向美国食品和药物管理局(FDA)提交其注册计划,并向欧洲药品管理局(EMA)提交其A3AR激动剂、银屑病新药——Piclidenson(用于中度至重度的银屑病)上市许可申请 (MAA)。
Can-Fite将报告其III期临床试验COMFORT™的方案及最终疗效和安全性结果,另外化学、制造和控制(CMC)、非临床数据和人体药代动力学数据以及其他支持临床药理学计划也一并提交给两个机构。
Piclidenoson
Piclidenoson(CF101)是A3AR(A3腺苷受体)的高特异性激动剂,其通过下调NF-κB-TNF-α信号通路,抑制炎症细胞因子白细胞介素17和23(IL-17和IL-23),从而抑制促炎细胞因子的产生和炎症细胞的凋亡。
Piclidenoson药物基本信息

截图来源:药融云全球药物研发数据库
根据Can-Fite公开的III期临床试验结果,Piclidenoson达到了改善银屑病患者症状的主要终点,通过银屑病面积和严重程度指数(PASI)75反应来衡量:Piclidenoson 3mg:9.7%对比安慰剂:2.6%(P<0.04)。
在次要终点,Can-Fite的Piclidenoson对比安进Otezla的PASI 75(分别为17%对26.2%)和PASI 50(分别为34.1%对49.5%),处于劣势,但是银屑病残疾指数(PDI)更有优势(20.5%和10.3%,P<0.05)。并且,Piclidenoson的安全性相比安进的Otezla更高,在对照实验中,Otezla胃肠道不良事件发生率为6%,而在接受安慰剂或Piclidenson治疗的患者中为1%,并且接受Otezla治疗的患者的治疗终止率明显更高。
A3AR
A3AR是一种G蛋白偶联腺苷受体(AR,4种不同的G蛋白偶联腺苷受体,即A 1、A 2A、A2B和A3),其在炎症、癌症和其他病理体细胞中高表达,而在正常细胞中低表达。腺苷可以以剂量依赖的方式激活A3AR,并且以自分泌方式促进受体表达。
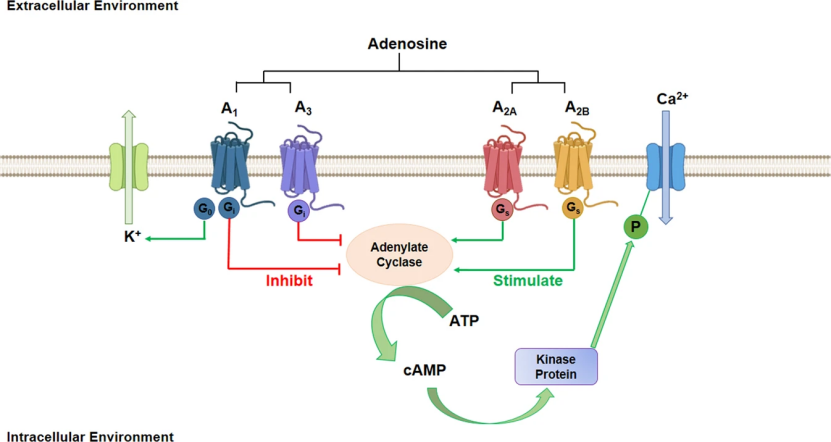
A3AR介导包括PI3K、GSK-3、PKA、PKB/Akt、IKK和NF-kB等关键信号蛋白,导致Wnt和NF-kB通路的失调,这些通路和癌症以及炎症细胞的凋亡相关。
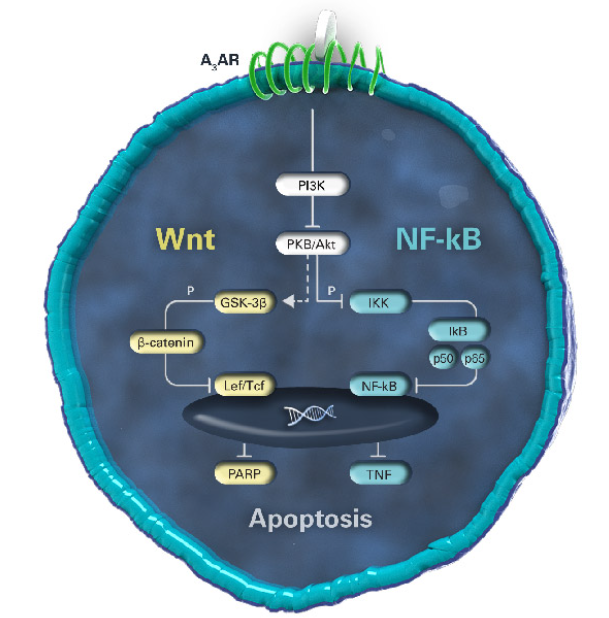
经药融云数据库查询,目前在A3AR激动剂创新药物研发领域布局企业还不算多,且进展较慢,无获批上市产品。其中,Can-Fite的Piclidenoson是所有A3AR激动剂(ADORA3)里面研究进展最快的,在中国地区的商业化已经授权给康哲药业。
A3AR激动剂产品研发情况(部分)
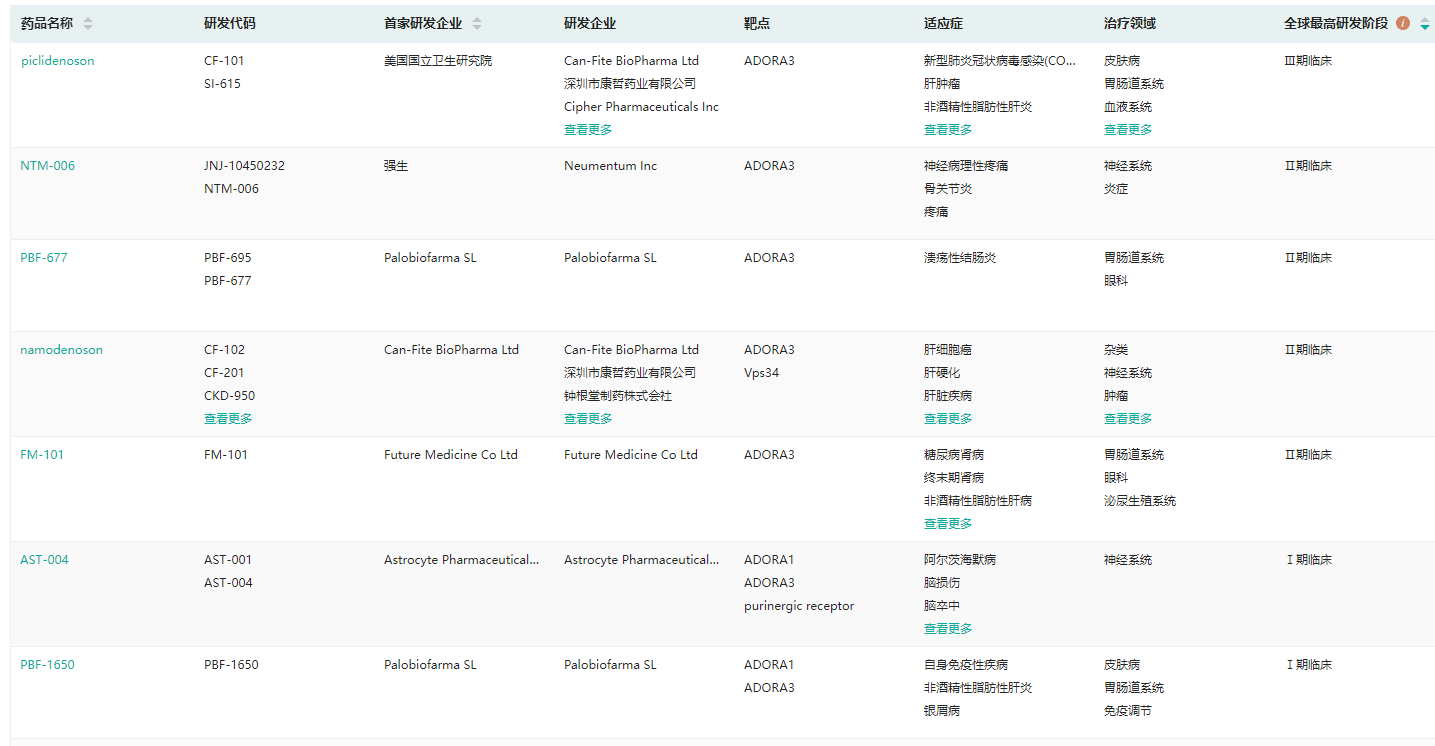
截图来源:药融云全球药物研发数据库
Can-Fite
Can-Fite BioPharma 是一家专注于药物发现和临床开发的以色列生物制药公司,构建了以G蛋白相关的A3腺苷受体作为治疗靶点的平台技术,在II期和III期临床开发中拥有先进的专有候选药物管线,覆盖炎症、肝脏和代谢疾病。
Can-Fite产品管线
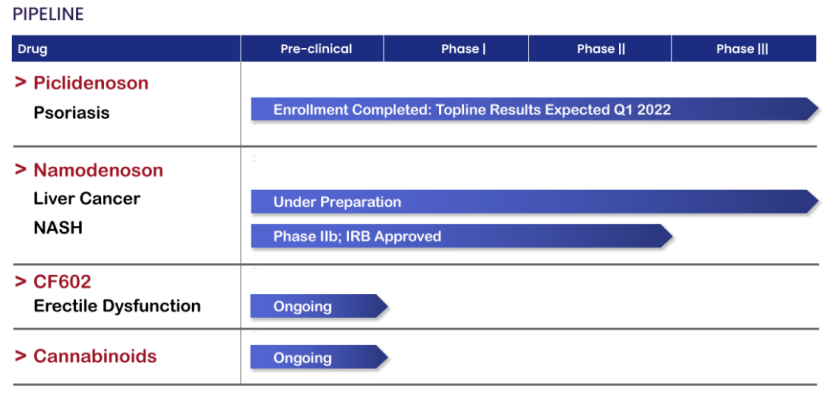
参考来源:
[1] https://www.canfite.com/
[2] Cancer biology and molecular genetics of A3 adenosine receptor
[3] 药融云数据库
想要解锁更多药企创新药信息吗?查询药融云数据库(https://www.pharnexcloud.com/?zmt-mhwz)掌握药企创新药产品布局、基本信息、研发阶段、最新进展、申报获批情况、临床试验信息、市场规模与前景,可否投入研发!注册立享15天免费试用和虎年首份医药数据大礼包!

<END>
















































 浙公网安备33011002015279
浙公网安备33011002015279 本网站未发布麻醉药品、精神药品、医疗用毒性药品、放射性药品、戒毒药品和医疗机构制剂的产品信息
本网站未发布麻醉药品、精神药品、医疗用毒性药品、放射性药品、戒毒药品和医疗机构制剂的产品信息
收藏
登录后参与评论
暂无评论