
2022年5月6日 IGM Biosciences 是一家专注于创造和开发工程化IgM抗体的临床阶段生物技术公司,今天宣布与赛诺菲完成全球合作协议。根据协议,IGM Biosciences 将获得1.5亿美元的预付款,潜在开发、监管和商业里程碑款项可能超过60亿美元。本次合作旨在创建、开发、制造和商业化针对三个肿瘤靶点和三个免疫/炎症靶点的IgM抗体激动剂。
IGM Biosciences 首席执行官 Fred Schwarzer 表示:“我们今天很高兴地宣布,我们与赛诺菲才华横溢且敬业的团队正式开始了激动人心的合作,现已完成交易。” “我们期待与赛诺菲建立长期合作关系,赛诺菲是创新疗法开发和商业化的全球领导者,并在我们目前的管道努力之外,加速我们在多个高度未满足需求领域的 IgM 抗体平台的开发。”
除了1.5亿美元的预付款外,IGM Biosciences 有资格获得可能超过60亿美元的总开发、监管和商业里程碑,以及在某些主要市场国家获得50:50的利润份额,并在其余国家获得净销售额的分级特许权使用费肿瘤学目标的全球净销售额,以及针对自身免疫/炎症目标的全球净销售额的分层特许权使用费。

IGM Biosciences 总部位于加利福尼亚州山景城,是一家临床阶段的生物技术公司,专注于创造和开发工程化 IgM 抗体。自 2010 年以来,IGM Biosciences 一直致力于克服限制 IgM 抗体治疗用途的制造和蛋白质工程障碍。通过努力,IGM Biosciences 创建了一个专有的 IgM 技术平台,用于开发 IgM 抗体,用于那些与 IgG 抗体相比,其固有特性可能提供优势的临床适应症。
据药融云数据库显示,IGM Biosciences目前创新药研发管线上共有11款产品,其中包括4个临床一期、3个临床前,以及4个药物发现。进度最快的是IGM-2333,该药是一款CD20\CD3双抗药物,针对肿瘤疾病领域的药物。目前针对边缘区B细胞淋巴瘤、非霍奇金淋巴瘤、套细胞淋巴瘤、滤泡中心淋巴瘤等适应症均处于临床一期试验中。
IGM Biosciences创新药研发管线
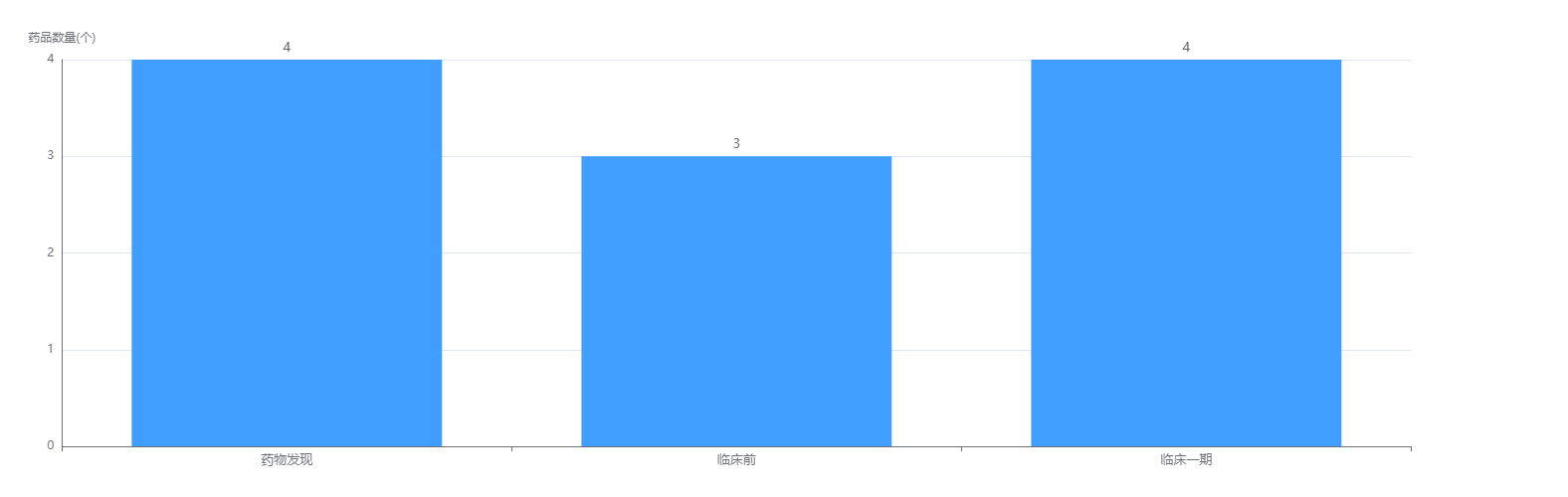
截图来源:药融云全球药物研发数据库
IGM Biosciences 研发管线(部分)
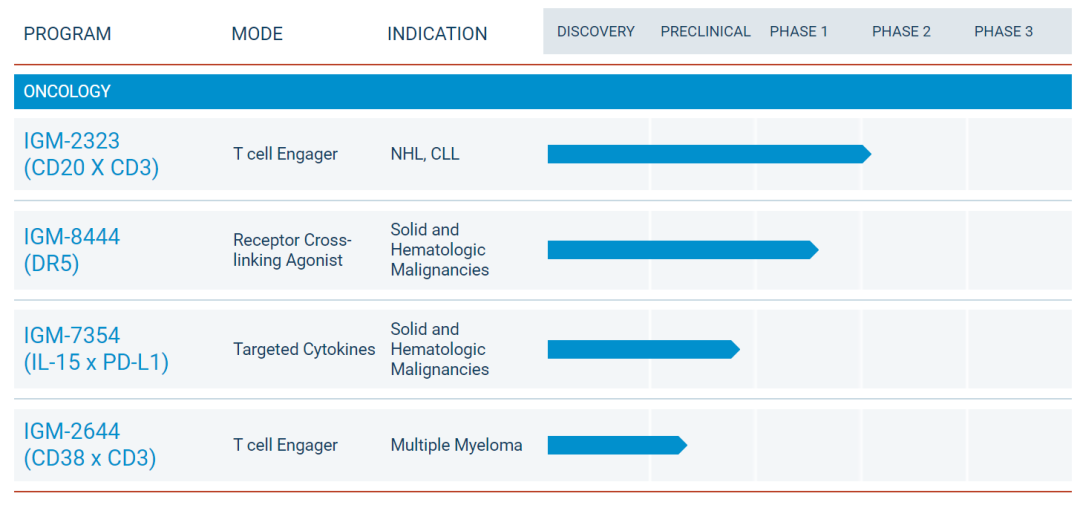
截图来源:IGM Biosciences官网
参考资料:
药融云数据库
想要解锁更多药企创新药信息吗?查询药融云数据库(https://www.pharnexcloud.com/?zmt-mhwz)掌握药企创新药产品布局、基本信息、最新进展、研发阶段、临床试验信息、市场规模与前景,可否投入研发!注册立享15天免费试用和虎年首份医药数据大礼包!

<END>






















































 川公网安备51019002008863号
川公网安备51019002008863号 本网站未发布麻醉药品、精神药品、医疗用毒性药品、放射性药品、戒毒药品和医疗机构制剂的产品信息
本网站未发布麻醉药品、精神药品、医疗用毒性药品、放射性药品、戒毒药品和医疗机构制剂的产品信息
收藏
登录后参与评论
暂无评论