
12月10日,美国临床试验收录网站Clinicaltrials显示,恒瑞医药启动了血管生成素样蛋白3(ANGPTL3)单抗SHR-1918的首个III期研究(SHR-1918-301)。该药物是首款进入III期阶段的国产ANGPTL3单抗。

SHR-1918是恒瑞医药自主研发的血管生成素样蛋白3(ANGPTL3)单克隆抗体,通过抑制 ANGPTL3 的活性,从而降低血清中的甘油三酯(TG)和 LDL-C 水平。
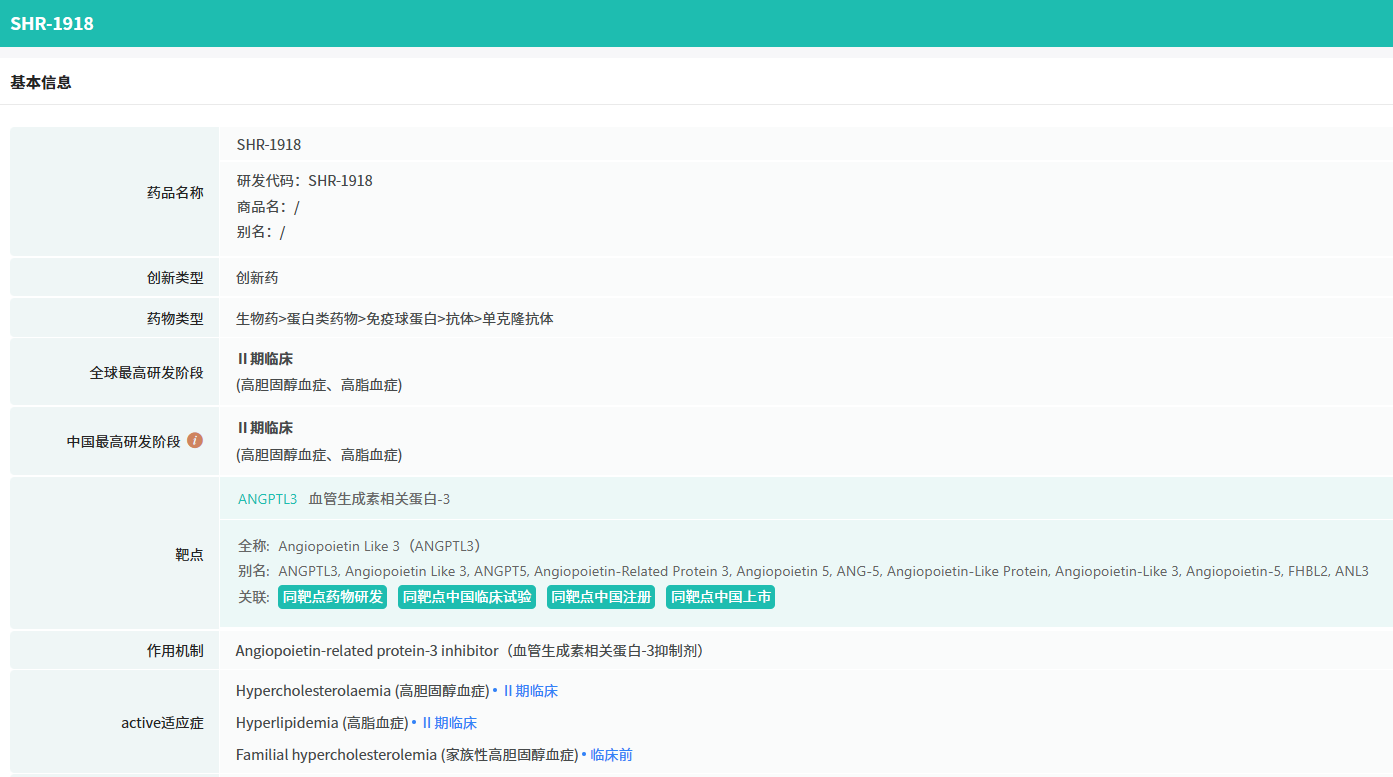
截图来源:摩熵医药数据库(全球药物研发数据库)
2024年欧洲心血管学会(ESC)年会上,恒瑞以口头汇报的形式,公布了 SHR-1918 的 I 期临床研究的积极结果(SHR-1918-101)。研究结果表明,SHR-1918 单次皮下注射在健康受试者中显示出良好的耐受性和药代动力学特性。
目前全球 ANGPTL3 单抗只有 4 款在研,其中再生元的依维苏单抗在 2021 年获 FDA 批准上市,用于 HoFH,这也是 FDA 批准的首个结合并阻断 ANGPTL3 功能的疗法,但此药并未在中国上市。除此之外,其他 3 款均处于临床阶段,恒瑞医药的 SHR-1918 是目前国内首个且唯一一个进入 III 期临床的ANGPTL3 靶向药物。
参考来源:
[1] 恒瑞医药官方披露
[2] 摩熵医药(原药融云)数据库
[3] Clinicaltrials官网
想要解锁更多药物研发信息吗?查询摩熵医药(原药融云)数据库(vip.pharnexcloud.com/?zmt-mhwz)掌握药物基本信息、市场竞争格局、销售情况与各维度分析、药企研发进展、临床试验情况、申报审批情况、各国上市情况、最新市场动态、市场规模与前景等,以及帮助企业抉择可否投入时提供数据参考!注册立享15天免费试用!


































![医药高地:核药!恒瑞医药镥[177Lu]氧奥曲肽注射液获批临床](https://yaorongyun-public.oss-cn-shanghai.aliyuncs.com/images/covers/202302/09/e3938ad9f1d23e2fd043611c4a98c02a.png)














 浙公网安备33011002015279
浙公网安备33011002015279 本网站未发布麻醉药品、精神药品、医疗用毒性药品、放射性药品、戒毒药品和医疗机构制剂的产品信息
本网站未发布麻醉药品、精神药品、医疗用毒性药品、放射性药品、戒毒药品和医疗机构制剂的产品信息
收藏
登录后参与评论
暂无评论