


自2023年7月底Mirus上市RevIT™ AAV Enhancer以来, RevIT™ AAV Enhancer的加入,允许不同血清AAV型别病毒基因组滴度提高1.2-4.9倍,并且在一定程度提升了实心率,使得AAV生产上游成本进一步降低成为可能,降低了基因治疗单剂量成本。由于可轻松灵活的将revIT整合入现有AAV生产工艺工作流程中,不仅可以搭配Mirus TransIT-VirusGEN® GMP 转染试剂,也适配于其他转染试(如PEI),RevIT™ AAV Enhancer得到了国内外AAV客户的广泛认可及好评,GMP级别试剂也按照计划如期上市,用于大规模的AAV GMP生产。
RevIT™ AAV Enhancer于2024年9月30日推出 GMP级别,由ISO 13485体系认证的工厂生产,符合 ISO 20399 以及 USP <1043> 标准。自2023年7月28上市的RevIT™ AAV Enhancer,已证明在不同血清型别、细胞培养基以及转染平台上,可提高至少 2-4 倍病毒滴度;在保持高质量滴度的同时,允许更低质粒 DNA用量,从而大幅度降低AAV病毒生产成本。
产品名称: RevIT™ GMP AAV Enhancer
上市日期:2024年9月30日
产品货号: MIR 8200-GMP
产品规格:200mL 液体

更多RevIT™ AAV Enhancer数据及RevIT™ AAV Enhancer详细信息,请点击查看《新上市RevIT™ AAV Enhancer, 提高AAV产量的又一利器!》
RevIT AAV Enhancer 以及TransIT-VirusGEN 转染试剂产品参数
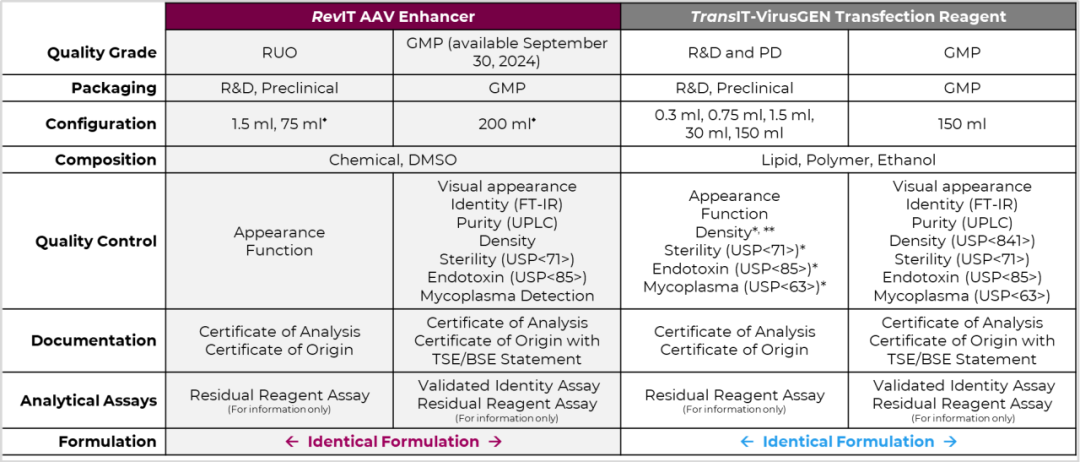
* HDPE材质管/瓶
* 只针对30 mL以及150 mL 规格试剂
**只针对150 mL 规格试剂
GMP支持详情
Residual Reagent Assay残留检测
Regulatory Support Package 法规支持文件
Product Safety Risk Assessment | Supplemental Information产品安全性风险评估| 补充信息
Manufactured and Tested in Alignment with Mirus 生产及检测与Mirus标准体系一致
ISO 13485 QM
Mirus Bio GMP 质量标准
ISO 13485验证体系
Mirus Bio 所开发以及供应的辅助材料(Ancillary material),可用于细胞和基因疗法的 RUO 和 GMP 合规性工艺生产。
Mirus Bio 的质量管理体系通过了 ISO 13485 认证,可用于技术转让以及分销 GMP 级辅助材料。
Mirus Bio 开发及实施以客户为中心的质量管理体系(QMS),可作为值得信赖的合作伙伴,满足细胞和基因治疗客户需求的承诺。以下指导文件为 Mirus Bio 建立质量管理体系所参考的质量标准文件:
ISO 13485:2016, Medical devices – Quality management systems – Requirements for regulatory purposes
ISO 20399:2022, as ancillary materials present during the production of cellular therapeutic products
USP<1043>, with respect to Tier 2 ancillary materials for cell, gene and tissue-engineered product

更多客户案例分享
1.最新线上webinar:Pairing a novel enhancer with transfection reagents to enable high-titer rAAV production
演讲者信息:
Florian Dziopa,MeiraGTx 上游工艺负责人(Director of Upstream Process) ,在MeiraGTx工作的过去六年里,一直致力基于悬浮HEK293细胞瞬转工艺的AAV生产平台优化。
René Gantier,Repligen 高级生物工艺应用研发Director,有着超过二十年的产品开发及工艺纯化经验。
Becky Reese,Mirus Bio研发
该Webinar可以 (线上观看):
了解如何实现病毒载体的生产工艺流程优化提升;
了解 VirusGEN® 转染试剂是如何帮助涉及不同种转染工作流程以及 AAV 血清型的工艺流程,其产量全面提升;
从生产工艺流程角度出发,如何降低细胞和基因疗法的单位剂量成本
简化了从技术评估到工艺生产的整个过程
Bridgebio在该poster中分享了基于AAV5型别,使用TransIT-VirusGEN® 转染试剂以及RevIT™ AAV Enhancer在摇瓶阶段线性放大至200L(125mL摇瓶→2L → 10L → 200L)病毒滴度和实心率数据结果(图左)。与之前工艺相比 (工艺A:PEIPro转染 + Expi293细胞/培养基),替换成TransIT-VirusGEN® 转染试剂的工艺流程 (工艺B:TransIT-VirusGEN® 转染试剂 + Expi293细胞 + BalanCD培养基;工艺C:TransIT-VirusGEN® 转染试剂 + VP2.0细胞 + BalanCD培养基),有着更高的病毒滴度(图右)及更低的宿主DNA和质粒DNA残留。

相关产品信息
产品名称 | 规格 | 货号 |
RevIT™ AAV Enhancer | 1.5 ml | MIR 8000 |
10 x 1.5 ml | MIR 8006 | |
75 ml | MIR 8080 | |
!新上市 RevIT™ GMP AAV Enhancer | 200 ml | MIR 8200-GMP |
VirusGEN® AAV转染试剂及RevIT™ AAV Enhancer | For 1L of Culture | MIR 8007 |
For 10L of Culture | MIR 8008 | |
TransIT-VirusGEN®转染试剂 | 0.3 ml | MIR 6703 |
0.75 ml | ||
1.5 ml | ||
5 x 1.5 ml | ||
10 x 1.5 ml | ||
30 ml | ||
TransIT-VirusGEN® GMP级别转染试剂 | 150 ml | MIR 6845-GMP |
VirusGEN® AAV转染试剂(套装) | 1 kit for 1 L of cell culture | MIR 6750 |
VirusGEN® GMP级别AAV转染试剂(套装) | 1 Kit - for 50 L of cell culture | MIR 6815-GMP |
VirusGEN® LV转染试剂(套装) | 1 kit for 1 L of cell culture | MIR 6760 |
VirusGEN® GMP级别LV转染试剂(套装) | 1 Kit - for 50 L of cell culture | MIR 6825-GMP |
新产品速递
TransIT®-AAViator 转染系统,基于Mirus Bio专利且成熟的聚合物和脂质技术平台上做开发,与单纯基于聚合物(PEI)的转染试剂相比,可进一步提高 AAV 载体的产量,并允许降低一半的质粒 DNA 用量。
TransIT-AAViator 系统由新型 TransIT-AAViator 转染试剂和 RevIT™ AAV 增强剂组成。结合使用后,极大的优化了AAV工艺生产中关键一环-上游转染,最大限度提高 AAV 滴度,更多详情敬请期待。






































 浙公网安备33011002015279
浙公网安备33011002015279 本网站未发布麻醉药品、精神药品、医疗用毒性药品、放射性药品、戒毒药品和医疗机构制剂的产品信息
本网站未发布麻醉药品、精神药品、医疗用毒性药品、放射性药品、戒毒药品和医疗机构制剂的产品信息
收藏
登录后参与评论