
9月13日,宜联生物在2024年ESMO大会上首次展示了YL201(靶向B7H3 ADC)的临床数据,该药物在小细胞肺癌(SCLC)中显示出超过 6 个月的无进展生存期(PFS),并且显示出对多种肿瘤类型的益处。
加拿大玛格丽特公主肿瘤中心的Lillian L Siu教授:“该类药物在小细胞肺癌中均展示了良好的疗效,YL201纳入的样本量最大,数据量最多,而且有效率也是最高的。”
国外媒体ApexOnco的撰稿人Madeleine Armstrong:“YL201看起来在二线及以上的小细胞肺癌中具有特别好的疗效,由于另外两家也公布了数据,跨试验比较非常容易得出结果,确认的客观有效率高达61%使YL201处于一个颇有竞争力的地位,加上待确认的缓解例数,总客观有效率可达到68%。”
DCR高达84%,有效治疗多种肿瘤
截至2024年8月9日,在中国和美国进行的I期研究(NCT05434234 & NCT06057922)中,共有312名患者参与了针对晚期实体瘤的YL201药物的剂量递增(49例)和扩展研究(263例)。首先进行的剂量爬坡试验,评估了0.8mg/kg,1.6 mg/kg,2.0 mg/kg,2.4 mg/kg,2.8 mg/kg和3.0 mg/kg,得到的最大耐受剂量为2.8 mg/kg,结合疗效和安全性,最终确定了2.0和2.4 mg/kg 两个推荐剂量。
随后,在多瘤种多线治疗失败后的实体瘤患者中进行了扩展试验,覆盖了广泛期小细胞肺癌(79例)、鼻咽癌(75例)、野生型非小细胞肺癌(腺癌29例、鳞癌14例和淋巴上皮瘤样癌25例)以及食管鳞癌37例。60%的患者此前已接受过至少2线的治疗。
研究结果显示,截至2024年08月09日,中位随访时间为5.4个月。所有患者的整体有效率达到45%,疾病控制率(DCR)高达84%,且有46%的患者仍在继续接受治疗。

在各类实体瘤中的相关数据:
广泛期小细胞肺癌:患者的有效率达到68%,其中61.1%的患者疗效得到确认。中位无进展生存期达到6.2个月,中位疾病缓解期达到了5.7个月。同时,对于脑转移的广泛期小细胞肺癌患者,YL201也取得了令人鼓舞的疗效,有效率达到52%,中位无进展生存期为5.3个月。这些入组的小细胞肺癌患者既往全部接受过含铂双药化疗,95%的患者既往接受过抗PD-1免疫治疗,YL201在多线失败后的小细胞肺癌人群中疗效非常显著。
鼻咽癌:该研究纳入的75例鼻咽癌病人全部接受过含铂双药化疗和抗PD-1免疫治疗,75%的病人接受过至少2线或以上系统治疗。YL201的整体有效率达到49%,中位无进展生存期为7.2个月,远高于经治鼻咽癌患者通常的10%-30%的有效率。在接受过大于两线治疗的鼻咽癌患者,YL201的表现更好,客观有效率达到51%,中位无进展生存期达到7个月。
肺淋巴上皮瘤样癌:一种较为罕见的非小细胞肺癌亚型,该类型的肺癌与EB病毒感染相关,常见于鼻咽癌流行区,如华南地区。肺淋巴上皮瘤样癌的患者对YL201的治疗响应率也非常高,有效率达到61%,中位无进展生存期达到8.1个月。鼻咽癌和肺淋巴上皮瘤样癌上的高响应率能提示YL201对EB病毒感染相关的肿瘤具有广泛的疗效。在非小细胞肺癌中,腺癌患者的疗效同样令人满意,后线治疗的患者能够达到约30%的有效率。在安全性评估方面,ADC药物均有治疗窗口较窄,有一定治疗相关毒性的特点。尤其是在以I型拓扑异构酶抑制剂为载体a的ADC药物中,血液学毒性发生率均不低。本研究同样观察到51%的3级及以上药物相关不良反应。这一比例与其他已报道的ADC药物相比处于相当水平,甚至更低。安全性事件以血液学毒性为主,与其他同类药物类似,具体包括白细胞计数下降、贫血症状以及血小板减少。值得注意的是,这些毒性反应均可进行有效管理和控制。
考虑到B7H3作为免疫相关靶点,研究者对于可能引发的免疫不良反应保持高度关注。欣慰的是,本研究中免疫性间质性肺炎的发生率较低,不足1%,进一步证实了YL201在安全性方面的可控性。
综上,YL201在本次I期临床研究中为实体瘤患者后线治疗带来了令人鼓舞的疗效改善,且具有可控的安全性和耐受性。
B7H3 ADC:SCLC激战正酣,YL201响应率占优
B7H3作为一种跨膜蛋白,和PD-L1同属B7家族。B7H3可在多个瘤种(如肺癌、前列腺癌、食管癌等)中过表达,已被证明与肿瘤免疫抑制和不良预后相关,从而使B7H3成为抗肿瘤治疗领域的潜力靶点。
然而,B7H3靶点的研发却并非一番风顺。从2019年CD3/B7H3双抗MGD009的Ⅰ期临床试验出现肝脏毒性被FDA叫停,到2022年B7H3单抗MGA271在II期临床试验中因遭遇重大挫折而宣布停止,再到靶向B7H3的RDC药物131I-omburtamab因试验未达中位OS而被16:0反对上市等等,众多研究在B7H3靶点上接连翻车。B7H3单抗、双抗、RDC 接连失利之后,B7H3 ADC成为最有潜力跑赢的研发管线。根据相关数据库数据显示,目前在研的B7H3 ADC药物约33种,有约14款药物进入临床在研阶段。
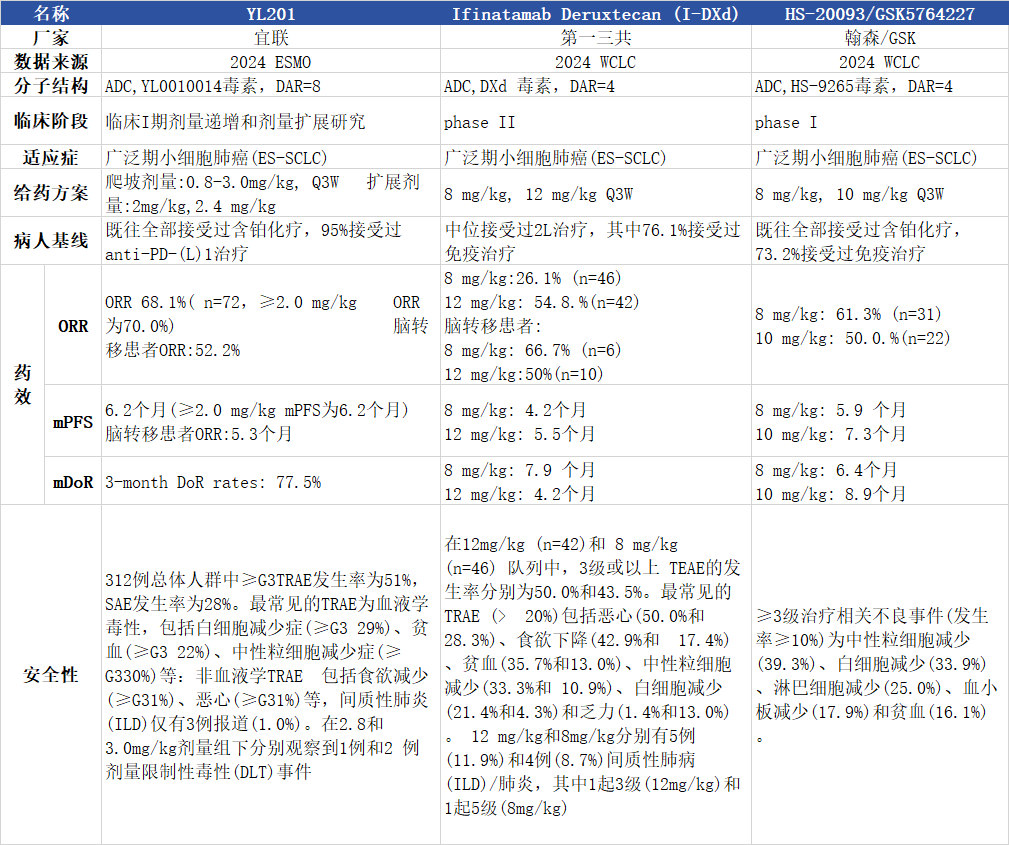
在小细胞肺癌领域,Amgen的DLL3/CD3双抗已经获批上市,开创了实体瘤TCE治疗的新篇章,而在ADC领域,随着近几年相关靶点药物的开发,SCLC临床布局竞争也相当激烈。其中B7H3也终于凭借SCLC逐步走向正途,包括第一三共的DS7300(i-Dxd),HS-20093等此前均已展示出不错的疗效:第一三共基于DXd模数转换器技术平台研发的DS-7300a,是目前首个推进到临床III期阶段的B7H3 ADC。2024 WCLC大会上公布的2期临床试验数据显示,对于经治的广泛期小细胞肺癌(ES-SCLC)患者而言,疾病控制率(DCR)高达90.5%,客观缓解率(ORR)则达到54.8%。此外,GSK/翰森制药的B7H3-ADC(HS-20093)也紧随其后,初期临床数据良好。2024 WCLC大会上公布的Ⅰ期(ARTEMIS-001)中,ORR 61.3%(8mg/kg)及50%(10mg/kg),中位PFS5.9月,中位DOR6.4月。宜联YL201与二者对比数据如下图所示,介于毒素活性YL0010014>HS-9265>DXd,且宜联的DAR为8而其余两者DAR为4,所以YL201的爬坡剂量明显低于I-DXd和HS-20093。- 药效方面,YL201展示出了最高的响应率,mPFS与HS-20093不分伯仲,优于I-DXd。
- 安全性方面,YL201与HS-20093的血液毒性旗鼓相当,略强于I-DXd,但是比I-DXd拥有更低的ILD比例。 YL201、DS7300、HS-20093在SCLC临床数据对比
宜联生物TMALIN®技术平台,可实现DAR值达8宜联生物作为一家专注于抗体偶联药物(ADC)和相关技术的创新药物开发公司,基于TMALIN技术平台打造了丰富的ADC管线,并实现了包括与BioNTech、Roche、再鼎、复宏汉霖、和铂(海外授权Pfizer)等多起合作。公司开发的最新一代具有自主知识产权的Tumor Microenvironment Activable LINker-payload(TMALIN®)新型抗体偶联药平台技术,可利用肿瘤微环境和传统溶酶体在胞外胞内实现双重裂解机制、兼具高水溶性、高均一性、高体内外稳定性以及肿瘤组织富集特性。目前已有多款基于该平台的ADC产品进入临床试验阶段。TMALIN技术形成的ADC具有许多优点,已在多个体内药效模型与大动物毒理评价实验中,展现出相比于现有ADC技术更宽的药物治疗窗。具体优势包括:1)具有极高的全身循环稳定性,可减少有效载荷在非靶组织中的脱落以及有效载荷在无靶组织中脱落所引起的“偏离靶”毒性。2)具有优异的溶解性和优异的化学稳定性,不存在传统ADC中马来酰亚胺连接方式引起的可逆Michael加成反应,可以获得高均匀度的ADC(DAR=8.0),并实现定点定量耦合。YL201采用了宜联生物的TMALIN®技术平台创新的TMALIN可裂解连接子设计,载体是I型拓扑异构酶抑制剂,DAR值达到了8。值得一提的是,在研的4个B7H3的抗体偶联药物,包括DS-7300,HS-20093,MHB008C和YL201,都是以I型拓扑异构酶抑制剂作为载体,而YL201的DAR值达到了8,其余3项都是4。
凯莱英生物作为宜联生物的战略合作伙伴,协助推进宜联生物 YL201的关键临床样品研发和生产。凯莱英生物在凯莱英医药集团毒素-连接子业务能力加持下,具备抗体 、毒素-连接子和偶联等多环节在内的ADC一站式CDMO服务能力,加速赋能全球客户偶联药物创新。
参考资料:
1、新药启航:B7-H3 ADC:宜联 vs. 翰森 vs. 第一三共,谁是同类最佳?2、医悦汇:2024ESMO | 新型B7H3抗体偶联药物初次亮相即创多个瘤肿后线疗效新高:张力、赵洪云教授团队口头汇报YL-201初步结果
3、宜联生物官方网站
<END>
*版权声明:本网站所转载的文章,均来自互联网,旨在传递更多信息。鉴于互联网的开放性和文章创作的复杂性,我们无法保证所转载的所有文章均已获得原作者的明确授权。如果您是原作者或拥有相关权益,请与我们联系,我们将立即删除未经授权的文章。本网站转载文章仅为方便读者查阅和了解相关信息,并不代表我们认同其观点和内容。读者应自行判断和鉴别转载文章的真实性、合法性和有效性。












































 浙公网安备33011002015279
浙公网安备33011002015279 本网站未发布麻醉药品、精神药品、医疗用毒性药品、放射性药品、戒毒药品和医疗机构制剂的产品信息
本网站未发布麻醉药品、精神药品、医疗用毒性药品、放射性药品、戒毒药品和医疗机构制剂的产品信息
收藏
登录后参与评论