
癌症的传统治疗方法以以手术、化疗和放疗为主。近年来,CAR-T疗法因其对于肿瘤细胞更具有杀伤力、靶向性更强,治疗更持久而备受关注。
自 2017年首次获批以来,已有6款CAR-T疗法获美国FDA批注用于治疗白血病和淋巴瘤等血液类癌症。然而,CAR-T疗法在占据癌症绝大多数的实体瘤中却疗效不佳。主要原因是实体瘤细胞的高度异质性,即使接受CAR-T细胞治疗后,仍有一些癌细胞能够逃逸免疫系统监测 。
2024年3月13日,一项由哈佛医学院、麻省总医院及丹娜·法伯癌症研究所的研究人员共同完成的研究在《新英格兰医学杂志》上发表,论文名为“Intraventricular CARv3-TEAM-E T Cells in Recurrent Glioblastoma”。
该研究介绍了3名复发性胶质母细胞瘤患者在接受CARv3-TEAM-E T细胞新疗法后要么出现肿瘤消退,要么出现肿瘤显著缩小;且患者均对治疗耐受性良好。
这一研究为CAR-T疗法治疗实体瘤带来了突破进展。
如今,我国已有超25款CAR-T产品处于研发阶段,多家领军企业如传奇生物、科济药业、药明巨诺等积极布局新一代CAR-T及异体CAR-T技术。据不完全统计,国内已有27家公司布局实体瘤CAR-T疗法。
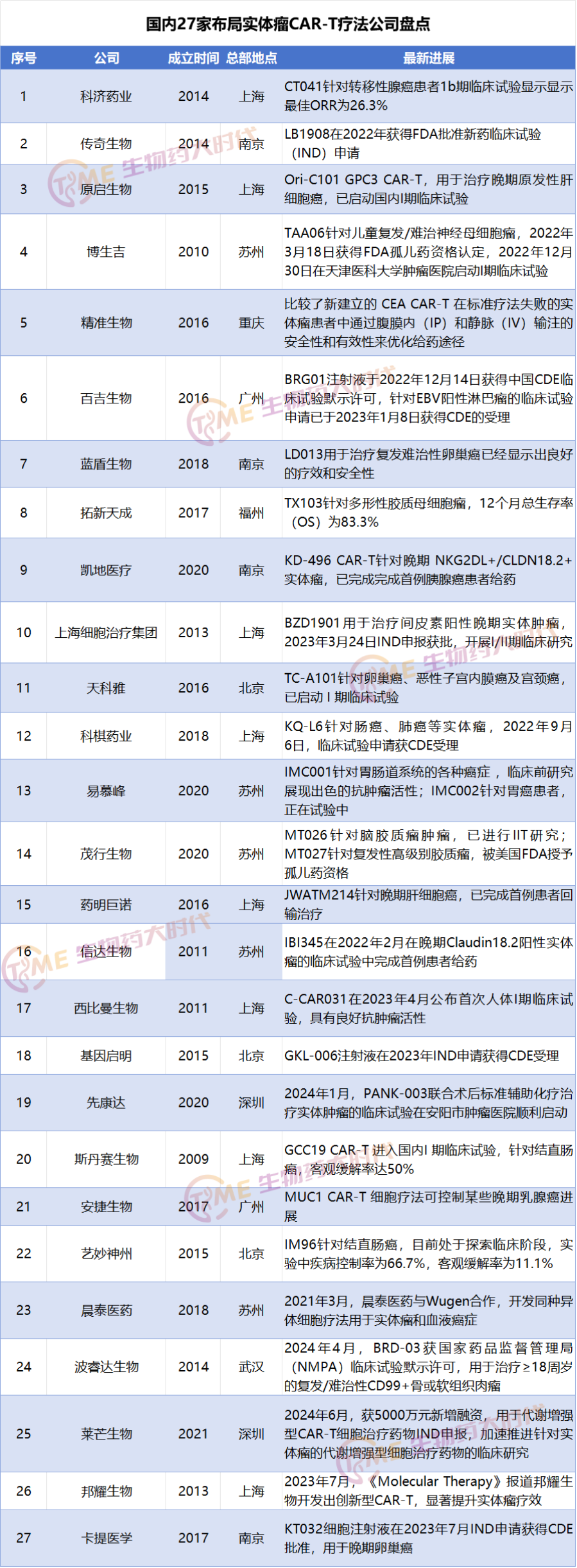
来源:生物药大时代整理
一、传奇生物
传奇生物成立于2014年,是中国CAR-T海外上市第一股,全球员工总数逾1500人。南京传奇生物正在开发广泛应用的细胞疗法组合,探索了多种具备创新性和突破性技术平台,用于治疗血液系统恶性肿瘤和实体肿瘤,包括:自体CAR-T、同种异体非基因编辑细胞CAR-T、自然杀伤细胞(NK)和γδ T 细胞。
LB1908是一种通过高亲和力VHH抗体选择性靶向Claudin 18.2的CAR-T疗法,用于治疗复发性或难治性胃癌、食管癌(包括胃食管连接部)或胰腺癌成人患者。2022年6月3日,传奇生物在美国正式宣布,美国食品药品管理局(FDA)批准了其新药临床试验(IND)申请,以评估在美国进行的LB1908的I期临床试验。
研发管线

二、科济药业
科济生物成立于2014年,是一家在港交所上市、在中国及美国拥有业务的生物制药公司,专注于实体瘤和血液恶性肿瘤的创新CAR-T疗法。科济药业无疑是国内实体瘤CAR-T疗法管线布局最多、进展最为迅速的企业。
其靶向CLDN18.2蛋白的自体CAR-T细胞候选产品CT041,主要治疗胃癌/食管胃结合部腺癌(GC/GEJ)及胰腺癌(PC),是全球唯一已获得美国FDA和中国国家药监局及加拿大卫生部的IND/CTA批准并正在进行临床试验研究的靶向CLDN18.2的CAR-T细胞候选产品。
2024年2月,2024 ASCO GI会议上CT041研究成果亮相。其I期临床试验显示最佳ORR为26.3%,中位缓解持续时间(DoR)为3.7个月,临床获益率(CBR)为42.1%。
研发管线
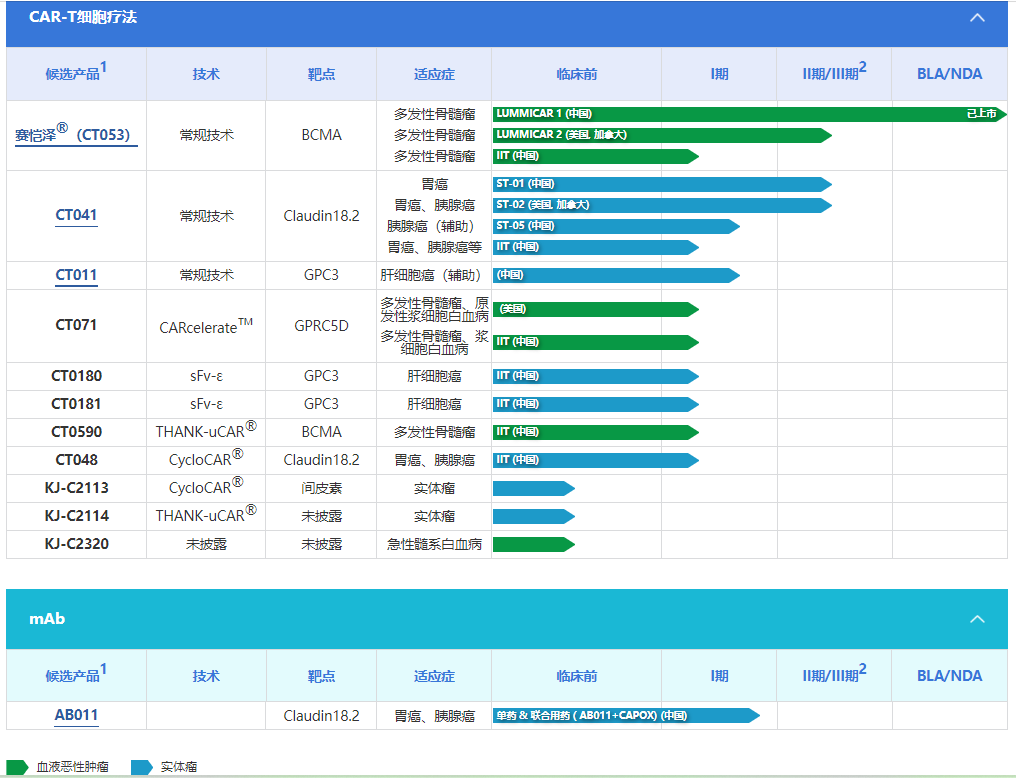
三、药明巨诺
药明巨诺的细胞免疫治疗产品开发平台涵盖了血液肿瘤、实体肿瘤和自身免疫性疾病的细胞免疫治疗产品管线。
JWATM204适应症为晚期肝细胞癌,2022年7月4日,JWATM204启动I期临床研究。初步临床前研究结果表明,JWATM204在肝细胞癌治疗方面表现出良好的临床开发潜力,表现出GPC3单克隆抗体的高亲和力和高特异性的同时,还拥有更好的安全性。JWATM214用于治疗晚期肝细胞癌,2023年2月28日启动临床研究,且完成了首例患者的回输治疗。
研发管线
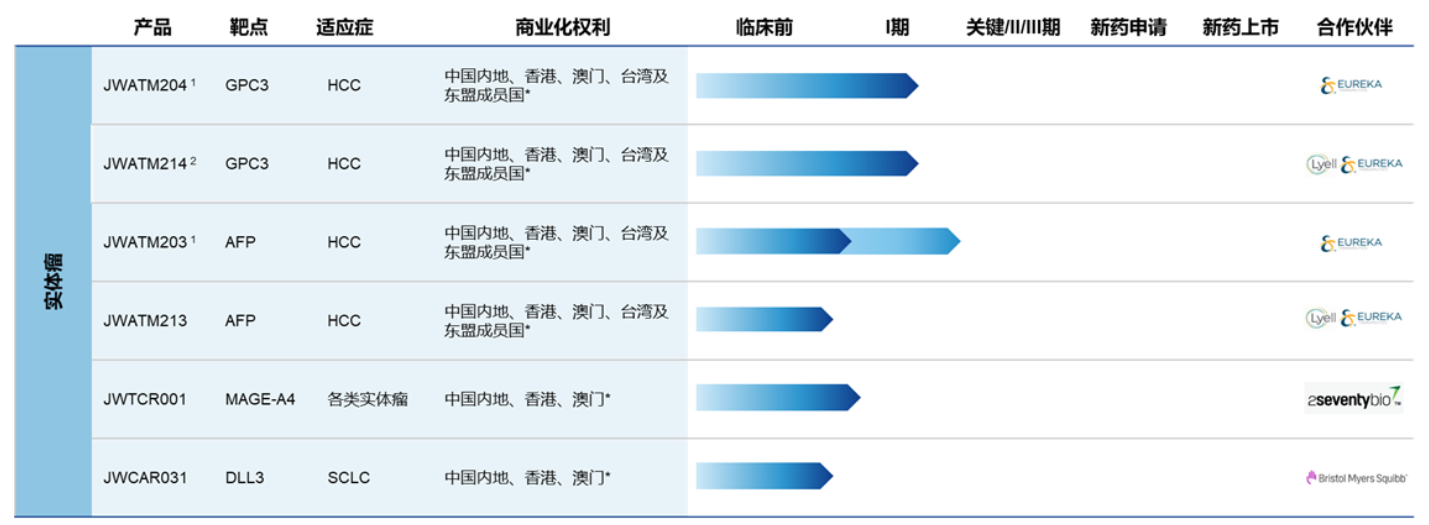
四、精准生物
精准生物技术有限公司主营基因与细胞药物开发应用,目前已成为国内CAR-T/NK领域头部企业之一。
C-13-60是一款靶向CEA的CAR-T细胞注射液,用于治疗≥18周岁CEA阳性晚期恶性实体肿瘤患者。2022年9月22日,C-13-60临床试验申请获得CDE受理,为CDE受理的我国首个靶向CEA的CAR-T产品。
研发管线
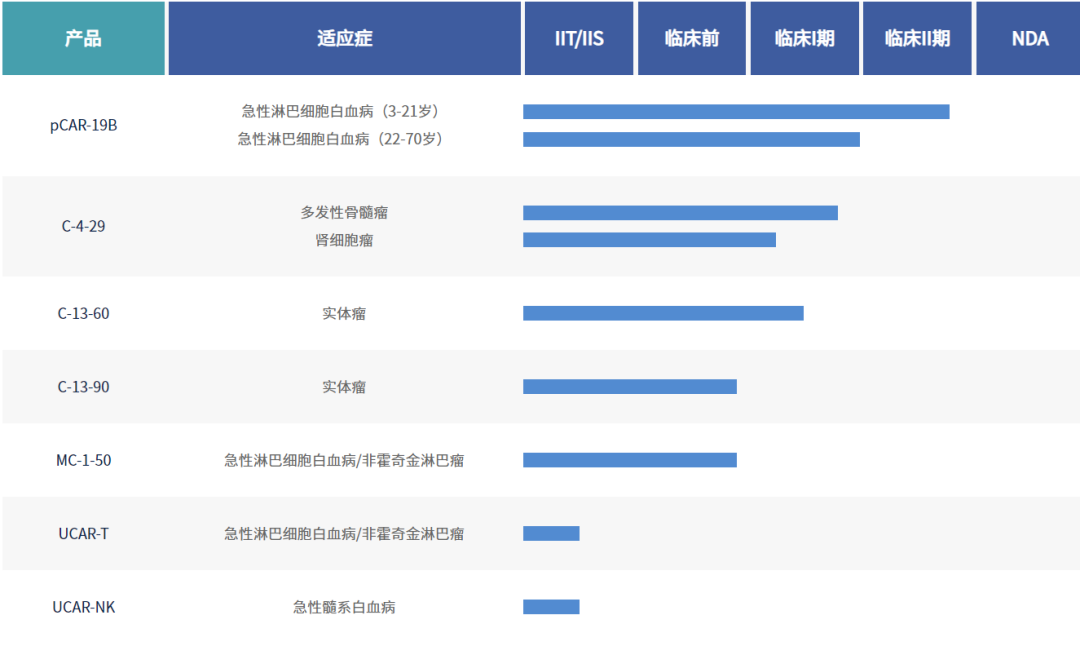
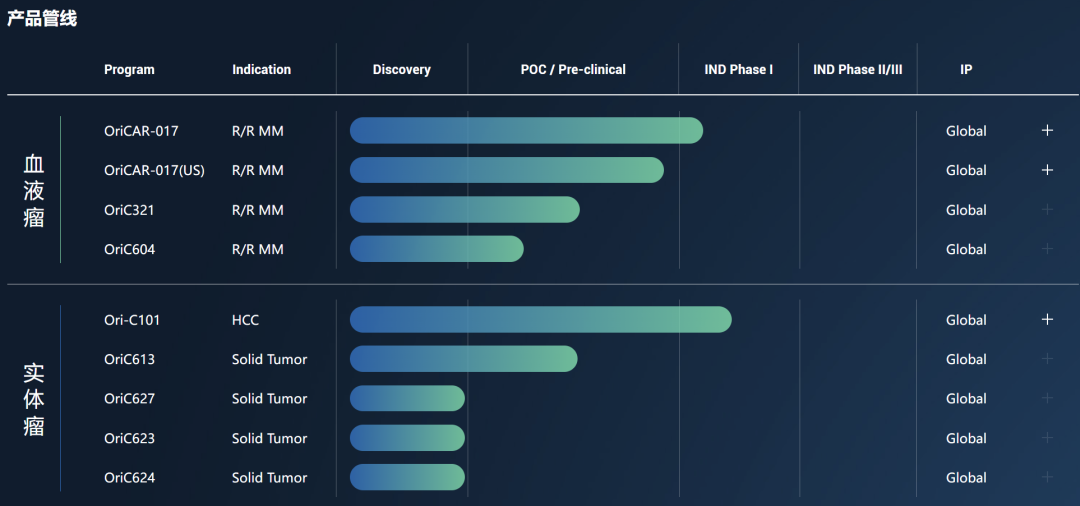
五、原启生物
原启生物运用自主创新技术平台开发肿瘤细胞免疫治疗产品,构建了基于肿瘤细胞免疫治疗的Ori®Ab、Ori®CAR等多个专利技术平台,并从抗体的筛选和优化、肿瘤免疫微环境改善、T细胞高效浸润与持久杀伤能力等方面着手突破了治疗实体肿瘤的疗效瓶颈。
2022年09月21日,Ori-C101注射液临床试验(IND)申请正式获批,适应症为晚期肝细胞癌,这标志着原启生物首个自主开发靶向GPC3(Glypican-3)治疗晚期肝癌的创新药物即将进入国内注册临床试验阶段。
研发管线
六、拓新天成
拓新天成关注实体肿瘤的免疫治疗,应用基因工程、单克隆抗体等技术对免疫细胞(包括T细胞、NK细胞)进行基因修饰和改造,形成抗肿瘤药物。
2022年8月25日,拓新天成TX103嵌合抗原受体T细胞(CAR-T细胞)注射液获得一项临床试验默示许可,拟开发用于TX103阳性、既往经标准治疗失败或发生不可耐受毒性、经病理确诊的晚期实体瘤患者。
七、天科雅
天科雅是众多免疫细胞疗法公司中专注于实体瘤的公司之一,该公司成立于 2016 年,同时研发 CAR/TCR-T 平台。据透露,该公司目前有近十个研发管线,主要适应症包括晚期复发转移性宫颈癌、鼻咽癌、肺鳞癌、卵巢癌、子宫内膜癌及脑癌等多个肿瘤。天科雅的最新一期融资是在 2019 年 4 月完成的 B 轮融资。
2022年9月11日,天科雅生物“首个用于泛妇科肿瘤的CAR-T 细胞免疫疗法”,在欧洲肿瘤内科学会上报告了临床前研发及初步的临床试验结果,启动了TC-A101用于复发性和转移性卵巢癌,子宫内膜癌及宫颈癌治疗的 I 期临床试验,以评估这种抗 ALPP CAR-T 的安全性、最大耐受剂量和临床疗效。
研发管线

八、西比曼生物
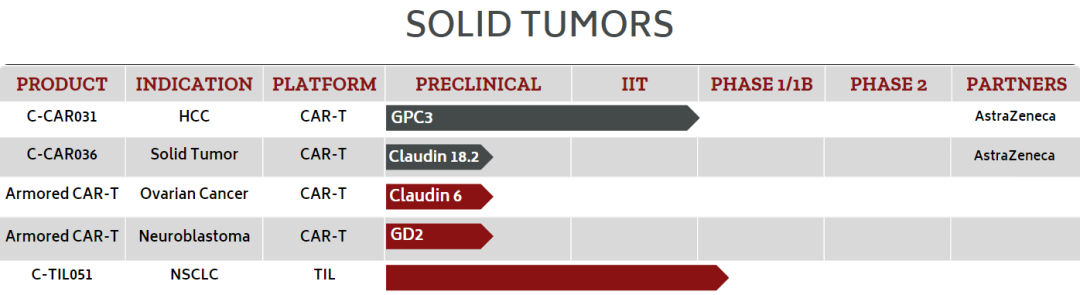
西比曼生物科技开发治疗血液和实体肿瘤的免疫细胞治疗产品。西比曼拥有三个主要的细胞技术平台,分别是自体嵌合抗原受体T细胞(CAR-T)、第四代armored CAR-T和肿瘤浸润淋巴细胞(TIL)的多样化的肿瘤免疫细胞治疗平台。
2023年4月17日,西比曼生物科技宣布在2023年美国癌症研究协会(AACR)年会上发布了其C-CAR031产品的首次人体(FIH)I期临床试验数据,数据显示由阿斯利康设计的新型靶向Glypican 3(GPC3)的细胞疗法C-CAR031具有良好的抗肿瘤活性。
研发管线
九、基因启明
基因启明创立于2015年,专注于iNKT免疫细胞疗法研究,目前已研发出对肝癌等多种恶性肿瘤的免疫细胞产品和治疗方法。
2023年2月14日,据CDE官网显示,基因启明的“GKL-006注射液”IND申请获得受理。
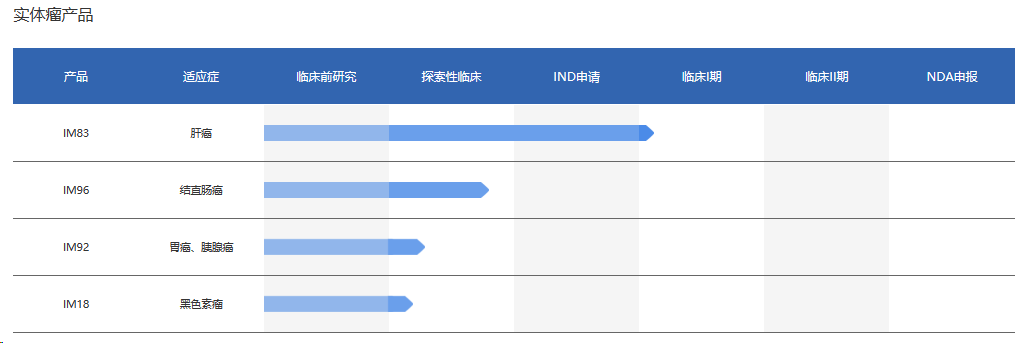
十、艺妙神州
艺妙神州自主研发的IM96是一款靶向GUCY2C(GCC)的CAR-T细胞疗法。根据此前艺妙神州在2023年欧洲肿瘤内科学会(ESMO)年会上公布的I期数据,在治疗晚期转移性结直肠癌患者的试验中,疾病控制率为66.7%,客观缓解率为11.1%,达到部分缓解的1例患者至今11个月仍持续缓解。安全性方面,所有入组患者未观察到神经毒性综合征和≥3级的细胞因子释放综合征。
研发管线
参考资料:公开资料、官网
<END>
想要解锁更多药企信息吗?查询药融云数据库(vip.pharnexcloud.com/?zmt-mhwz)掌握药企公司基本信息、投融资情况、产品管线分布、药物销售情况与各维度分析、药物研发情况、年度报告、最新进展动态、临床试验信息、市场规模与前景等,以及帮助企业抉择可否投入时提供数据参考!注册立享15天免费试用!
















































 浙公网安备33011002015279
浙公网安备33011002015279 本网站未发布麻醉药品、精神药品、医疗用毒性药品、放射性药品、戒毒药品和医疗机构制剂的产品信息
本网站未发布麻醉药品、精神药品、医疗用毒性药品、放射性药品、戒毒药品和医疗机构制剂的产品信息
收藏
登录后参与评论
暂无评论