
资金是企业的生命线,药物研发也不可一味去烧钱。不同类型制药企业对新药的可承担风险能力不一,期待企业理性布局与扎实深耕某一模块。
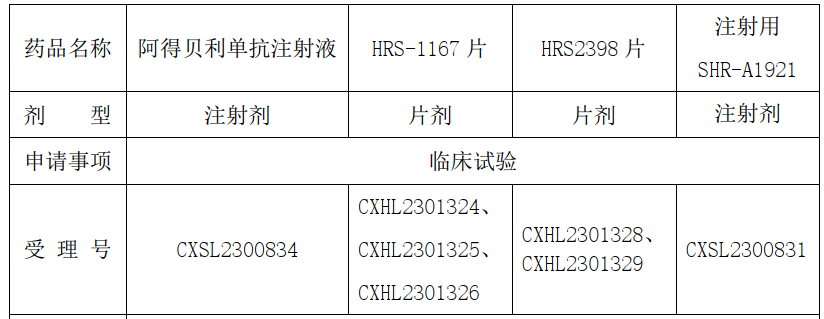
药融云数据监测显示:近期,头部企业的HRS2398 联合抗肿瘤疗法治疗晚期实体肿瘤的开放、多中心Ⅰb/Ⅱ 期临床研究获准在中国开展。其中涉及多种联用治疗,投入不菲。
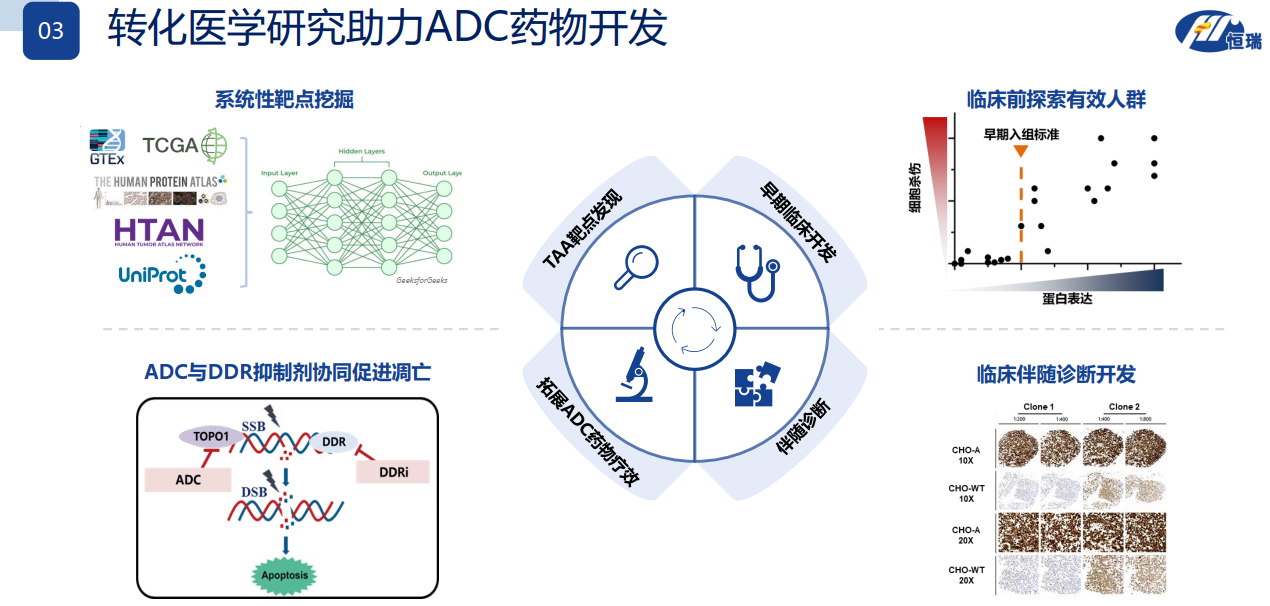
ADC与DDR协同促进凋亡
1.HRS-1167片
其中,HRS-1167片为恒瑞医药自主研发且具有知识产权的高选择性、高活性、可口服的PARP1小分子抑制剂,属于第二代PARP抑制剂。多聚腺苷二磷酸核糖聚合酶(PARP)是修复DNA损伤的关键,第一代PARP抑制剂已被证明对同源重组修复缺陷(HRR)阳性的肿瘤是有效的,例如带有BRCA突变的乳腺癌、卵巢癌、前列腺癌和胰腺癌。与第一代PARP抑制剂相比,HRS-1167对PARP1的选择性更高、亲和力更强,且可诱导DNA捕获。HRS-1167目前处于早期临床开发阶段,有潜力作为单一疗法和联合疗法治疗更多患者,包括此前无法应用PARP抑制剂的肿瘤患者。经查询,国内外暂无同类产品获批上市。截至目前(2024年3月18日),HRS-1167片相关项目累计已投入研发费用约4,567万元人民币。
(2023年10月,德国默克与恒瑞医药达成战略合作,德国默克将获得在中国大陆以外的全球范围内开发、生产和商业化HRS-1167的独家权利。该协议还包括恒瑞自主研发的Claudin-18.2抗体药物偶联物(ADC)SHR-A1904的独家选择权。根据协议条款,恒瑞将获得1.6亿欧元的首付款、高至9000万欧元的技术转移费和行权费,以及研发里程碑付款、销售里程碑付款。以上潜在的付款总额可能高达14亿欧元。除此之外,默克还将向恒瑞支付高至两位数百分比的销售提成。具体条款如下图)

BD license out交易条款模版
2.注射用SHR-A1921
注射用SHR-A1921为靶向TROP2肿瘤相关抗原的抗体药物偶联物(ADC),通过与肿瘤细胞表面的靶抗原结合,使得药物被内吞进入细胞后释放小分子毒素杀伤肿瘤细胞。国内已有一款同类产品获批上市,多个同类药物处于临床开发阶段,适应症以晚期恶性肿瘤为主。截至目前,注射用SHR-A1921相关项目累计已投入研发费用约7,813万元人民币。
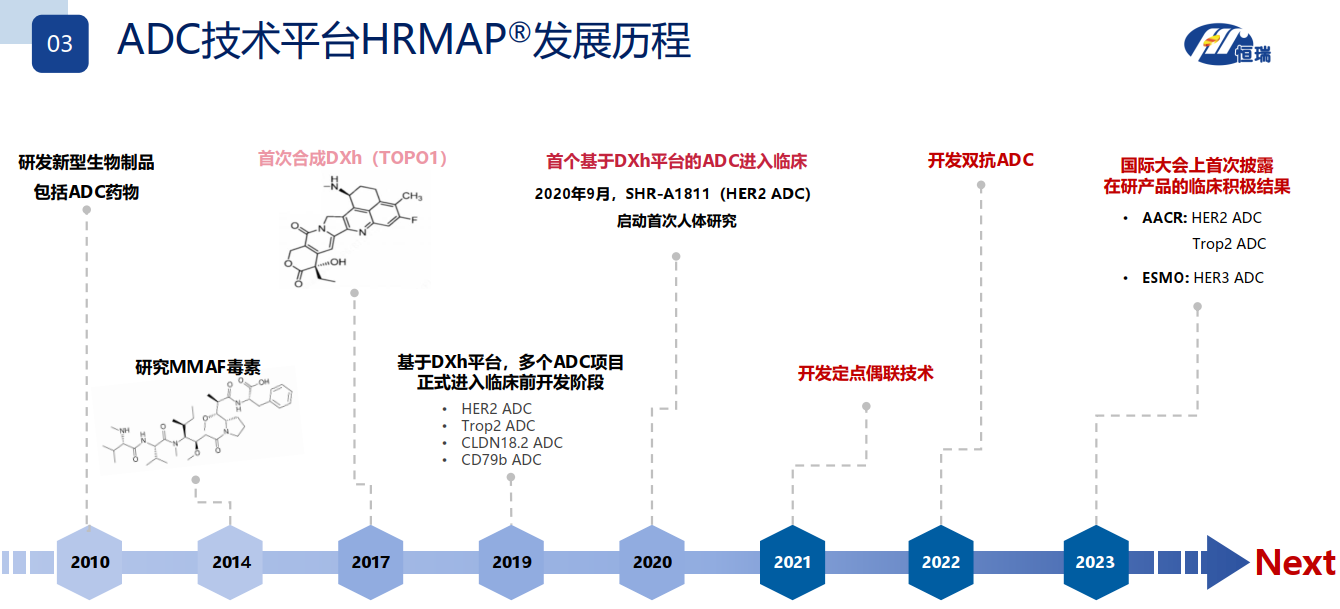
药融圈获悉:恒瑞医药模块化ADC创新平台(HRMAP),经过10年的ADC研发积累。恒瑞成为国内在热门靶点上布局进展相对靠前、兼具诸多差异化ADC产品的企业。

3.HRS2398片
HRS2398片为公司自主研发的新型、高效、口服的ATR抑制剂,能够有效抑制ATR激酶活性,加剧DNA双链损伤,抑制细胞增殖,发挥抗肿瘤作用。HRS2398片目前正处于早期临床开发阶段,有潜力作为单一疗法和联合疗法治疗更多肿瘤患者。目前全球尚未有同靶点药物获批上市。截至目前,HRS2398片相关研发项目累计已投入研发费用约为4,029万元人民币。(公司同样还有HRS2398缓释片在研发中)
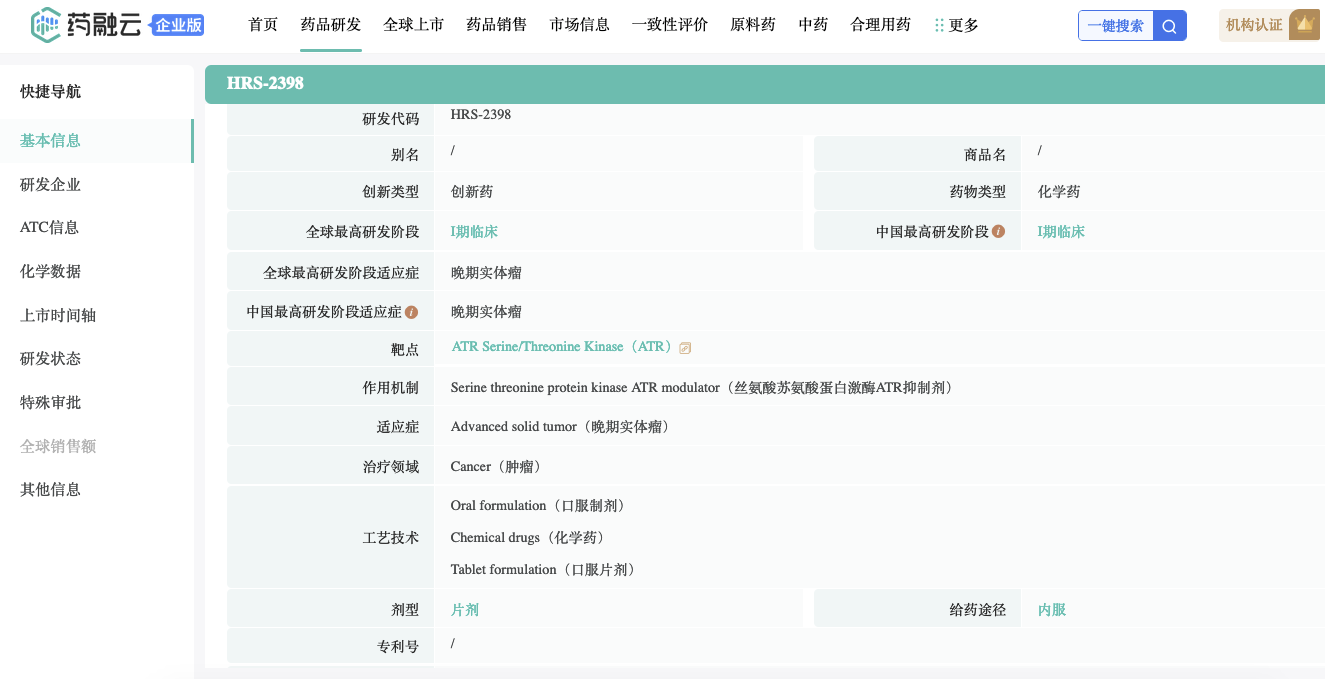
截图自药融云数据库
4.阿得贝利单抗
阿得贝利单抗是公司自主研发的人源化抗 PD-L1 单克隆抗体,能通过特异性 结合 PD-L1 分子从而阻断导致肿瘤免疫耐受的 PD-1/PD-L1 通路。阿得贝利单抗注射液已于 2023 年 3月获批上市,获批的适应症为与卡铂和依托泊苷联合用于广泛期小细胞肺癌患者 的一线治疗。经查询,2022 年 Atezolizumab、Avelumab 和 Durvalumab 全球销 售额合计约为 73.46 亿美元。其他适应症继续开发中,截至目前,阿得贝利单抗注射液相关项目累计已投入研发费用约 5.64亿元人民币。
参考:
NMPA/CDE;
药融云数据;
FDA/EMA/PMDA;相关公司公开披露;恒瑞医药:恒瑞医药关于获得药物临床试验批准通知书的公告,20240319;https://data.eastmoney.com/notices/detail/600276/AN202403181626971155.html;
Current status and future promise of next-generation poly (ADP-Ribose) polymerase 1-selective inhibitor AZD5305. doi: 10.3389/fphar.2022.979873;
<END>
要解锁更多企业药品研发信息吗?查询药融云数据库(vip.pharnexcloud.com/?zmt-mhwz)掌握药品各国上市情况、药品批文信息、销售情况与各维度分析、市场竞争格局、一致性评价情况、集采中标情况、药企申报审批信息、最新动态与前景等,以及帮助企业抉择可否投入时提供数据参考!注册立享15天免费试用!























































 川公网安备51019002008863号
川公网安备51019002008863号 本网站未发布麻醉药品、精神药品、医疗用毒性药品、放射性药品、戒毒药品和医疗机构制剂的产品信息
本网站未发布麻醉药品、精神药品、医疗用毒性药品、放射性药品、戒毒药品和医疗机构制剂的产品信息
收藏
登录后参与评论
暂无评论