据《药融云医药行业观察周报》数据统计,在2023.05.15-2023.05.21期间,共有62项仿制药注册申请获CDE承办,其中新注册分类上市申请受理号53项(包括化药3类,4类,5.2类),一致性评价申请受理号9项;共9个品种通过一致性评价仿制药(按受理号计11项),25个品种视同通过一致性评价(按受理号计31项)。
其中,首次过评/视同过评品种有11个,分别是贝前列素钠片、尼莫地平注射液、美司钠注射液、复方利多卡因乳膏、丙戊酸钠口服溶液、奥拉帕利片、沙格列汀二甲双胍缓释片(Ⅰ)、沙格列汀二甲双胍缓释片(Ⅲ)、丁苯那嗪片、去氧孕烯炔雌醇片、甲钴胺分散片;涉及科伦药业、恒瑞医药、齐鲁制药、海思科制药、福元医药等10家企业。
本周首次过评/视同过评品种
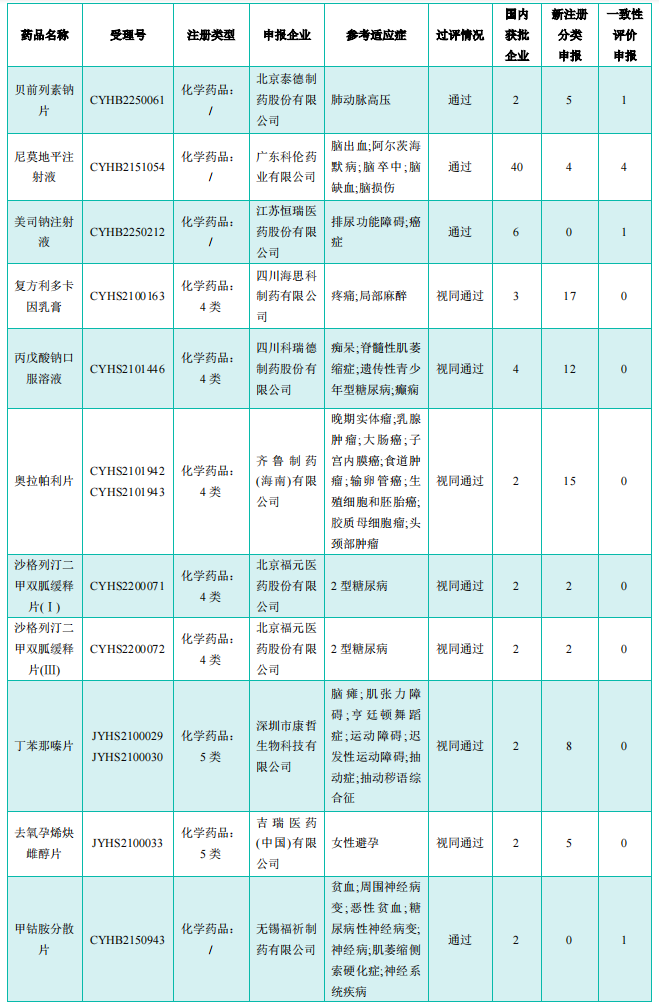
图片来源:《药融云医药行业观察周报》
一、美司钠注射液——化疗“减”毒用药
恒瑞医药的美司钠注射液通过仿制药质量和疗效一致性评价,成为国内该品种“首仿”过评产品。美司钠注射液,用于预防氧氮磷环类化疗药物(环磷酰胺、异环磷酰胺、曲磷胺)引起的泌尿道毒性,尤其是既往接受小骨盆放疗、既往使用异环磷酰胺、环磷酰胺或曲磷胺治疗导致膀胱炎或存在泌尿道疾病史的高危患者。
药融云数据库显示,美司钠注射液的原研企业为德国爱斯达制药,最初于1979年12月在德国获批上市,后于1988年12月在美国上市,2002年7月,获准进口中国。恒瑞医药研发的美司钠注射液于2020年启动该品种的一致性评价工作,2022年4月获得药审中心承办,从承办到通过仿制药一致性评价总耗时400天。美司钠注射液已进入国家基药目录和医保目录。
恒瑞医药美司钠注射液过评审评时间轴
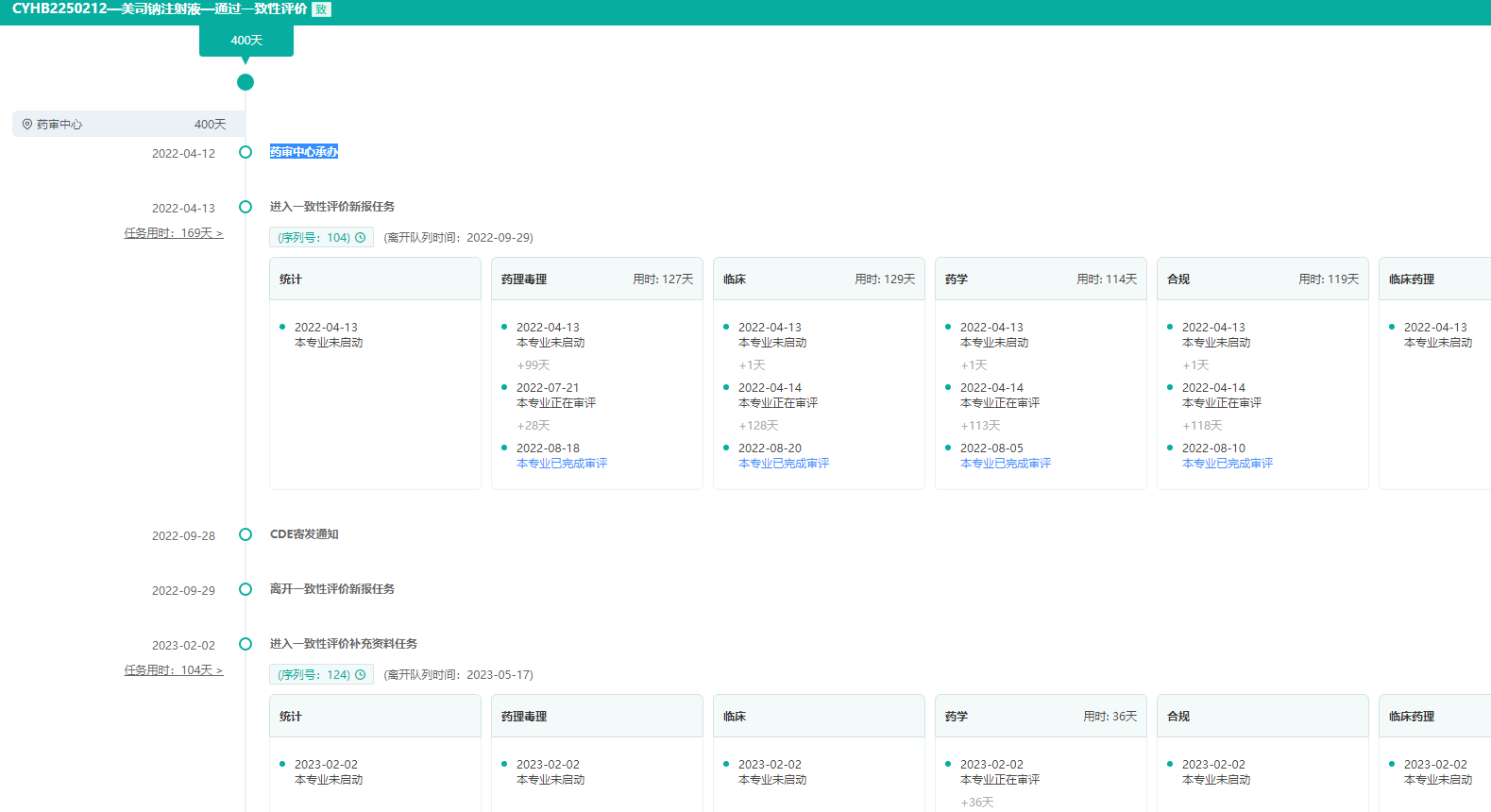
图片来源:药融云中国药品审评数据库
恒瑞医药在仿制药首家过评方面,据药融云一致性评价数据库统计,截至目前,恒瑞医药及子公司已经有52款仿制药首家过评,涉及36个品种,包括加巴喷丁胶囊、卡培他滨片、吸入用七氟烷、帕立骨化醇注射液、注射用醋酸卡泊芬净、注射用环磷酰胺、钆特酸葡胺注射液、盐酸右美托咪定氯化钠注射液、酒石酸布托啡诺注射液等;其中,已进入国家医保目录品种30个。
从治疗领域来看,这些首家过评的药物主要为抗肿瘤药和免疫机能调节药、神经系统用药、心血管系统用药、消化系统与代谢药等,其中抗肿瘤药和免疫机能调节药占比32.07%,排名第一,其次是神经系统用药,占比22.64%。
恒瑞医药首仿药品治疗领域布局

图片来源:药融云一致性评价数据库
恒瑞医药作为国内的“创新药一哥”,创新药是其抢占更多市场、未来拉动业绩的关键。但在大力发展创新药之余,恒瑞对优质的仿制药市场仍继续开拓,高端仿制药与创新药研发并举,仿创结合,可以满足更多目前尚未被满足的临床需求,从而造福患者。
二、尼莫地平注射液——预防和治疗缺血性神经损伤
广东科伦药业的尼莫地平注射液以补充申请获批过评,成为其首家过评企业。药融云数据库显示,目前国内已上市的尼莫地平有尼莫地平片、尼莫地平胶囊、尼莫地平软胶囊、尼莫地平缓释片、尼莫地平缓释胶囊、尼莫地平分散片、注射用尼莫地平、尼莫地平注射液,尼莫地平口服溶液等11种制剂。
尼莫地平注射液主要用于预防和治疗动脉瘤性蛛网膜下腔出血后脑管痉挛引起的缺血性神经损伤;也用于轻、中度原发性高血压,如合并脑血管疾病者,还可用于血管性头痛、缺血性突发性耳聋、多型痴呆。
药融云数据库显示,2021年在全国医院终端市场尼莫地平注射液的销售规模达到4.76亿元,同比上涨2.66%;其中,拜耳的市场份额最大,占据73.45%;其次是辰欣药业和青岛金峰制药排第二、三位,分别占据9.78%、6.17%的市场份额。
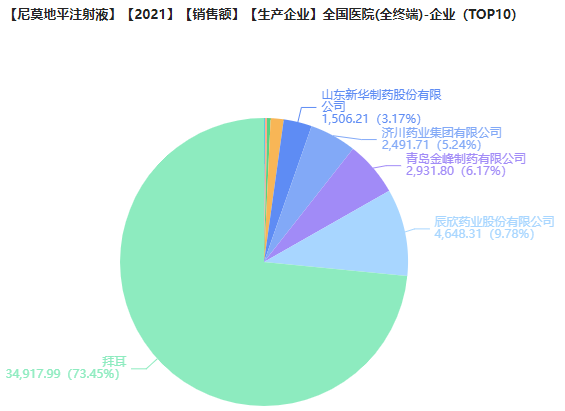
图片利用:药融云全国医院销售(全终端)数据库
尼莫地平最早由德国拜耳公司以尼莫地平片(Nimotop)上市,为原研制剂。目前,在中国上市的尼莫地平拥有227个生产批文,在使用的160个;涉及11个品种,145家生产企业;其中获批品种数排名前五的企业,分别是亚宝药业、普利制药、新华制药、拜耳、天致药业。
其中,尼莫地平注射液有83个生产批文,在使用的有57个,涉及40家生产企业。药融云数据库显示,目前,普利制药和济川药业的一致性评价补充申请还在审评审批中,汇宇制药、北京柏雅联合、辽宁亿帆药业、北京百美特生物4家均以仿制4类报产在审。
尼莫地平注射液审评情况查询(部分,完整内容请登录“药融云数据库www.pharnexcloud.com/?mh”查看)
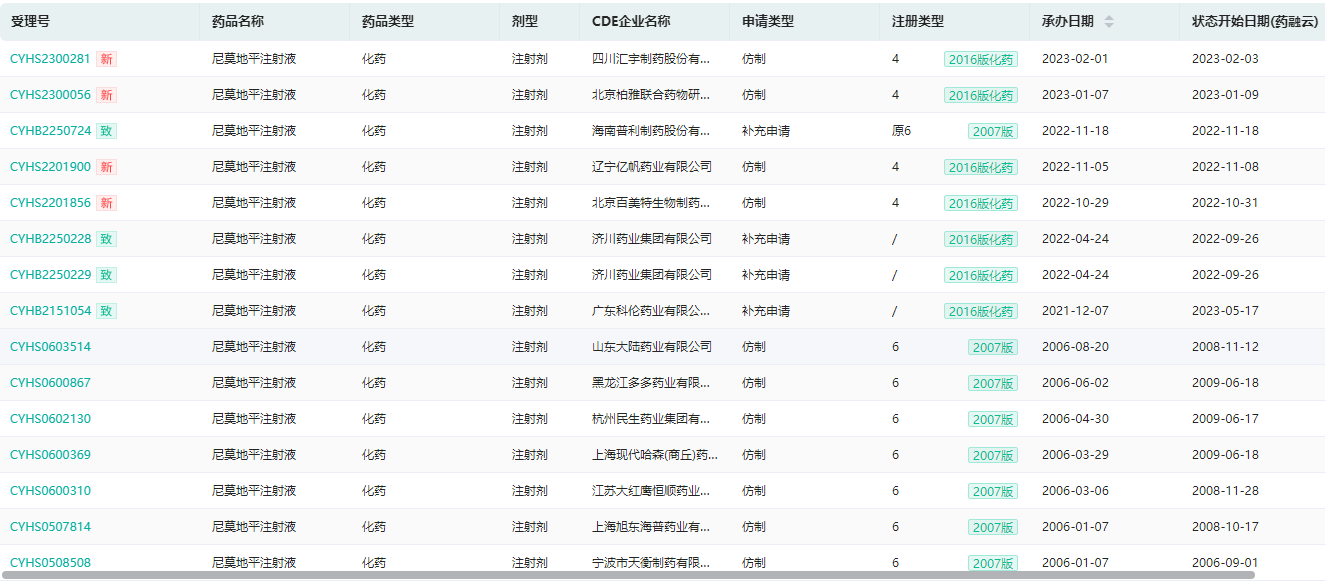
图片来源:药融云中国药品审评数据库
三、奥拉帕利片——PARP抑制剂
齐鲁制药的奥拉帕利片以仿制4类报产的奥拉帕利片获批生产,为该品种的国内首仿+首家过评。
药融云数据库显示,阿斯利康/默沙东的奥拉帕利是全球首款获批上市的口服多腺苷二磷酸核糖聚合酶(PARP)抑制剂,最早于2014年先后在欧盟和美国获批上市。2018年8月,获NMPA批准上市,是国内首个上市的PARP抑制剂;2019年通过谈判纳入全国医保乙类目录。
奥拉帕利通过抑制PARP酶活性和防止PARP与DNA解离,协同DNA损伤修复功能缺陷,杀死肿瘤细胞。目前已相继斩获卵巢肿瘤、转移性乳腺癌、输卵管恶性肿瘤、腹膜或腹膜后肿瘤、卵巢转移性恶性肿瘤、激素抵抗性前列腺癌等多项适应症。
奥拉帕利不同适应症研发情况查询
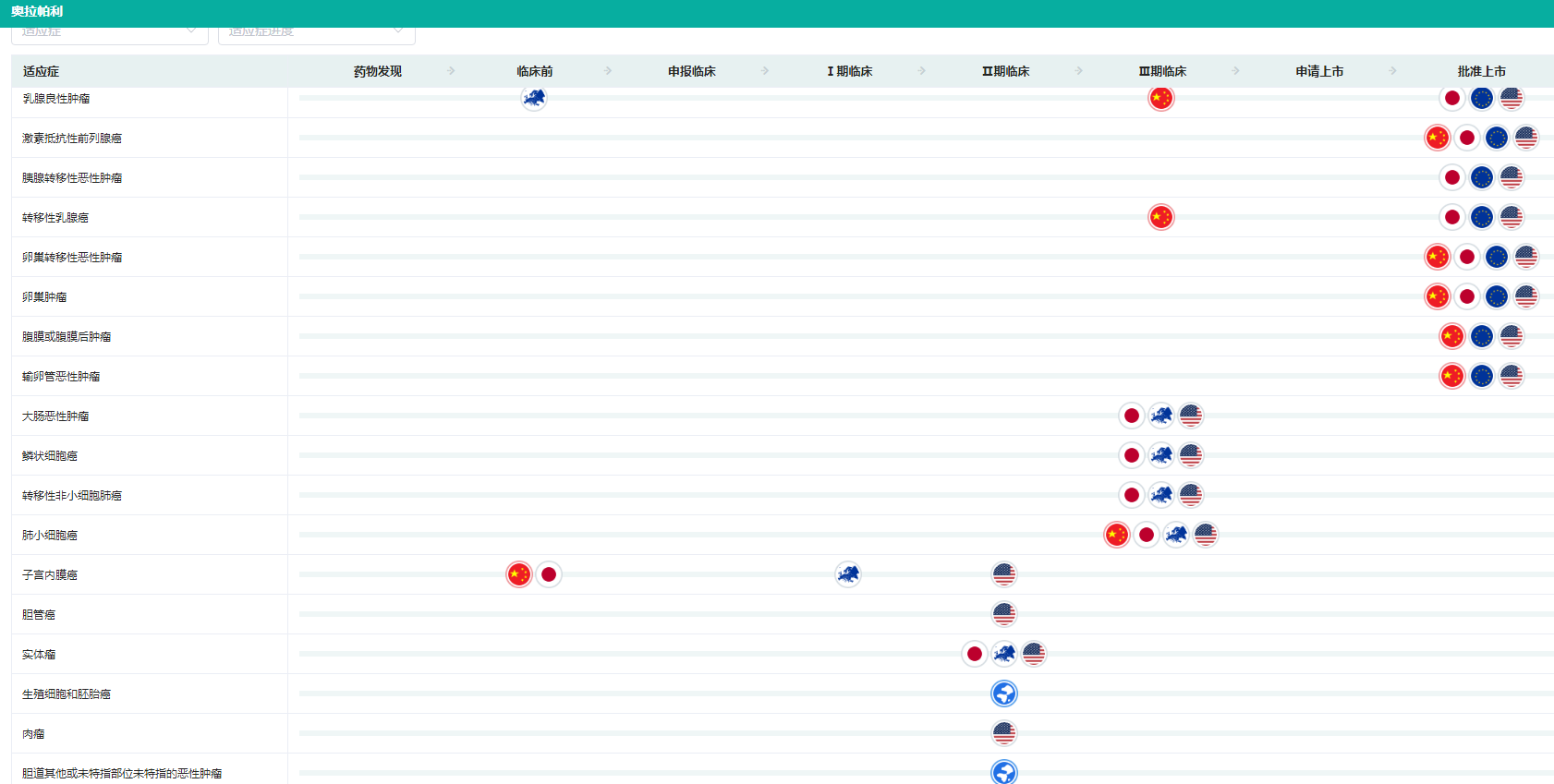
图片来源:药融云全球药物研发数据库
据阿斯利康财报显示,2022年奥拉帕利全球销售额已达26.38亿美元。在国内医院终端市场,近年来奥拉帕利的销售额逐年上涨,2022年已突破10亿元大关。
在仿制药过评方面,截至目前,齐鲁制药共有123个品种通过或视同通过一致性评价,其中有50个为国内首家过评,包括盐酸昂丹司琼注射液、依托考昔片、来那度胺胶囊、利培酮口崩片、哌柏西利胶囊、培唑帕尼片、地夸磷索钠滴眼液、恩扎卢胺软胶囊等。
药融云一致性评价数据库显示,齐鲁制药以93个品种领跑通过/视同通过一致性评价排行榜,石药集团欧意药业则以79个品种位列第二,其次是扬子江药业以68个品种排名第三,倍特药业、科伦药业紧随其后。
仿制药过评品种数量TOP10企业
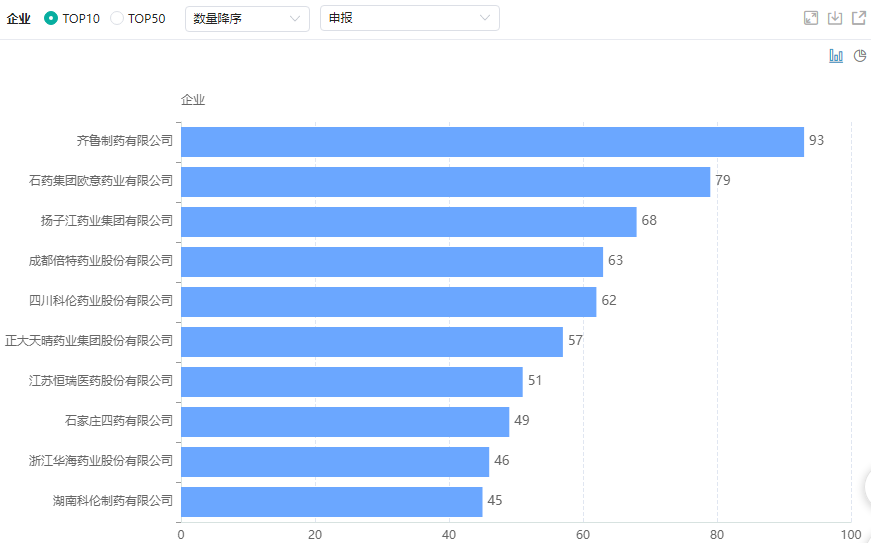
图片来源:药融云一致性评价数据库
随着药品带量采购和仿制药一致性评价的推进,药价下行压力持续加大,国内众多仿制药企布局一致性评价积极性提高,抢先过评、拿下集采中选资格。仿制药淘汰赛后产能会更加集中,活下来的企业可以获得较稳定的回报。
无论您是在药企从事研发注册、商务拓展(BD)、战略研究,或是在风投、券商从事医药投资、行业分析,相信您都可以借助《药融云医药行业观察周报》,快速、高效地获取最核心的新药情报信息。
想要获取完整报告内容,请关注“药融云公众号(yrydata)”,后台回复关键词“报告”进行领取;或者前往“药融文库(wenku.pharnexcloud.com/?mh)”「原创报告」中进行全文下载。
想要解锁更多药品信息吗?查询药融云数据库(vip.pharnexcloud.com/?zmt-mhwz)掌握药品各国上市情况、药品批文信息、销售情况与各维度分析、市场竞争格局、一致性评价情况、集采中标情况、药企申报审批信息、最新动态与前景等,以及帮助企业抉择可否投入时提供数据参考!注册立享15天免费试用!

<END>
















































 浙公网安备33011002015279
浙公网安备33011002015279 本网站未发布麻醉药品、精神药品、医疗用毒性药品、放射性药品、戒毒药品和医疗机构制剂的产品信息
本网站未发布麻醉药品、精神药品、医疗用毒性药品、放射性药品、戒毒药品和医疗机构制剂的产品信息
收藏
登录后参与评论
暂无评论