2023年2月17日,Ligand Pharmaceuticals Incorporated (NASDAQ:LGND)宣布,其合作伙伴Travere Therapeutics, Inc. (NASDAQ: TVTX) 已经获得FDA对FILSPARI™ (sparsentan)的加速批准,用于降低原发性免疫球蛋白A肾病(IgAN)成年人的蛋白尿风险,通常是尿蛋白/肌酐比(UPCR)≥1.5g/g(创新药奇缺领域:这种罕见肾病将迎来重磅新药!)
该适应症基于蛋白尿减少而获得加速批准。Sparsentan是一种每日口服药物,旨在选择性靶向IgAN疾病进展中的两个关键途径(内皮素-1和血管紧张素II),是首个也是唯一一个获得治疗该病症非免疫抑制剂批准的药物。IgAN是一种罕见的肾脏疾病,也是由肾小球疾病引起的肾衰竭的主要原因之一,影响美国高达15万人,其中大约有3万到5万名患者符合加速批准适应症。
根据药融云www.pharnexcloud.com/?zmt-mhwz及企业公开信息,Sparsentan此前已在美国和欧盟获得治疗IgA肾病的孤儿药资格认定,并在美国获得优先审评资格。此外,欧洲药品管理局(EMA)已在2022年8月受理Sparsentan的有条件上市许可,预计将于2023年下半年做出审查决定。
截图自药融云数据库
FILSPARI的批准是在FDA加速批准途径下获得的,该途径基于在至关重要且正在进行的PROTECT研究中,与活性对照相比,在蛋白尿方面出现了临床上显著和统计学意义的改善。PROTECT研究是迄今为止IgAN最大的头对头干预研究,是一项全球性的、随机的、多中心的、双盲的、活性对照的临床试验,评估了404名18岁及以上的IgAN患者,这些患者尽管接受了最大耐受的ACE或ARB治疗,仍有持续的蛋白尿,比较了400mg FILSPARI和300mg缬沙坦的安全性和有效性。
药融云数据显示:根据Ligand与Travere关于sparsentan的许可协议,Ligand有权获得一笔净里程碑费用1530万美元,以及其他可能的里程碑付款和未来全球净产品销售的9%净版税。
Ligand的CEO Todd Davis表示:“我们非常高兴看到sparsentan,即FILSPARI的批准,这是改善患有IgA肾病患者生活的重要一步。我们与Travere的合作历程是非常值得一提的,我们为能够帮助将这种创新性治疗方法推向市场感到自豪。祝贺Travere团队取得这一成就。”

Ligand Pharmaceuticals Incorporated于1987年在特拉华州注册,于1997年在纳斯达克上市,是一家总部位于美国加州圣地亚哥的生物制药公司。公司致力于发现、开发和推广新的药物和治疗方法,特别是针对癌症和自身免疫疾病等难治性疾病的治疗方法。
截图来源:药融云投融资数据库
公司商业模式为:开发或收购能产生收益的资产,将其融合到精益企业的成本结构中。由于公司的商业模式是基于与其他制药公司合作,商业化利用并销售新药相关资产,因此公司不少收入来自合作伙伴提供的相关权益使用费。

图 | Ligand投资理论描述
Ligand很早就认识到了制药行业药物制剂开发的重要性,2011年,公司将Captisol药物递送平台并购(从CyDex公司获得)。CAPTISOL是一个功能强大的配方技术,拥有多个美国食品药品管理局/FDA批准的产品,包括Pfizer公司的VFEND IV、Baxter International公司的Nexterone、吉利德瑞德西韦、安进公司的KYPROLIS、Acrotech Biopharma L.L.C.和CASI Pharmaceuticals的EVOMELA、Melinta Therapeutics的BAXDELA®™和Sage Therapeutics的ZULRESSO™等等,以及其他一些在临床阶段投入使用的合作伙伴项目。
与同行的其他公司相比,公司已经组建了一个最大的行业多元化资产组合,在未来能产生显著的收益。资产组合中发展的治疗方案可以解决许多尚未得到解决的医疗需求缺口,包括肝炎、肌肉萎缩、老年痴呆症、血脂异常、糖尿病、贫血、哮喘、类风湿关节炎、和骨质疏松症。
Ligand是较为少见的license-out模式为主的新药开发公司,合作伙伴逾130多个,遍及世界500强各大药企,以及欧美亚多个国家的公司,在中国的合作方有华润双鹤、西安新通(科创板IPO过程中)、誉衡药业、基石药业、药明康德/药明生物等。
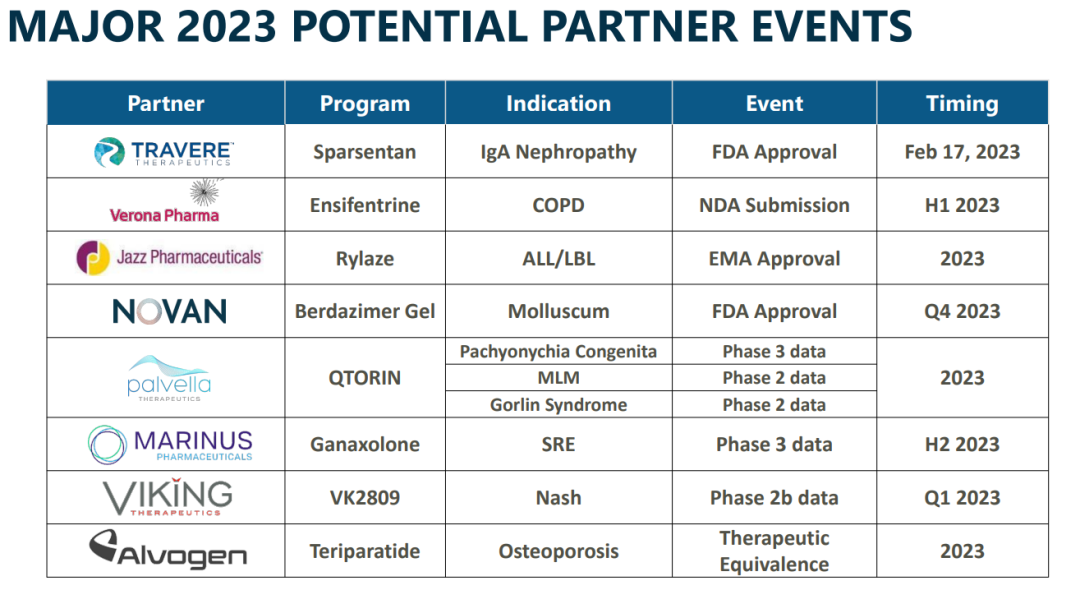
图|2023年Ligand潜力合作项目
2022年11月1日,Ligand完成了对子公司Omniab的预期免税分拆。在这之前,Ligand拥有多个具有潜力的产品和技术平台,其中包括Captisol药物递送技术、OmniAb技术、Pelican等。在剥离Omniab抗体发现业务后,该公司拥有两大技术平台:Captisol和Pelican。分拆后,Ligand公司150名员工中约有一半离开,据2022年12月13日公司发布的简报,现有员工人数为79人。

Todd C. Davis -Ligand现任CEO
2022年12月5日,Ligand宣布Todd C. Davis任职公司CEO,前CEO John Higgins于2022年12月31日辞去公司董事职务。Davis在生物制药和生命科学运营及投资领域拥有近30年的经验,拥有美国海军学院的学士学位和哈佛大学的MBA学位,是Palvella Therapeutics(一家私人生物制药公司)、Vaxart(一家上市生物技术公司)和ViroCell Biologics,Ltd.(一家私人生物技术公司)的董事会成员。
一、主要技术平台
- 01.Captisol

Captisol药物递送技术是一种受专利保护的化学修饰环糊精,其结构旨在优化药物的溶解度和稳定性。Captisol能够解决不溶解药物或者不稳定的药物活性成分在人体内的递送困难问题,将一些普通方法难以递送到患者血液的药物成功递送,并良好融入发挥效应。它的关键优势在于以下几点:
(1) 改善API的溶解度和配方:它允许配制所有剂型的不溶于水的API,包括口服、注射剂、眼科制剂、鼻腔给药、吸入制剂等。并且对于口服药物是无味的,对于鼻腔和吸入制剂而言还可以充当掩味剂。还可以减少可注射配方对注射部位的刺激。
(2) 提高生物利用度和递送效率:相比于纳米递送系统和溶剂系统而言,具有更好的生物利用度。进而能够降低需要递送的API的剂量。
(3) 药物起效快,能够帮助一些已经批准的口服药物更快地起效。
(4) 生产制造:明确的杂质分布和长期稳定性以提高安全性。
Captisol药物递送技术是由美国堪萨斯大学Higuchi生物科学中心的大学特聘教授Valentino Stella博士的实验室里的科学家发明的,最初是为了专门用于药物开发和制剂配方。这项独特的技术已经使一些FDA批准的产品成为可能。
- 02.Pelican

Pelican表达技术平台是一个重组蛋白生产平台,特别适合于传统系统不适合的复杂、大规模蛋白生产。该技术目前已被授权用于许多商业和开发阶段的候选新药项目。

该平台的多功能性已在生产酶、肽、抗体衍生物和工程非天然蛋白质方面得到证明。一些药企寻求该平台合作,因为它可以通过缩短开发时间和降低生产治疗药物和疫苗的成本,为生物制药开发项目贡献巨大商业价值。
二、剥离Omniab业务,Ligand完成分拆后焕然一新
2022年11月1日,Ligand完成其抗体发现业务及若干相关资产及负债的分拆,方式为按比例将Omniab分拆至Ligand于2022年10月26日登记在册的股东,并根据合并协议及分拆协议以反向莫里斯信托交易将Omniab与APAC的全资附属公司合并。交易前一天,Omniab更名为Omniab Operations,Inc.,APAC更名为Omniab,Inc.。

根据交易协议,Ligand向Omniab提供现金及构成Omniab业务的若干资产及负债,包括Ligand的若干相关附属公司。作为出资的对价,Omniab向Ligand发行了额外的Omniab普通股股份,以使当时发行在外的Omniab普通股股份数量等于进行分配所需的OmniAB普通股股份数量。根据分配,截至股权登记日,Ligand股东每持有一股Ligand普通股,将获得一股Omniab普通股。根据合并协议,每股Omniab普通股随后被交换为接收4.90007股新Omniab普通股和0.75842股新OmniAB普通股的权利(“Earnout股份”),这些股份受基于价格的获利能力触发机制的影响。
2022年11月2日,抗体药物发现公司OmniAB完成与SPAC公司AHPA的合并上市,该交易对OmniAB的估值约为8.5亿美元。由于面临收入挑战,Ligand对Omniab的分拆使Ligand的规模得到了适当的调整。
关于OmniAb®平台

OmniAB此前是Ligand(NASDAQ:LGND)旗下的抗体药物发现平台。2016年1月,Ligand以1.78亿美元现金加股票收购了Open Monoclonal Technology Inc,获得了OmniRat(转基因大鼠),OmniMouse(转基因小鼠)和OmniFlic(OmniRat的一个分支,可以用于开发双特抗),又在2017年收购了Crystal BioSciences的转基因鸡人源抗体平台,并改名为OmniChicken,在此基础上建立了OmniAb平台。OmniAb平台主要是依托于新型的锌指核酸酶技术ZFNs进行基因编辑,并结合B细胞单细胞筛选技术,以加速单抗的研发和生产。
OmniAb平台的核心是其专有转基因动物的Biological Intelligence™(BI),包括Omnirat、Omnichicken和Omnimouse,这些转基因动物经过基因改造,可产生具有人类序列的抗体,以促进人类候选治疗药物的开发。OmniFLIC(转基因大鼠)和OmNICLIC(转基因鸡)通过共同的轻链方法满足了双特异性抗体应用的行业需求,OmNITAUR具有奶牛抗体的独特结构属性,可用于复杂的靶标。OmniAb的技术套件涵盖了从双动力库生成到尖端抗体发现和优化,为全球制药行业不断增长的发现需求提供了高效和可定制的端到端解决方案。
三、主要产品与业务
下表是2022年前三季度Ligand的授权费、Captisol和合同收入的盈利情况(以千计),通过此数据对Ligand目前主要产品与业务情况进行分析:
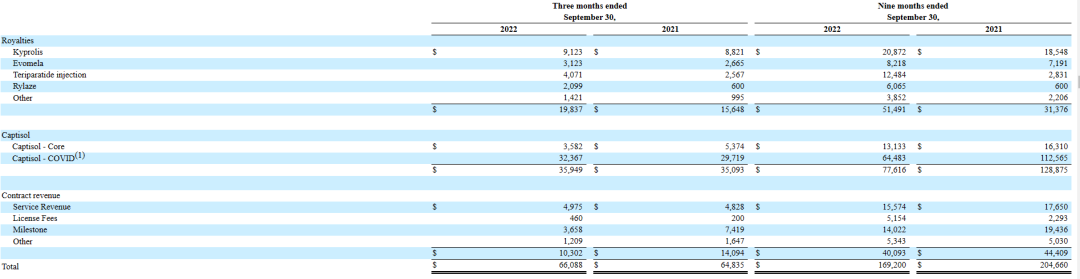
在Ligand公司官方公告中,公司表示其收入主要来自合作伙伴商业化的授权费、Captisol技术、服务合同收入、许可费和开发、监管和基于销售的里程碑付款。而对于Ligand来说,它的一个重要吸引力就在于它能够以降低的程度,参与到世界上最具生产力的几十个制药公司的药物开发经验中,这让Ligand及其投资者可以享受多重成功机会。
数据显示,在2022年前三季度,由Ligand技术实现的重要药物,也是给Ligand带来最多收入的,排名前四的是Kyprolis、Evomela、Teriparatide注射剂和Rylaze。在授权费、Captisol、合同收入这三大项主要营收来源中,Captisol可以说是Ligand最“有利可图”的资产。2022年,由于Ligand与吉利德(GILD)签订了有利的协议,为吉利德的COVID-19治疗药物Remdesivir/瑞德西韦提供Captisol作为关键成分,Ligand成功把握住了大流行环境中的机会。这笔交易给Ligand带来了3236.6万美元的回报,在Ligand上面的分解收入图表中,以“Captisol-COVID”作为迄今为止最大的一项单独列出。
同时,来自Captisol-COVID的超高收入也成为Ligand公司面临的巨大挑战。在2021年和2022年的第三季度中,Captisol-COVID盈利约占其总收入的一半。在2021年和2022年前三季度的收入中,这个比例有所改善,2022年前三季度的比例约为38%,较2021年的约55%有所下降。这个比例的差异是由于Captisol-COVID前三季度的收入从112,565美元降至64,483美元。来自Teriparatide注射和Rylaze的九个月授权费的大幅增长也在一定程度上帮助降低了Captisol-COVID的收入比例。
对于预计Captisol-COVID的收入在疫情结束后逐渐减少一事,Ligand一直非常坦诚。Ligand的前CEO Higgins曾表示:“Captisol-COVID在未来几个季度中的收入将逐渐降至零。”其实除了在Remdesivir中的作用,Captisol在其他一些被称为Captisol的治疗中也得到了应用,但数据显示Captisol-核心的收入远远小于Captisol-COVID的收入。
此外,合同交易是Ligand增长战略的重要组成部分。Ligand将交易达到了一种“机械化”的程度,将其融入了公司文化中。其经验丰富的中央交易团队通常每年审查约300个交易机会。通过各阶段的筛选,最终只剩下少数几笔真正的进展。
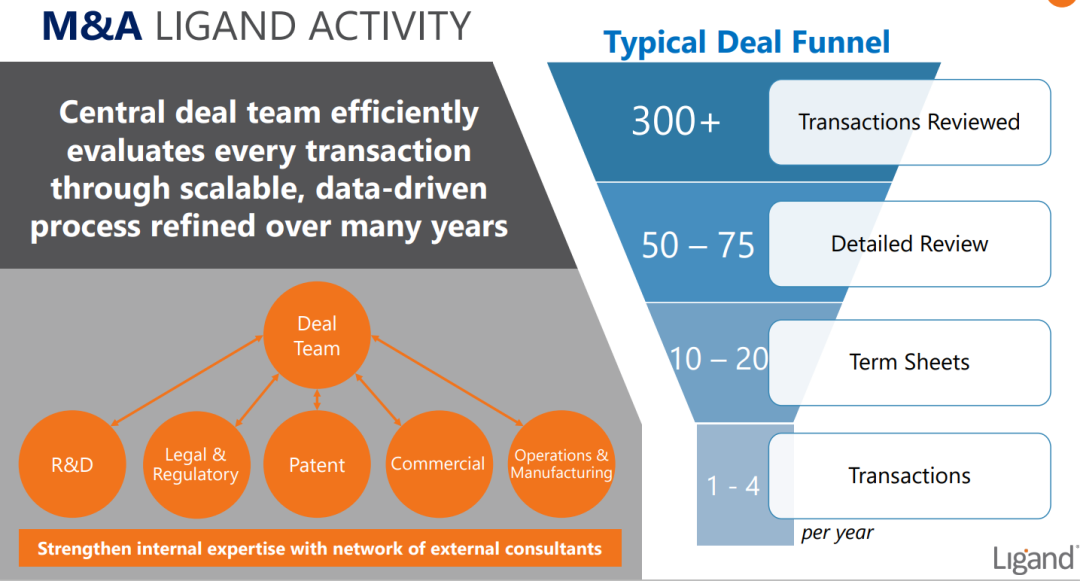
(Ligand交易筛选流程)
药融云数据vip.pharnexcloud.com/?zmt-mhwz显示:Ligand公司高效的交易产生了一系列合作管线,包括6个已获批准的项目,其中许多项目包括在其上述分类收入中。它的三个最重要的合作项目仍处于临床试验阶段,包括:
- Sparsentan是其与Travere Therapeutics公司合作开发的治疗IgA肾病的领先疗法,于2023年获得FDA批准,分析师一致认为2027年的特许权使用费收入约为6000万美元。
- Ensifentrine(PDE4新药)是维持治疗慢性阻塞性肺病的三期第一候选药物,与Verona Pharma (VRNA)合作,计划2023年提交FDA,分析师一致认为2028年版税收入约为1000万美元。
- Berdazimer凝胶,由Novan公司开发,作为软疣和寻常痤疮的局部治疗,预计近期将提交FDA,分析师一致认为2028年授权费营收约为1700万美元。
Ligand公司的上述收入潜力取决于FDA的批准,值得注意的是,Ligand基于特许权使用费的模式使其免受与开发这些疗法有关的费用。截至2022年12月13日,交易合作超过100个处于活跃阶段的项目,拥有经济利益。

(合作产品线概览)
四、财务表现
- 01.2021年年报
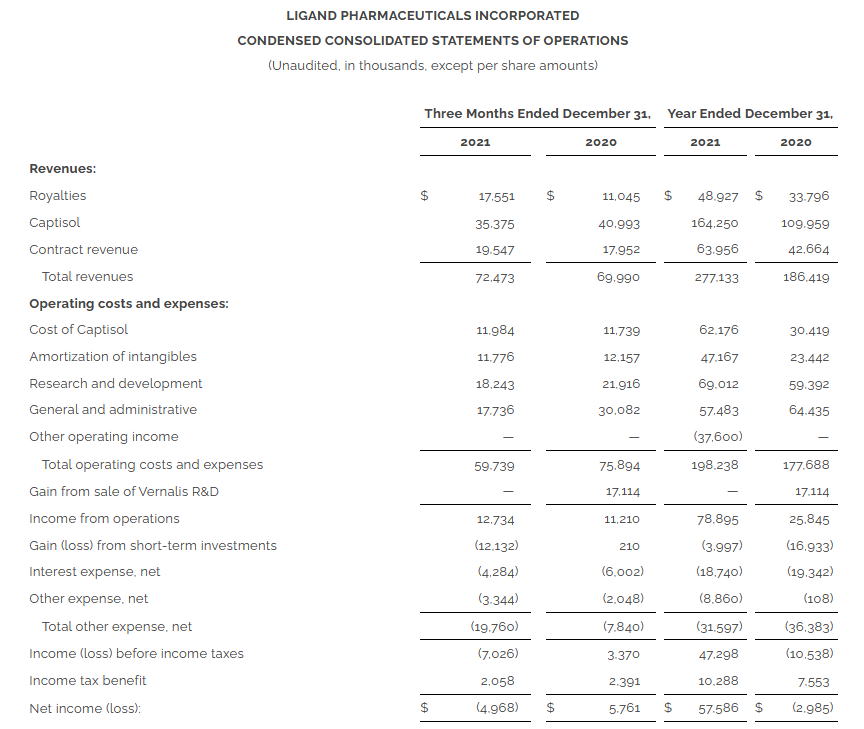
2021年财年Ligand公司总收入为2.771亿美元,同比上涨48.66%。
2021年,该公司授权费为4.89千万美元,增长主要归因于使用Pelican平台销售药品所产生的额外授权费;Captisol销售额为1.643亿美元,主要反映了与remdesivir使用的Captisol销售额增加;合同收入为6.4千万美元,增长主要归因于2020年4月收购Icagen和2020年10月收购Pfenex所带来的收入;其他营业收入为3760万美元,代表与消除剩余的Pfenex CVR负债相关的非现金估值调整。2021年净收入为5760万美元,每股摊薄收益为3.34美元。
- 02.2022年三季度报
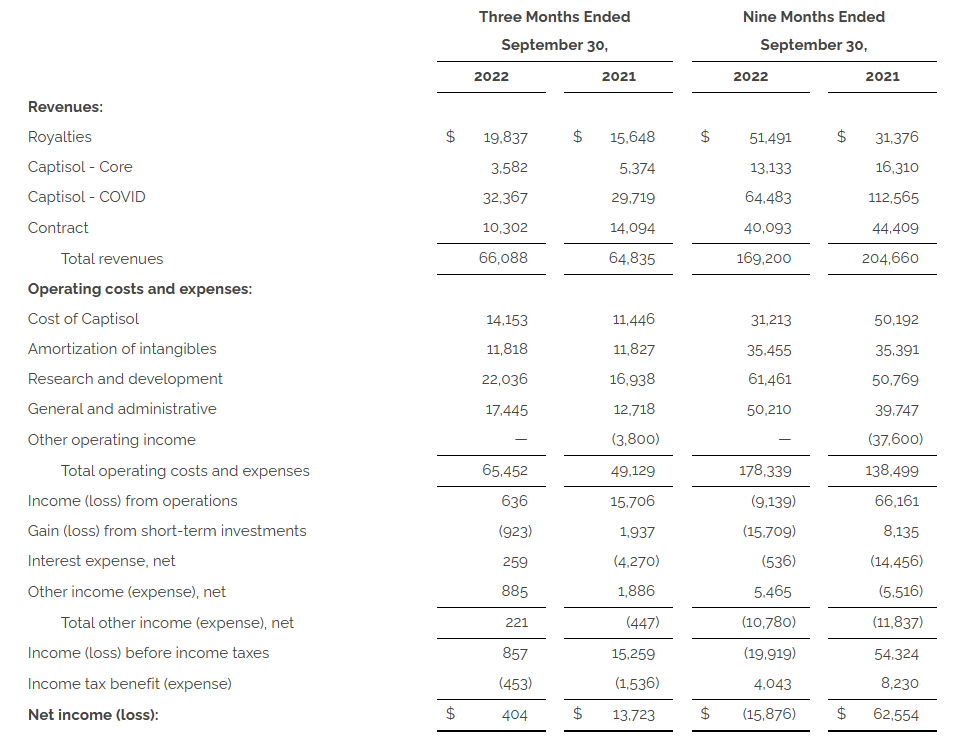
2022年前三季度,Ligand公司收入为1.692亿美元。Ligand净亏损为1590万美元,每股亏损0.94美元。除了由于消除剩余的Pfenex CVR负债而导致的非现金估值调整,没有其他运营收入。
- 其中专利费收入为5150万美元,主要是由于Kyprolis、Rylaze和Teriparatide等产品的贡献;
- Captisol-核心销售额为1310万美元,原因是客户订单的时间问题; Captisol-COVID销售额为6450万美元,系对疫情相关治疗的需求减少;
- 合同收入为4010万美元,原因是合作伙伴里程碑事件的时间差异而产生了变化;
- OmniAb业务收入为2330万美元。
成本支出方面,2022年9月30日止的Captisol成本为3120万美元,相比2021年同期的5020万美元下降,主要是由于Captisol总销售额下降;无形资产摊销费用为3550万美元,相比2021年同期的3540万美元基本持平;研发支出为6150万美元,相比2021年同期的5080万美元增长,主要是由于继续投资于OmniAb业务,包括设施和员工支出,以准备分拆;总行政支出为5020万美元,相比2021年同期的3970万美元增长,主要是由于与OmniAb的分拆有关的交易费用、与OmniAb相关的员工支出以及额外法律费用。
- 03.2022年全年财务

在拆分完成后,OmniAb将被视为已停止运营的业务,并因此在随后的所有财务报表期间将被排除在Ligand的报告收入和调整后的收益之外。因此,该财务展望不包括OmniAb的贡献。
Ligand预计2022年全年总收入为1.84亿美元至1.89亿美元,实际的财报显示业绩为1.96亿美元(2023年2月28日披露财报)。
其中,此前预计的授权费收入为6,600万美元至6,900万美元,Captisol销售额约1亿美元,合同收入为1,800万美元至2,000万美元。在预计的1亿美元Captisol销售额中,Ligand预计约1,500万美元归因于Captisol-核心销售,其余归因于用于COVID-19治疗。除去与COVID相关的Captisol销售,Ligand预计收入为9900万美元至1.04亿美元。
- 04.2023财务预期

2023年2月6日,Ligand公司推出了2023年的财务指引,具体如下:
- 总核心收入为1.18亿美元~1.22亿美元,同比增长约20%。(包括来自授权费的7,200万美元~7,600万美元、来自Captisol销售的2,100万美元(不包括与COVID相关的销售)和合同收入的2,500万美元)
- 运营现金支出为4,600万美元
- 现金流入5500万美元,调整后稀释每股收益为3.10美元至3.30美元,同比增长超过50%
- 2022年年底的资产负债表中包含的1.5亿美元现金和证券用于支持2023年的投资
此文仅用于向医疗卫生专业人士提供科学信息,不代表平台立场
参考:
NMPA/CDE;
药融云数据,vip.pharnexcloud.com/?zmt-mhwz;
FDA/EMA/PMDA;
相关公司公开披露(除标注外,正文图片均来自企业官方);
https://www.ligand.com/;
https://investor.ligand.com/press-releases/detail/482/ligands-partner-travere-therapeutics-announces-fda;
History of Ligand Pharmaceuticals Incorporated – FundingUniverse;
https://mp.weixin.qq.com/s/Xl3zfrrEY_dV4wvOcd86Zw;
A New Ligand Is Taking Shape (NASDAQ:LGND) | Seeking Alpha;
PowerPoint Presentation (d1io3yog0oux5.cloudfront.net);
https://www.sec.gov/Archives/edgar/data/886163/000088616322000030/lgnd-20211231.htm;
https://www.sec.gov/Archives/edgar/data/886163/000088616322000135/lgnd-20220930.htm;等等。
想要解锁更多药企信息吗?查询药融云数据库(vip.pharnexcloud.com/?zmt-mhwz)掌握药企公司基本信息、投融资情况、产品管线分布、药物销售情况与各维度分析、药物研发情况、年度报告、最新进展动态、临床试验信息、市场规模与前景等,以及帮助企业抉择可否投入时提供数据参考!注册立享15天免费试用!

<END>























































 川公网安备51019002008863号
川公网安备51019002008863号 本网站未发布麻醉药品、精神药品、医疗用毒性药品、放射性药品、戒毒药品和医疗机构制剂的产品信息
本网站未发布麻醉药品、精神药品、医疗用毒性药品、放射性药品、戒毒药品和医疗机构制剂的产品信息
收藏
登录后参与评论
暂无评论