
2023年1月31日,辉瑞公司公布了2022全年营收数据,达到了创纪录的1003亿美元。其中多款明星药物达到重磅药物级别,其中CDK4/6抑制剂Ibrance(爱博新,哌柏西利)2022年全球销售额为51.2亿美元,同比下降6%。哌柏西利中国化合物专利于2023年1月10日到期,截止目前已经有13个哌柏西利胶囊的仿制药批文获批,庞大乳腺癌市场,仿制药与原研混战局面一触即发。
通过药融云中国批文数据库最新数据显示,目前已经有5个国内厂家获得了哌柏西利胶囊的仿制药批文,分别是齐鲁制药(获得首仿)、江苏豪森药业、江西山香药业(青峰医药子公司)、江苏奥赛康和科伦药业子公司。
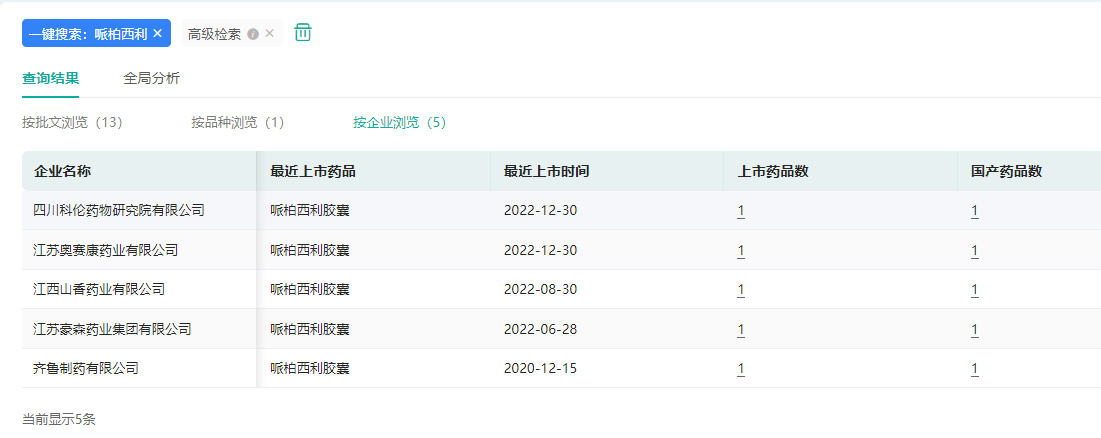
来源:药融云中国批文数据库
一、全球首款CDK4/6抑制剂
2015年2月3日,辉瑞全球首款CDK4/6抑制剂新药哌柏西利(Ibrance)获得美国FDA获批上市,批准用于激素受体阳性、人表皮生长因子受体-2(HER-2)阴性进展期乳腺癌的一线、二线治疗,同年便取得7.23亿美金全球销售额,到2021年,哌柏西利全球销售额已经达53.92亿美元(预计本年销售额为峰值),2022年该药全球销售额为51.2亿美元,呈现下降趋势。2018年7月辉瑞的哌柏西利胶囊获国家药监局批准上市。2019年11月,辉瑞开发的另一口服剂型哌柏西利片获美国FDA批准上市;2022年8月,辉瑞25mg、125mg的哌柏西利片获批在国内上市。
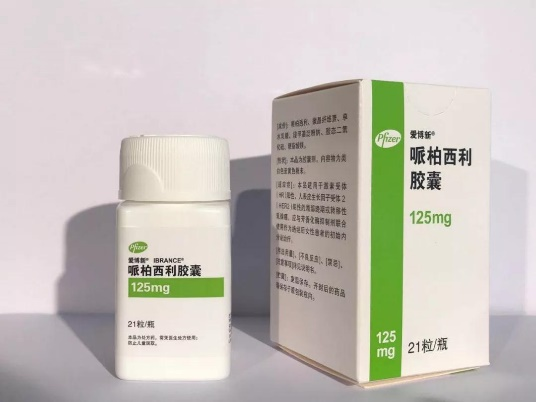
乳腺癌是全球第一大癌。据世界卫生组织统计,2020年,全球乳腺癌新发病例高达226万例,超过了第二大癌症——肺癌的220万例。在中国,2020年42万例的乳腺癌新发病例占据了女性新发癌症病例数的五分之一,位居女性高发癌症首位。2020年有12万女性因乳腺癌死亡。CDK4/6抑制剂的确改变了HR+/HER2-乳腺癌患者的治疗结局,可以有效克服或延迟内分泌抵抗的出现,为患者争取更长的生存时间。
哌柏西利在中国上市主要基于多项国际多中心III期研究结果(PALOMA-1,2,3),PALOMA-2是一项全球多中心、随机双盲、安慰剂对照的III期临床研究,纳入666例绝经后未经晚期系统性治疗的ER阳性HER2阴性晚期乳腺癌患者,主要研究终点是由研究者评估的无进展生存期(PFS),次要终点包括总生存期(OS)、客观缓解率、临床获益、患者报告结局及安全性。中位随访38个月,PAL+LET组相比对照组,显著改善mPFS(27.6 vs 14.5个月;HR=0.563),且所有亚组患者均获益;在有可测量疾病的患者中,PAL+LET的ORR为55.3%,PBO+LET的ORR为44.4%(odds ratio 1.55[1.05–2.28];P=0.03);PAL+LET长期使用没有累积的毒性;维持了生活质量。
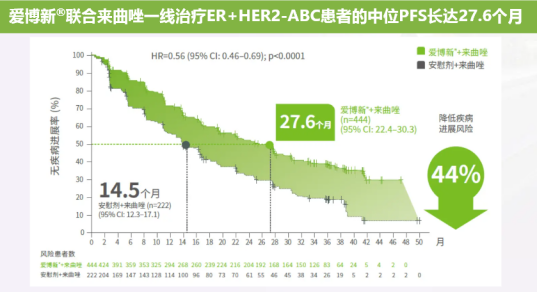
二、哌柏西利胶囊三个规格均满足3+1!集采或将到来
2023年1月18日,国家医保局发布了最新的2022版医保药品目录(2023年3月1日开始生效),共有14个抗癌新药首次进医保,其中包括4个治疗乳腺癌的新药,分别是:哌柏西利胶囊(CDK4/6抑制剂)、注射用恩美曲妥珠单抗(HER2/TUBR抑制剂)、达尔西利片(CDK4/6抑制剂)、优替德隆注射液。其中哌柏西利胶囊的最新价格已经公布,相比之前大幅度降价。进医保之前,哌柏西利胶囊的价格是9238元每盒(75mg/粒)、11520元每盒(100mg/粒)、13668元每盒(125mg/粒)。哌柏西利胶囊进医保后的价格已经公布,最新价格是:2891.7元每盒(75mg/粒)、3604.23元每盒(100mg/粒)、4275.6元每盒(125mg/粒)。
进医保后,哌柏西利胶囊的价格降幅达到68.7%,确实是大降价进医保。根据哌柏西利胶囊的推荐用量,按照70%的报销比例计算,医保报销后每个月费用只需1282元!
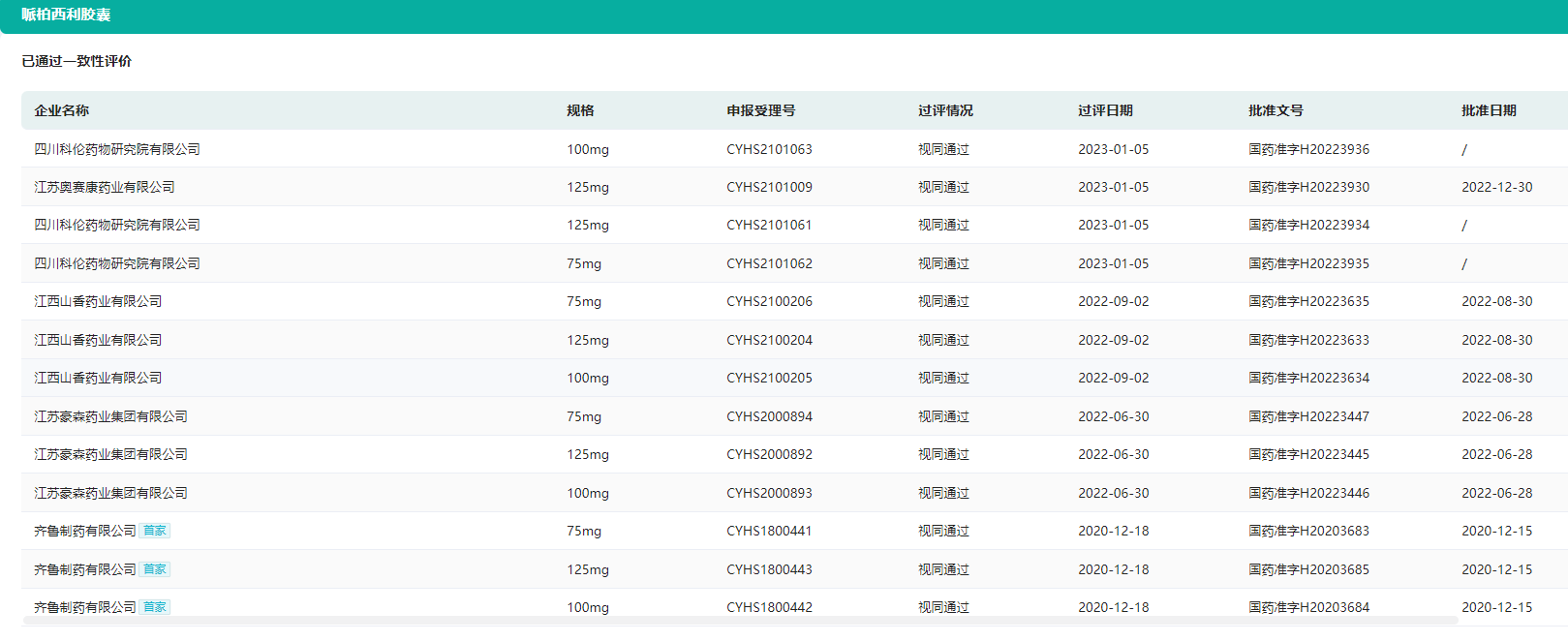
来源:药融云一致性评价数据库
根据药融云一致性评价数据最新数据,截止目前,哌柏西利胶囊的75mg规格处于4+1的竞争格局(4家国产+1家原研),100mg规格处于4+1的竞争格局,125mg规格处于5+1的竞争格局,均已经满足了集采条件,进入国家集采是迟早的事情。
三、哌柏西利的片剂已被盯上!多家CDK4/6抑制剂新药加入战局
哌柏西利片,目前国内仅有原研厂家辉瑞获批上市。2022年4月18日,齐鲁制药提交了哌柏西利片的上市申请;同年12月24日,石药集团欧意药业提交了上市申请,预计2023年均可获批。
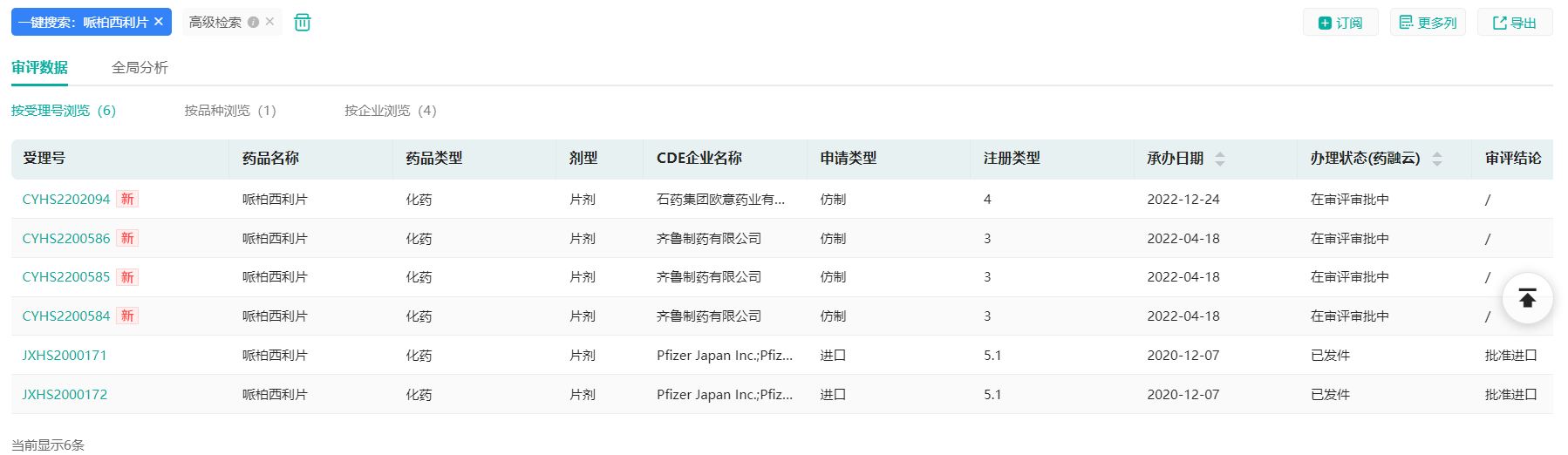
来源:药融云中国药品审评数据库
截至目前,国内共有5款CDK4/6抑制剂获批上市,即辉瑞的哌柏西利、礼来的阿贝西利、恒瑞医药自主研发的达尔西利、先声药业引进的曲拉西利和诺华的瑞波西利。另外根据药融云药品研发数据库,国内已有40多家企业布局了CDK4/6抑制剂赛道,正大天晴、贝达药业等多家知名企业均已入场,市场红海在即。
参考来源:
[1] 辉瑞年报
[2] 药融云数据库
想要解锁更多药品信息吗?查询药融云数据库(vip.pharnexcloud.com/?zmt-mhwz)掌握药品各国上市情况、药品批文信息、销售情况与各维度分析、市场竞争格局、药企申报审批信息、最新动态与前景等,以及帮助企业抉择可否投入时提供数据参考!注册立享15天免费试用!

<END>






















































 川公网安备51019002008863号
川公网安备51019002008863号 本网站未发布麻醉药品、精神药品、医疗用毒性药品、放射性药品、戒毒药品和医疗机构制剂的产品信息
本网站未发布麻醉药品、精神药品、医疗用毒性药品、放射性药品、戒毒药品和医疗机构制剂的产品信息
收藏
登录后参与评论
暂无评论