
一月,江苏恒瑞医药多款糖尿病新药迎来重大进展,标志着恒瑞医药在300亿糖尿病市场又向前迈进了一大步。目前恒瑞医药共有5款糖尿病药物进入医保,已上市的糖尿病新药有1款为SGLT2抑制剂恒格列净;处于申报上市阶段的有3款,分别是恒格列净二甲双胍缓释片(2.3类)、DPP-4抑制剂瑞格列汀和瑞格列汀二甲双胍片。另有10余款糖尿病新药已进入临床阶段。

一、2款DPP-4糖尿病新药冲刺上市
二甲双胍被许多临床实践指南推荐为2型糖尿病患者的首选治疗药物,但许多患者会对二甲双胍产生耐受,因此开发合适的联合用药产品变得更加重要,联合用药有望达到更好的临床疗效。
药融云数据库显示,尽管国内进口的6款DPP-4 抑制剂已有多款仿制药获批,但国产DPP-4抑制剂创新药尚无品种获批上市,其中进展最快的当属恒瑞医药,已有2款新药递交上市申请。
1月13日,CDE官网显示,恒瑞医药1类化药新药瑞格列汀二甲双胍片(Ⅰ/Ⅱ)上市申请获受理,用于治疗2型糖尿病。加上恒瑞医药2020年递交的磷酸瑞格列汀片,目前恒瑞医药共有2款糖尿病新药已申报上市。
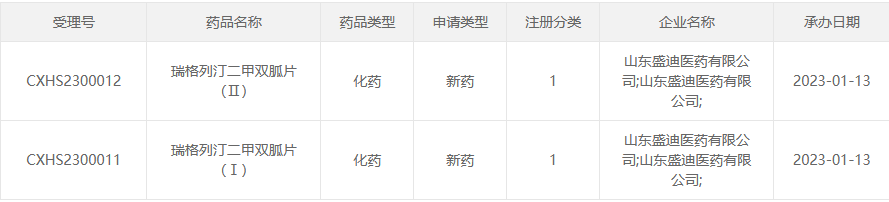
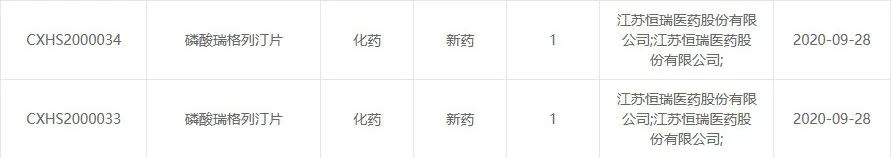
截图来源:CDE官网
瑞格列汀二甲双胍片(HRX0701)是恒瑞医药开发的二肽基肽酶Ⅳ(DPP-4)抑制剂磷酸瑞格列汀与盐酸二甲双胍固定剂量复方制剂,通过两种不同作用机制达到更好的降血糖作用,同时提高患者用药的依从性。
恒瑞医药的DPP-4抑制剂磷酸瑞格列汀片已于2020年9月向NMPA递交上市申请并获受理。该药物结构上与西格列汀相似。同时期报产的脯氨酸恒格列净片赶在了2021年底最后一天获批上市,成为中国首个自主研发的SGLT-2糖尿病新药,瑞格列汀能否在今年获批令人关注。
二、又一糖尿病新药进入III期临床,15款共同加注这一领域
1月17日,恒瑞医药的长效胰岛素糖尿病新药——INS068启动III期临床,这是一项随机、开放、平行对照的多中心临床研究,旨在比较INS068注射液和甘精胰岛素在基础胰岛素治疗血糖控制不佳的2型糖尿病患者中的有效性和安全性。
1月26日,INS068还在Clinicaltrials.gov网站上注册了INS068的三期临床,该三期临床计划入组501例二型糖尿病患者,与甘精胰岛素头对头对照。
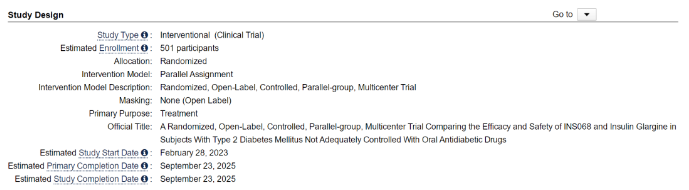
截至目前,恒瑞医药已有15款糖尿病新药进入IND及以上阶段。在生物制剂领域,恒瑞医药布局了长效胰岛素INS068、长效胰岛素/GLP-1复方制剂HR17031、GLP-1类似物诺利糖肽;在如今降糖领域研发热门方向GLP-1/GIP双靶点激动剂方面,恒瑞医药同样做了布局。详情见下方表格。
恒瑞医药主要糖尿病新药
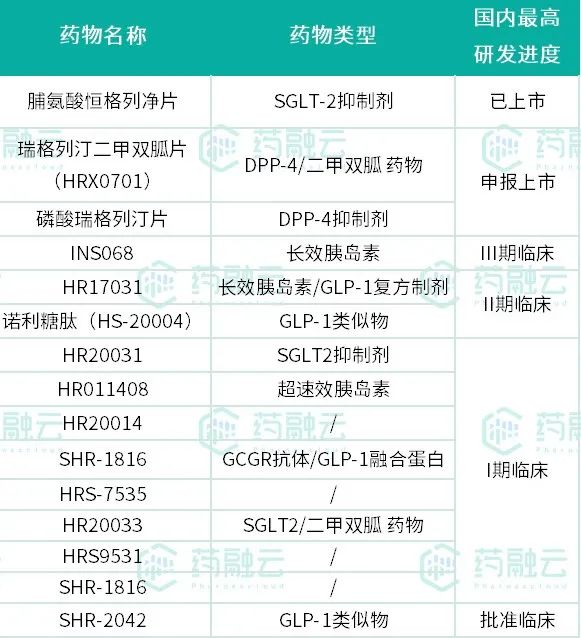
数据来源:药融云数据库,恒瑞医药企业财报
三、恒格列净进医保,“以价换量”猛攻300亿糖尿病市场
1月19日,恒瑞医药发布公告,其脯氨酸恒格列净片(商品名:瑞沁)正式被纳入《国家基本医疗保险、工伤保险和生育保险药品目录(2022年)》,为乙类药品,用于改善成人2型糖尿病(T2DM)患者的血糖控制。新版目录将于2023年3月1日起正式执行。

截图来源:恒瑞医药企业公告
作为新型SGLT-2i,恒格列净结构优化,结构中引入氟原子及L-脯氨酸基团,显著提高受体选择特异性,疗效和安全性更优。此次纳入医保,瑞沁有望成为恒瑞医药业绩增长的又一助力。
至此,恒瑞医药累计纳入国家医保的产品已有93个,除了此次的糖尿病新药脯氨酸恒格列净片外,还有罗格列酮片(独家)、盐酸二甲双胍缓释片、格列齐特缓释片和格列喹酮片等4个糖尿病用药也被纳入医保。
据药融云数据库显示,中国糖尿病市场(化学药/生物药)院内销售额由2014年200亿元增长到2021年343亿元,年复合增长率为7.99%(《2022年糖尿病新药研发!内卷加剧,药企合力进攻300亿院内市场》)。
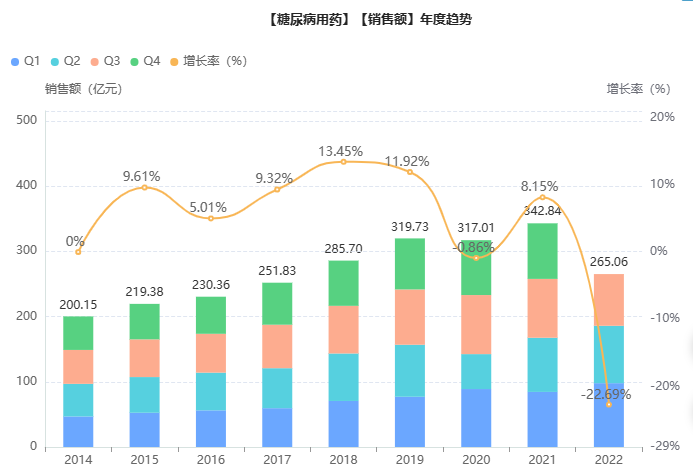
截图来源:药融云全国医药销售数据库
而从企业来看,目前在糖尿病药物领域,国内市场主要还是由诺和诺德、赛诺菲、阿斯利康等跨国药企占领,本土药企则以甘李药业、通化东宝、杭州中美华东制药等领跑。恒瑞医药大力布局糖尿病市场,力求多得一席之地,目前可以说已迈出了其糖尿病新药商业化的第一步。
参考来源:
[1] CDE官网
[2] 药融云数据库
[3] 恒瑞医药官方公告
想要解锁更多药企信息吗?查询药融云数据库(vip.pharnexcloud.com/?zmt-mhwz)掌握药企公司基本信息、投融资情况、产品管线分布、药物销售情况与各维度分析、药物研发情况、年度报告、最新进展动态、临床试验信息、市场规模与前景等,以及帮助企业抉择可否投入时提供数据参考!注册立享15天免费试用!

—END—






















































 川公网安备51019002008863号
川公网安备51019002008863号 本网站未发布麻醉药品、精神药品、医疗用毒性药品、放射性药品、戒毒药品和医疗机构制剂的产品信息
本网站未发布麻醉药品、精神药品、医疗用毒性药品、放射性药品、戒毒药品和医疗机构制剂的产品信息
收藏
登录后参与评论
暂无评论